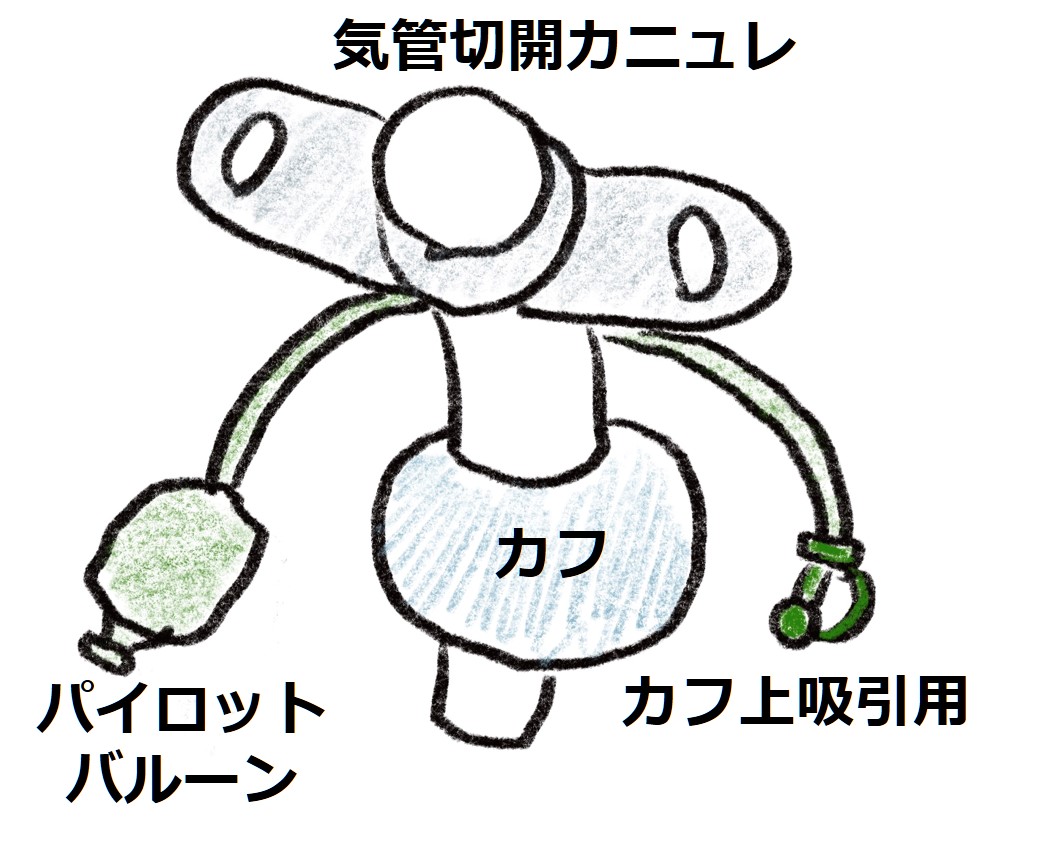
1:病態
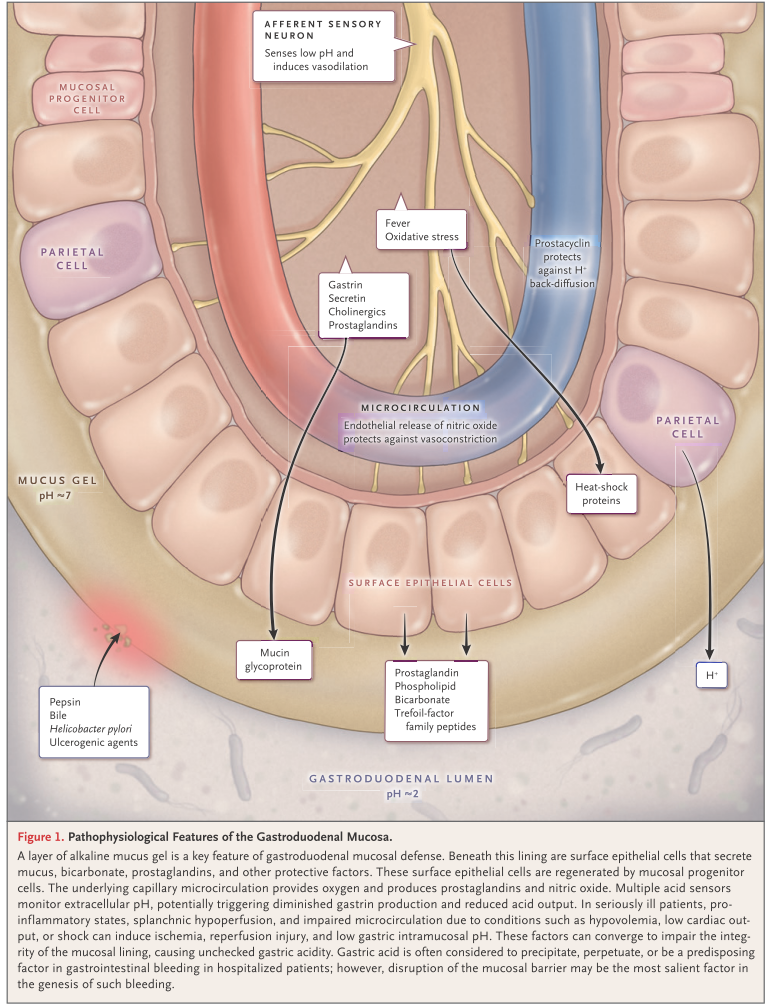
通常胃内はpH=2程度の強酸性で、このままの状態だと組織障害性が高いですが、胃粘膜を保護する粘液を産生することでバランスがとられています。普段胃への血流のうち70~90%が胃粘膜に供給されますが、ICUに入室するような重症患者は循環不全などで胃粘膜への血流不全がおこり、ストレス関連粘膜障害(SRMD: stress-related mucosal damage)が起こるとされています。消化管の血流不全に対する脆弱性として、
・消化管血流は”autoregulation”を備えていない
・交感神経刺激などで真っ先に血流が低下する(皮膚、消化管が代表)ことで、他の重要臓器へ血流を再分配する
などが原因として挙げられます。ストレス潰瘍(stress ulcer)はこのストレス関連粘膜障害の範疇です。ストレス潰瘍では、一般の胃潰瘍と異なり腹痛といった自覚症状に乏しい特徴があります。
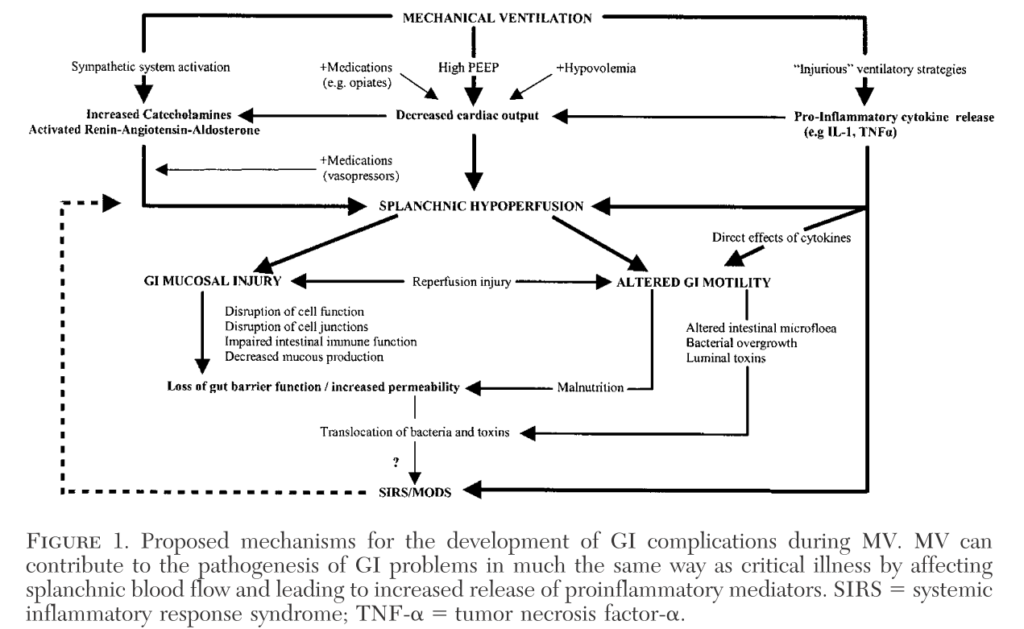
人工呼吸器は後で述べますがリスクとして特に重要で、機序としてはPEEPによる循環血症量の低下、カテコラミン放出やRAAS活性化による消化管血流低下、サイトカイン放出の影響などが示唆されています(下図)。
ICU入室24時間以内の患者の胃粘膜を確認すると75-100%で粘膜障害を示唆する所見を認めたと報告がありますが、実際に臨床上重要なのは内視鏡的止血処置や輸血を必要とするような出血(これをClinically important gastrointestinal bleedingを表現します)で重症患者の3%程度に認めるとされています(内科・外科一般床患者では0.2%程度)。この臨床上重要な消化管出血をどれだけ防ぐことが出来るのか?がテーマになります。ちなみに、粘膜びらん(erosion)と潰瘍(ulcer)の違いですが、びらんは浅い病変ですが、粘膜病変が深くなり粘膜下層まで及ぶと血管を障害し出血に至ります(下図)。
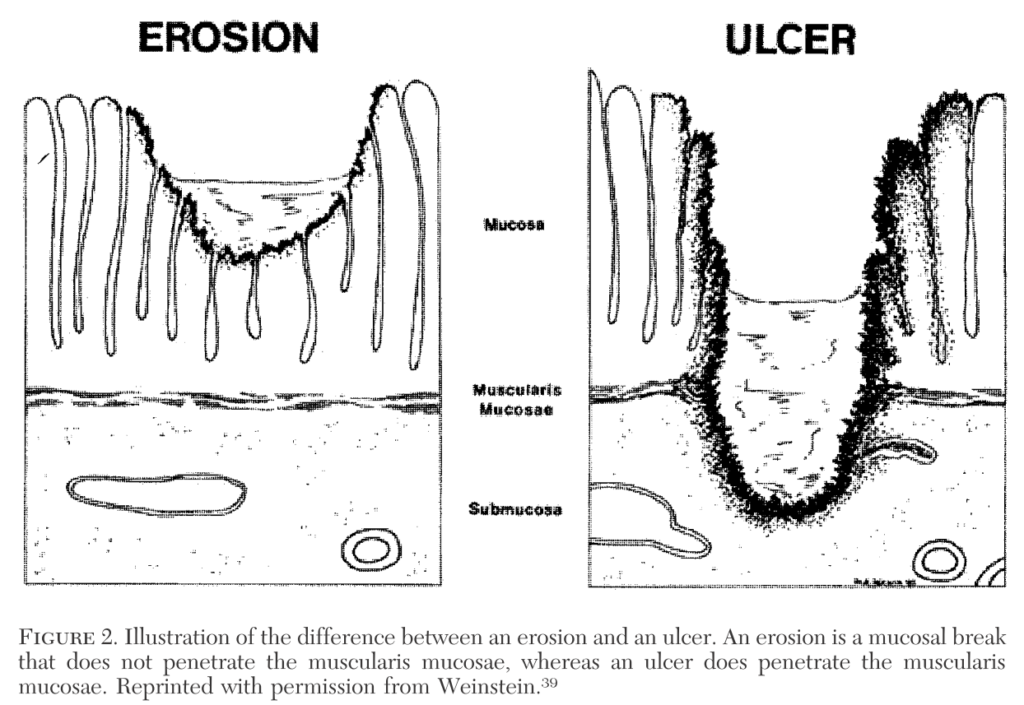
2:リスク
上記の病態を引き起こすリスクに関して解説します。
・48時間以上の人工呼吸管理(OR15.6, 95%CI, 3.0 to 80.1)
・凝固異常(PT-INR>1.5倍、APTT>正常上限2倍、血小板<5万/μLのうちいづれかに該当する)(OR4.5, 95%CI, 1.8 to 10.3)
この2つがリスクファクターの代表です(2252人のICU患者・前向きコホート・患者背景心臓血管術後48.5%と最多 NEJM 1994; 330:377 ストレス潰瘍のリスク因子を検討した論文としておそらく最も引用されている)。この研究では全体の1.5%にClinically important GIBを認め、上記リスクがいずれもない患者は0.1%、1つリスク因子があると3.7%であったと報告しています。その他以下のものがリスクとして挙げられています。
その他のリスク因子をまとめると下図のものが報告されています。
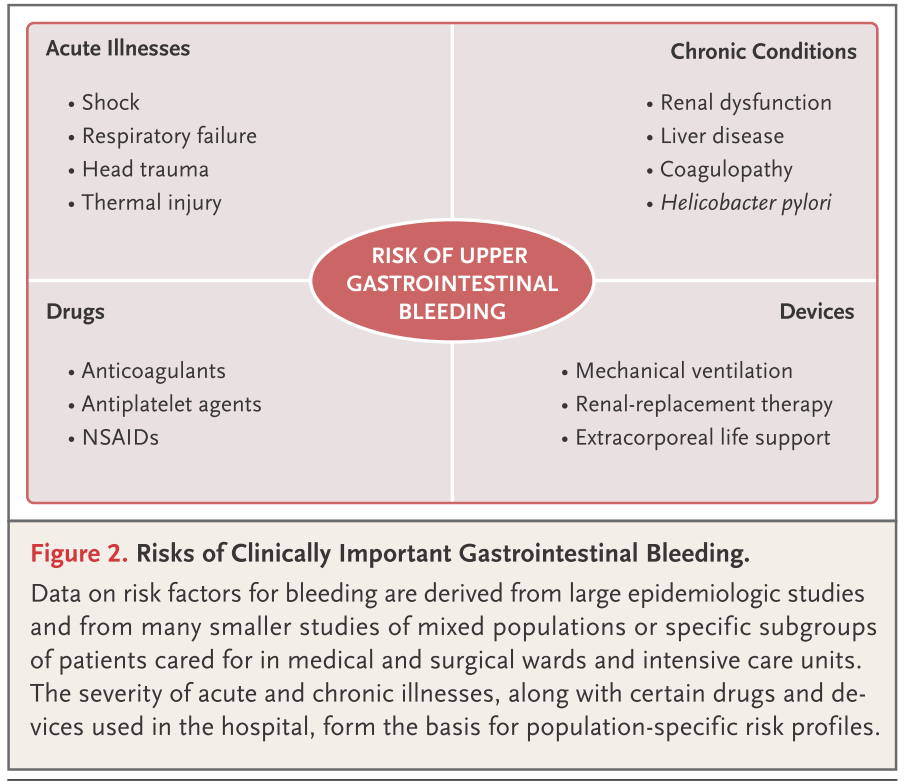
3:予防
■適応
難しい点はどのリスクファクターがある患者でストレス潰瘍予防をすれば良いか?という問いへの答えがまだ確立されていないことです。このため統一見解はなく、解釈は様々です(Up to dateとガイドラインとICU bookとCCMの最近reviewでもそれぞればらばらです)。Guidelineは古いものですが1999年発表されたものがあり、これが現在でも代表的なものです。その基準に則ると、
以下いずれかに該当する場合
・人工呼吸器管理が48時間以上
・凝固異常
もしくは、以下のリスク因子が2つ以上ある場合
・敗血症
・ICU滞在7日以上
・肝不全、腎不全
・頭部外傷GCS<10
・多発外傷
・広範囲熱傷(体表面積35%以上)
・臓器移植早期
・胃十二指腸潰瘍既往
・高容量ステロイド使用(ヒドロコルチゾン>250mg/日)
・脊髄損傷
が適応とされています。一般床入院患者はストレス潰瘍予防の適応ではないととされています。
■使用する薬剤
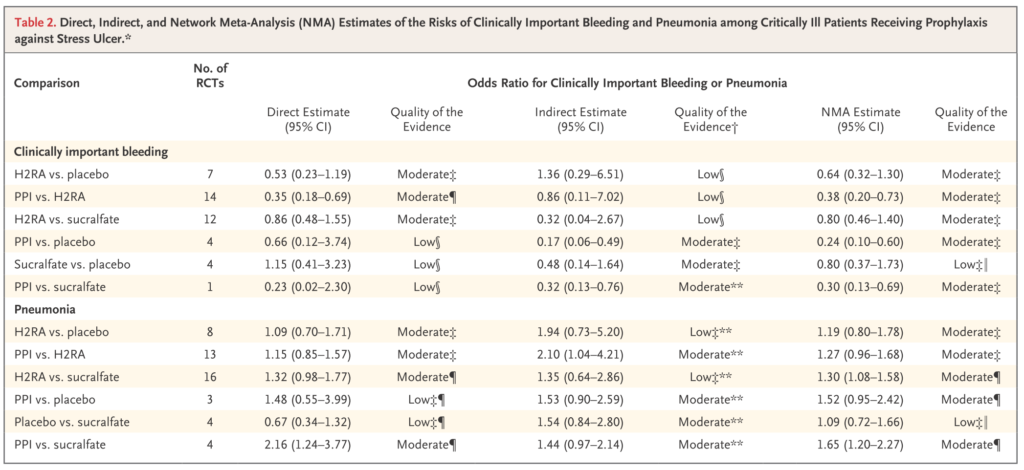
PPI・H2RA・胃粘膜保護(スクラルファート)が使用されます。予防効果としてはPPI > H2RA ≧ スクラルファートとなります。基本的にはPPI or H2RAを使用します。ただ、PPI, H2RAでは肺炎、CD腸炎のリスクが増加することが指摘されており、潰瘍予防効果が副作用を上回るかどうかが重要です。以下に具体的な処方例を提示します。
・PPI (proton pump inhibitor)
・オメプラゾール20mg 2T2x po or 20mg 1日2回 iv
・ランソプラゾール(タケプロン®)30mg 1T1x po
肝代謝なので腎機能障害による用量調節は必要ありません。
・H2RA (histamine2 receptor antagonist)
・ファモチジン(ガスター®)20mg 2T2x or 20mg 1日2回 iv
腎機能障害では薬剤量の調節が必要です。
・胃粘膜保護
・スクラルファート(アルサルミン®細粒)1g/包 1包4回(各食後+眠前)/日
薬剤相互作用が非常に多いため注意が必要です(キノロン系・ワーファリン・テトラサイクリン系・抗真菌薬・フェニトイン・テオフィリンなど)
・経腸栄養
薬剤ではないですが早期経腸栄養は消化管への血流を増加させるなどの機序でストレス潰瘍予防に有効かもしれないと報告されています。これは今後エビデンスが集積してくると思います。
■中止基準
リスク因子が解除された、もしくはICUを退出したタイミングで予防薬を中止するべきです。しかし、実際にはICU退出後も約60%が、退院後も約35%が不適切に予防薬を継続していたと報告されており(Crit Care Resusc 2013; 15:147)、きちんと開始するタイミングでいつ止めるかまで考えておくことが必要だと思います。漫然と長期処方にならないようにしたいです。
あとがき
予防薬の難しいところは、予防薬を使用しないで何かイベントが起こってしまった場合に「予防薬を使用しなかったせいだと」我々医療者が心理的に考えたくなってしまう点にあります(実際そのように責められることもあるかもしれません)。しかし、実際には予防薬を使用することでの害(具体的には肺炎・CD腸炎)もあるため、benefitとharmを天秤にかけた科学的判断が重要です。ストレス潰瘍予防に関しては現時点でまだ十分な質の高いエビデンスに乏しいですが、今までのストレス潰瘍予防が過剰であった(実際ICU患者の80-90%に処方されている)ため、きちんと適応を考えようという流れにあることは間違いありません。
・思ったよりも臨床的に意義のある消化管出血が少ない→潰瘍予防によるNNTが少ないため、NNHが上回るかもしれない
・早期経管栄養によるストレス潰瘍予防効果がどうか?これからのエビデンスに期待
など時代の流れと共に背景や考え方が変化している領域でもあります。施設ごとにプロトコルを作るなどして、暫定的なストレス潰瘍予防を設定するのが現時点ではよいのではないかなと思います。
参考文献
・N Engl J Med 2018;378:2506 入院患者の潰瘍予防 review
・CHEST 2001; 119:1222 人工呼吸器使用とGI副作用の関係に関しての包括的なreview
・亀田総合病院ICUのブログ 素晴らしい内容で私が書いた内容よりも難渋ばいも情報量があります、おすすめですhttp://www.kameda.com/pr/intensive_care_medicine/post_38.html