病態/病型
原因がまだ解明されていませんが、全身の上位運動ニューロンと下位運動ニューロンが選択的に障害され、進行性の病態をとります。
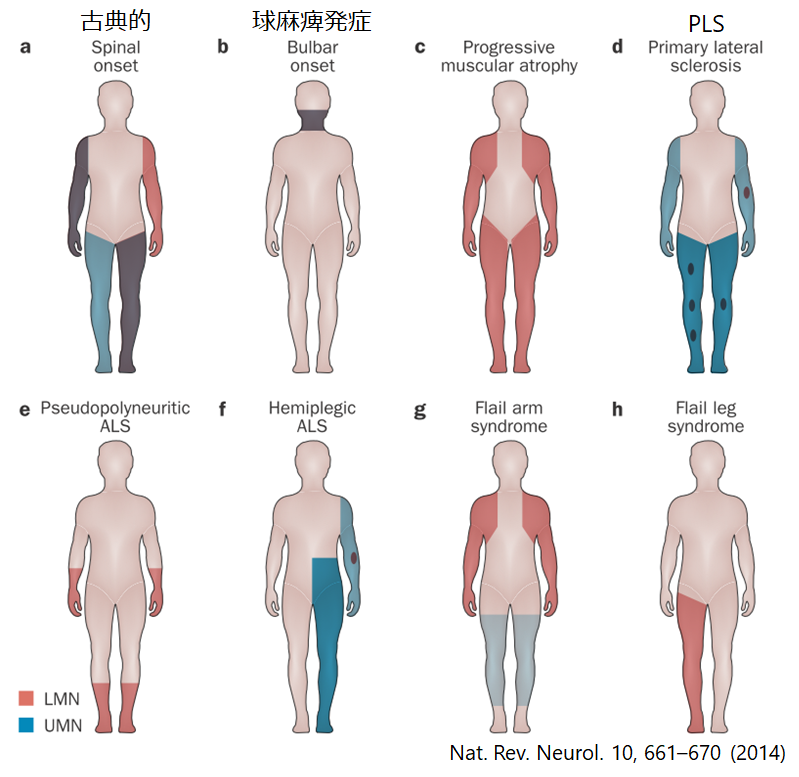
1:上位+下位運動ニューロン障害
・古典型
・進行性球麻痺型 PBP(progressive bulbar palsy)
2:下位運動ニューロン障害主体(上位運動ニューロン障害を欠く)
・脊髄性筋萎縮症
・Flail arm(Brachial amyotrophic diplegia, Man-in-the-Barrel) *こちらを参照
・Flail leg(偽神経炎型)
3:上位運動ニューロン障害主体(下位運動ニューロン障害を欠く)
・PLS(primary lateral sclerosis) *こちらを参照
・Milles syndrome
4:その他
・認知症を伴うALS
・呼吸筋麻痺型
*FALS(家族性筋萎縮性側索硬化症)の遺伝子に関して *家族性に関する明確な定義はなし
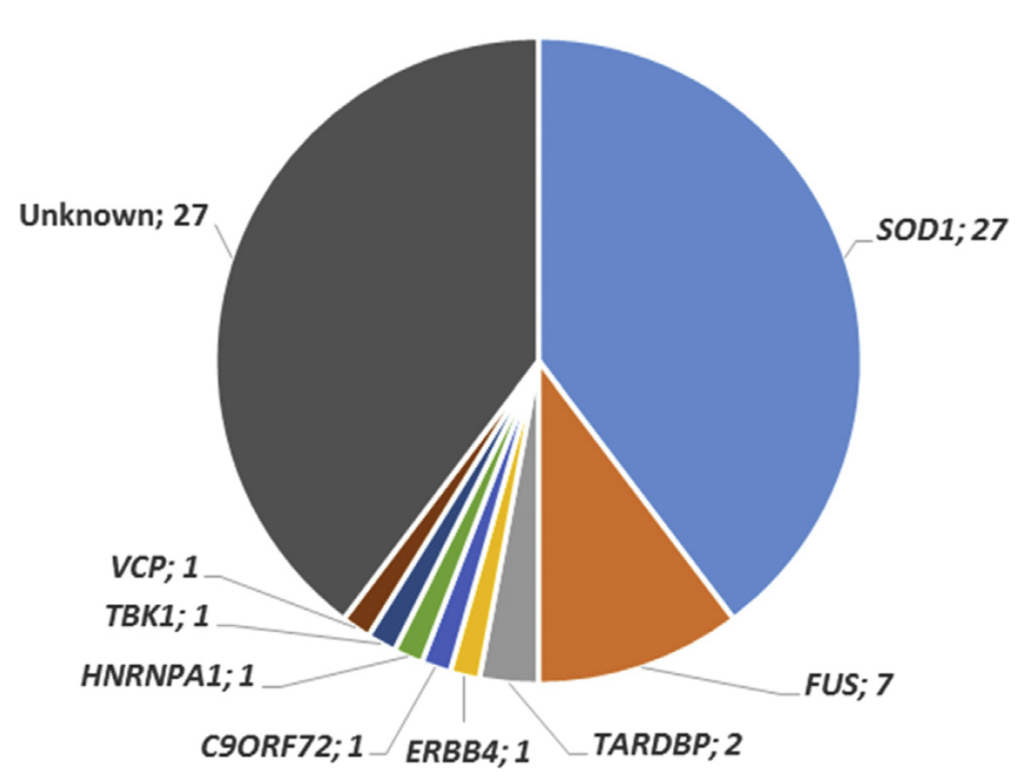
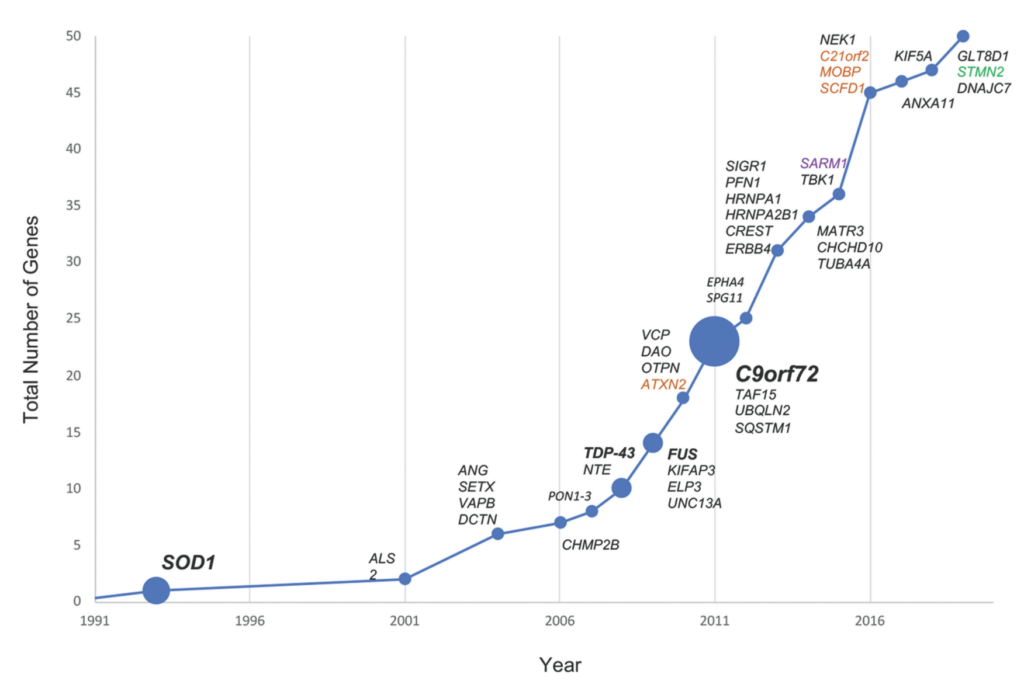
・日本での頻度(5~10%):SOD1>FUS>TARDBP 遺伝形式はADが多い・下図はH. Naruse et al. / Neurobiology of Aging 61 (2018) 255.e9e255.e16より引用(海外ではC9ORF72が最も頻度が高いが本邦では少ない)
・臨床像のみでFALSを鑑別することは難しい・同一病型ないでも発症年齢、進行速度などに拡がりがある
臨床像
・発症様式:70%が四肢の筋力低下発症(特に左右非対称で遠位優位の場合が多い)、25%が球症状発症、残りの少数が呼吸障害発症です。眼球運動は後期まで保たれる傾向があります。
・経過:進行性・他の部位への進展という点が何よりも診断上重要で、進行して一度停止する場合、部位が一か所にだけとどまり続けて広がりをみせない場合などはその他の疾患を考慮します。
・症状:上位/下位運動ニューロン障害が共存している点がポイントで、身体所見上では「萎縮している筋で深部腱反射が亢進している」という点が特徴的です。また障害が末梢神経や髄節の分布に沿わないという点も重要で、特に頚椎症性筋萎縮症が上肢発症のALSと鑑別になることが多いですが、頚椎症性筋萎縮症は必ず髄節に沿った障害を呈しますが、ALSは髄節と関係なく障害が広がる点が大きな違いです(髄節に関してはこちらを参照ください)。
*参考:頸部前屈の筋力低下
・頚椎症では障害されず、ALSでは障害されるため重要なポイント
・筋疾患:筋炎では最も早く筋力低下をきたす筋のうちのひとつ(多くの筋ジストロフィーでは障害されにくいため鑑別に役立つ)*通常頸部伸展が屈曲より先に障害されることは筋炎ではまれ
・筋力低下の分布:上肢は園生先生の教科書には「三角筋>上腕二頭筋/上腕三頭筋<小手筋」の分布が特徴的と記載されています。つまり三角筋や第一背側骨間筋などの障害が早期とされています。
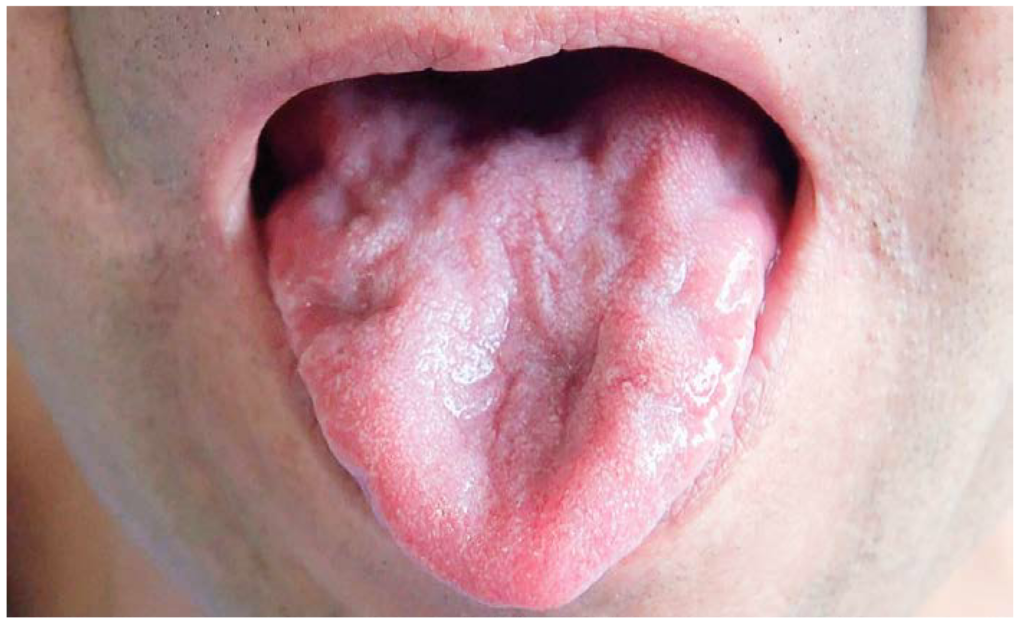
・ALSの開鼻声は特徴的で、声を聴いただけで「あれっこれはALS?」と疑う場合もあります。bulbarの症状のみで発症し急性進行性、また頭部MRI検査で他疾患(血管障害や悪性腫瘍)の可能性が除外される場合はALSの可能性を強く考慮します(嚥下障害の鑑別はこちらもご参照ください)。舌のfasciculationは挺舌させると誘発されるため、「挺舌しない状態でfasciculationが存在するかどうか?」を特に診察では意識します。下図はN Engl J Med 2014; 371:e7より引用。
・体重減少:悪性腫瘍を疑うほど体重が減少する場合もあり注意が必要です(体重減少の鑑別にALSを入れるべきと個人的には考えます:機序は解明されていない)
・四肢が攣る(cramp):これもALSでは特徴的な症状で患者さんはかなりはっきりと自覚しています。文献を調べられていなくて恐縮ですが、個人的には病初期に認めることが多い印象を受けます。
特徴的な障害分布
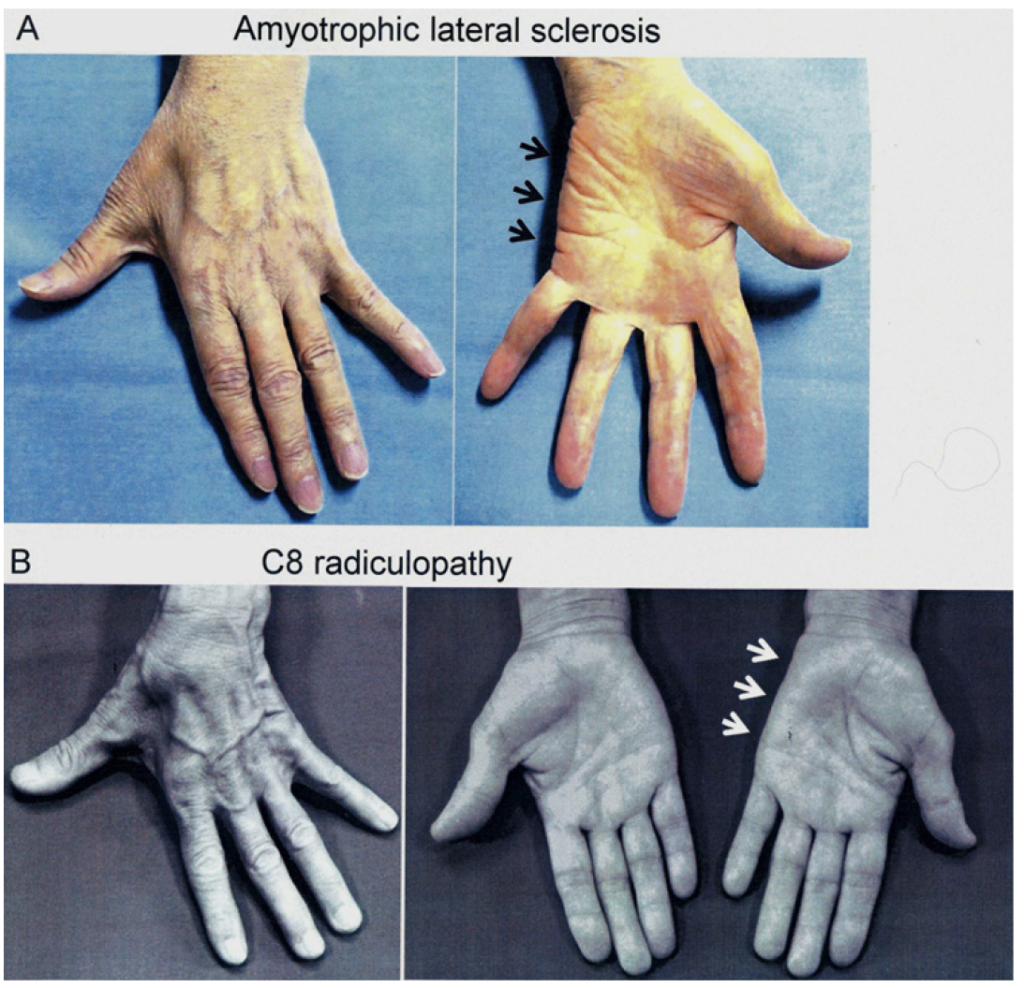
“Split hand”:母指球筋や背側骨間筋(FDI)の萎縮が目立つのに比して、小指球が保たれる分布を同じ手内筋の中で解離があるということで”split hand”と表現しALSで有名な徴候です(J Neurol Neurosurg Psychiatry. 2012;83:399-403.)。尺骨神経障害であれば小指球筋も障害されるはずであるため、ALSを疑うヒントとなる所見です(下図も上記のJNNPより引用)。
*参考:FDI(first dorsal interossei: 第1背側骨間筋 C8/尺骨神経支配)に関して
・ALSで最も早期に障害される筋のうちの1つ(園生先生の教科書には下肢初発、または球症状初発のALSでもFDIに既に筋力低下を認めることに関しての言及があります)
・MMTではADMと異なりphysiological weaknessを認めない点が有用。橈骨神経麻痺などにより手指伸展障害があるとうまく力が入らない場合があり、この場合は他動的に伸展位を保持した状態でMMTを評価する必要がある(重要)。
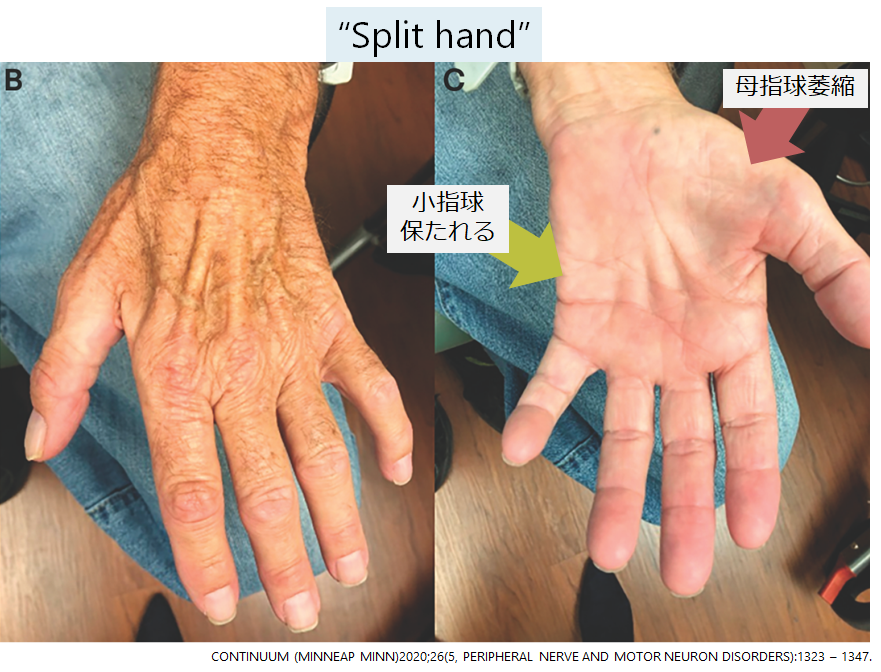
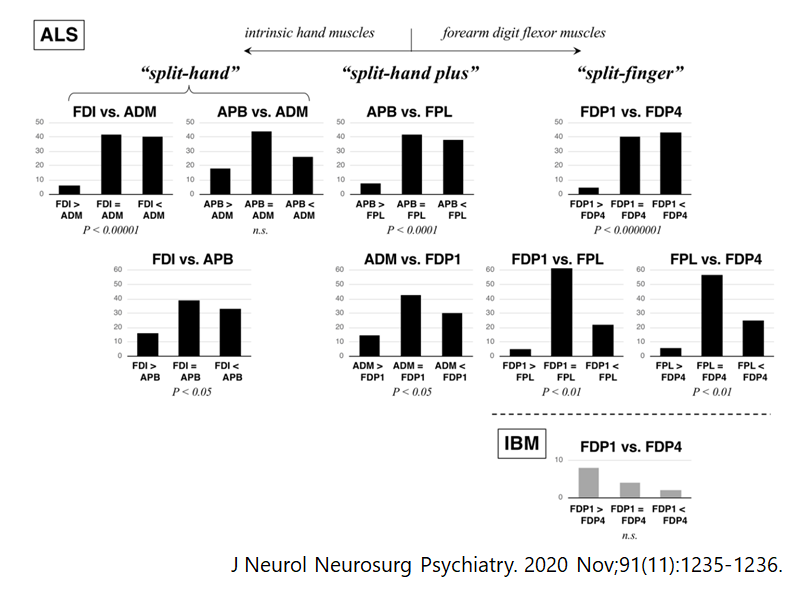
“Split hand plus”:母指球が萎縮するにも関わらず、長母指屈筋(FPL)が比較的保たれることを表した所見として報告されています(Amyotroph Lateral Scler Frontotemporal Degener. 2013 May;14(4):315-8.)。
“Split finger”:深指屈筋(FDP)の中でFDP1がFDP4よりもより強く障害される所見として園生先生がJNNPで投稿されていらっしゃいます(J Neurol Neurosurg Psychiatry. 2020 Nov;91(11):1235-1236.)。FDPに関しては封入体筋炎の記事で簡単なまとめがあるのでこちらをご参照ください。
検査
採血検査:他疾患除外目的
・CK値:ALSでも上昇するが通常は<1000U/Lである。著明な上昇は筋疾患を疑うが、IBMなどはCKがそこまで上昇しないため注意が必要。
・異常蛋白血症:SLONM-MGUSはALS mimicsとして注意が必要
・感染症関連:HTLV1(HAM/TSP), HIV(脊髄障害の鑑別)
・自己抗体:抗AChR抗体、抗MuSK抗体
・抗ガングリオシド抗体(抗GM1-IgM抗体):MMNを疑う場合参考として提出(感度は50%程度であるが)
・内分泌代謝:甲状腺機能、ビタミンB12、銅(代謝性脊髄障害)、抗GAD抗体(SPS
を疑う場合)
髄液検査:MSや感染、脱髄疾患での蛋白細胞解離など他疾患の除外目的
遺伝子検査:SBMA、HSP(遺伝性痙性対麻痺)を疑う場合
電気生理検査
■神経伝導検査
MCS:通常前角細胞障害に伴いCMAP振幅は低下します。LEMSを疑う場合は強収縮前後でのCMAP振幅を比較します。
SCS:SBMAではSNAP振幅がたとえ臨床的に感覚障害を認めなくとも低下することが特徴として挙げられます。SNAP低下は必ずSBMAに注意(こちらを参照)
F波:前角細胞の障害を反映してF波の出現頻度低下を認めます。
■針筋電図:”subclinical”な下位運動ニューロン障害を検出するために必須の検査です。
<ALSでの針筋電図の原則>
・脳幹領域(1か所)+頚髄領域(2か所)+胸髄領域(1か所)+腰髄領域(2か所)の4部位
・脳幹領域:胸鎖乳突筋もしくは僧帽筋 *僧帽筋は上位頚髄の支配もあるため純粋な脳幹領域ではない
・頚髄領域:上腕、前腕、手内筋のうちから2か所を選択
・胸髄領域:通常は傍脊柱起立筋を選択する場合が多い
・腰髄領域:大腿と下腿からそれぞれ1か所選択し計2か所
・萎縮を認める部位の検査を優先する
*反復神経刺激試験を行い頚椎症由来の神経障害と鑑別する方法もあります(未熟な神経再支配領域では神経筋伝達の安全性が低下するため、decrementを認めます。こちらを参照)
*上位運動ニューロン障害を検出する電気生理検査としてはMEPが有名ですが、診断基準には現状組み込まれていません。
画像検査:他疾患除外目的
・頭部MRI検査
・脊髄MRI検査(特に頚髄):他疾患の鑑別目的に重要かつ必須・平山病を疑う場合は前屈位の頚髄MRIも追加する
*ポイント:ALSで脊髄前角にT2WI高信号を呈することはない。
診断基準:Awaji基準
診断のポイント
1:上位/下位運動ニューロン障害の共存
2:進行性の経過
3:他疾患の除外*これが何よりも重要
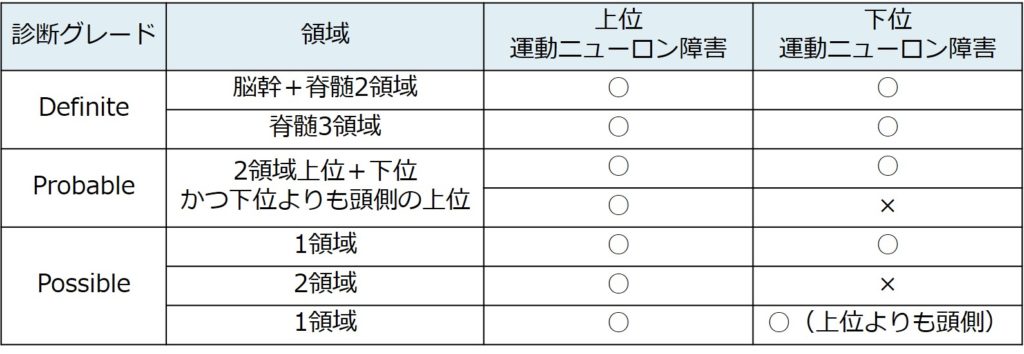
Awaji基準
変更点1:筋電図異常を臨床的な筋萎縮と同等に扱う
変更点2:fasciculation potentialを急性脱神経所見として採用
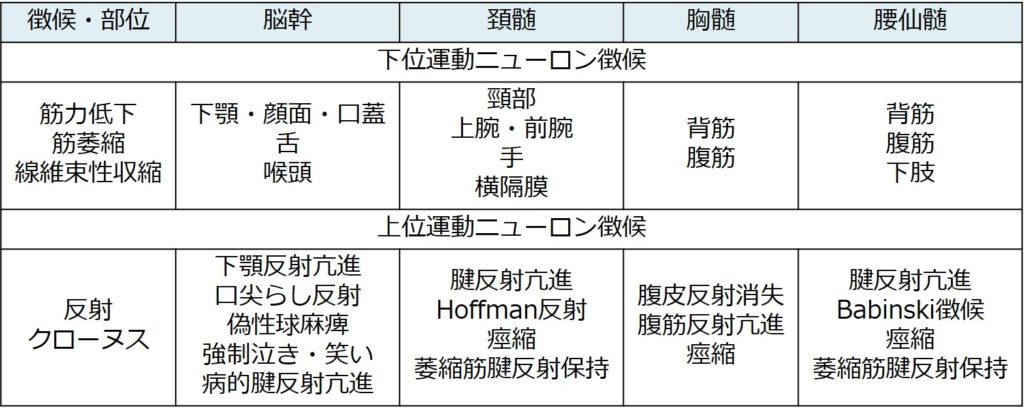
*上位/下位運動ニューロン障害
鑑別診断
ALSは臨床的には「あっこれはきっとALSだな」と積極的に疑うことが可能な疾患ですが、実際のアプローチは他疾患(特に治療可能な疾患)を除外していく除外診断を行います。私は昔尊敬する先生に「どんなにALSらしいと思っても、ALSと医者が決めた瞬間に引導を渡すことになってしまうから徹底的に他の疾患を考慮することが重要」と教わりました。私の師匠もほぼ全例セカンドオピニオンを自ら勧めるとおっしゃっており、この疾患を診断することへの重みを痛感しています。
1:下位運動ニューロン徴候が主体の場合
■duropathies:多髄節性筋萎縮症(MRI検査で脊髄前の硬膜をきちんと評価することが重要)、平山病(こちらを参照)など
■筋疾患:特に封入体筋炎(こちらを参照)がCK上昇にも乏しく鑑別上難しい(私自身も当初ALSと診断した方が後日封入体筋炎と判明した症例の経験があります)。IBMは深指屈筋と大腿四頭筋に筋力低下のアクセントが強いことが特徴。またSLONM-MGUS(こちらを参照)
■頚椎症:頚椎症性筋萎縮症(CSA):髄節性、頸部の筋力、球症状の有無などが鑑別点として重要です(こちらを参照)
■末梢神経障害
・SBMA:進行スピードが緩徐である点、女性化乳房、NCSでのSNAP振幅低下が鑑別点のポイント(こちらを参照)
・MMN:左右非対称/上肢優位/遠位優位、末梢神経に沿った障害で特に免疫グロブリン療法で治療できる点でよく鑑別が問題となる(こちらを参照)
・その他:CIDP、CMT、神経痛性筋萎縮症(NA: neuralgic amyotrophy)、post-polio syndrome
■神経筋接合部疾患:重症筋無力症(特にMuSK抗体陽性例は萎縮もするしbulbarに強く似る)、LEMS(個人的にALS疑いとされて紹介されたLEMS症例の経験があります こちら)
*上位運動ニューロン徴候が乏しく下位運動ニューロン徴候のみが目立つ場合の方が診断が難しく注意が必要になります。
2:上位運動ニューロン徴候が主体の場合
・脊髄障害:HTLV1, HIV, ビタミンB12欠乏、銅欠乏、dAVF、頚椎症性脊髄症(こちらを参照)
・副腎白質ジストロフィー
・SPS:こちらを参照
・遺伝性痙性対麻痺
・成人発症Tay-Sachs病
・多発性硬化症
治療
根本的な治療薬は残念ながらまだ存在しません。現状は進行を抑制する作用がある薬剤が紹介されています。
1:リルゾール riluzole 商品名:リルテック
作用機序:グルタミン酸伝達抑制
製剤:50mg/錠
処方例:リルテック50mg 2錠分2 朝夕食前
副作用:肝逸脱酵素上昇、消化管症状
効果:2-3か月の生存期間延長効果、筋力改善効果はなし
<根拠となる文献>
・N Engl J Med 1994;330(9):585 – 591.:RCTでの有用性の証明
・Cochrane Database Syst Rev 2012;(2):CD001447.:その後のsystematic review(まとめ:3か月の生存期間延長効果)
2:エダラボン edaravone
作用機序:フリーラジカルスカベンジャー
製剤:30mg/20mL(注射製剤)、30mg/100mL(点滴静注バッグ)
処方例:60mg 1日1回投与(60分かけて投与) *1クールは28日間
第1クール:最初14日連日点滴、後14日休薬
第2クール以降:最初14日のうち10日間点滴、後14日休薬 *第2クール以降の10日間点滴は連日でなくても大丈夫であり、平日だけなど生活スタイルに合わせて変更可能。
<根拠となる文献>
・Amyotroph Lateral Scler Frontotemporal Degener 2014; 15: 610–17.:edaravone初のRCTで6か月後のALSFRS-R scoreをprimary outcomeに設定し、placeboと有意差を示せず。
・Lancet Neurol 2017;16(7):505 – 512.:上記studyのpost-hoc analysisで、発症2年以下、呼吸機能保たれる、重症度分類1 or 2の症例では有用性が証明。
次に薬剤以外の介入点に関してまとめます。ここからはかなり個人的な経験/意見が入っております。私はALS患者さんの在宅診療を何度かしたことがありますが、そこで感じた点などを中心にまとめます。
NPPVに関して
・早期からのNPPV導入はQOL・予後改善につながるという報告があり(Lancet Neurol 2006; 5: 140–47)、私は積極的に使用をすすめています。神経筋疾患の呼吸不全の初期は決して「息が苦しい」という症状を呈する訳ではなく、「朝頭痛がする(夜間低換気によるPaCO2上昇による脳血管拡張)」、「日中の集中力が低下した(夜間低換気による睡眠障害)」などの一見呼吸とは関係ないような症状でくる場合があるため医療者が注意する必要があります(神経筋疾患の呼吸不全に関してはこちらにまとめがあるのでご参照ください)。
・NPPVはいきなり24時間使用するのではなく、まずは夜間だけ導入する方法をとります。私は短期間入院して慣れてもらってから在宅へつなげるケースが多いです。独居の場合などでマスクが夜間にずれてしまい、上肢の筋力低下によりマスクをもとに戻せない方などは一度マスクがずれてしまうと夜間ずっとアラームが鳴ってほとんど眠れないというトラブルが起こったこともあり介護の点と合わせて話し合いを持つ必要があります。
・ALS患者さんでの問題点は通常呼吸障害があるALS患者さんは球麻痺も伴っているという点で、喀痰の喀出がNPPVではより難しくなる難点を抱えています(気道閉塞のリスク)。私はメラチューブ(下図参照:https://www.mera.co.jp/medical/product-info/603/#より引用)をNPPVマスクの脇から口腔内に入れて唾液持続吸引をしながらマスクを使用する場合が多いですがやはりleakの問題もあり悩ましいです。

気管切開に関して
・ここもdecision-makingが非常に難しい点です。「ほとんどの患者さんご家族は最初気管切開に対して拒否の姿勢をとられることが多い」です。
・ただ問題点は上気道のトラブルは薬剤などで如何とも対応し難くかつ患者さんご自身もかなり苦しいという問題点が挙げられます。いくら鎮静の薬剤を使用してもこの苦しさを根本的に解決することは難しく、気管切開しか根本的な解決方法はないことが多いです。当初は気管切開に難色を示されていた患者さんが、気道閉塞を起こされてしまい気管切開を実施されて、「気管切開によって圧倒的に楽になった」とおっしゃる方がいらっしゃることも経験上事実です。
・私は決して全例に気管切開をすすめる訳ではないですが、やはり早い段階から「気管切開は絶対に行わない」と決めつけてしまう点には躊躇する場合があります。
胃ろうに関して
・患者さんとそのご家族は「胃ろう」に対しての昔のnegativeなイメージを持たれていることが非常に多いです。なのでまずは正しい情報を提供することが何より重要で、看護師さんなどにも入ってもらい情報をきちんと提供します。
・「胃ろう」を作ってしまったらこの先口から全く食べられない訳ではないこともよく説明します。私は「必要な栄養は胃ろうからしっかり投与して体を元気に保って、好きな食べ物を食べやすい形にして1日少しだけ食べるという方法」をよく薦めています。必要な栄養素を経口摂取だけで補うことにはご家族も食事に時間がかかりすぎて難しいと感じていることが多いのでこの点に関してはご同意いただけるケースが多い印象です。
・「胃ろう」は早め増設することが重要です。%FVC50%以上の時期が低リスクであり薦められます(%FVC30-50%は中リスク、%FVC30%未満は高リスク)。
患者さんへの情報
日本ALS協会ホームページ(JALSA):http://alsjapan.org/
参考文献
・CONTINUUM (MINNEAP MINN)2020;26(5, PERIPHERAL NERVE AND MOTOR NEURON DISORDERS):1323 – 1347.
・筋萎縮性側索硬化症診療ガイドライン2013 日本神経学会


