病態
・孤発的にoligodendrocyteにα-synuclein(αシヌクレイン)が蓄積する病態です。0.6人/100,000/年
*参考:α-synucleinoopathy
1:神経細胞に蓄積→レヴィ小体 疾患:パーキンソン病・LBD
2:オリゴデンドロサイトに蓄積→GCI(glial cytoplasmic inclusion:グリア細胞質封入体) 疾患:MSA
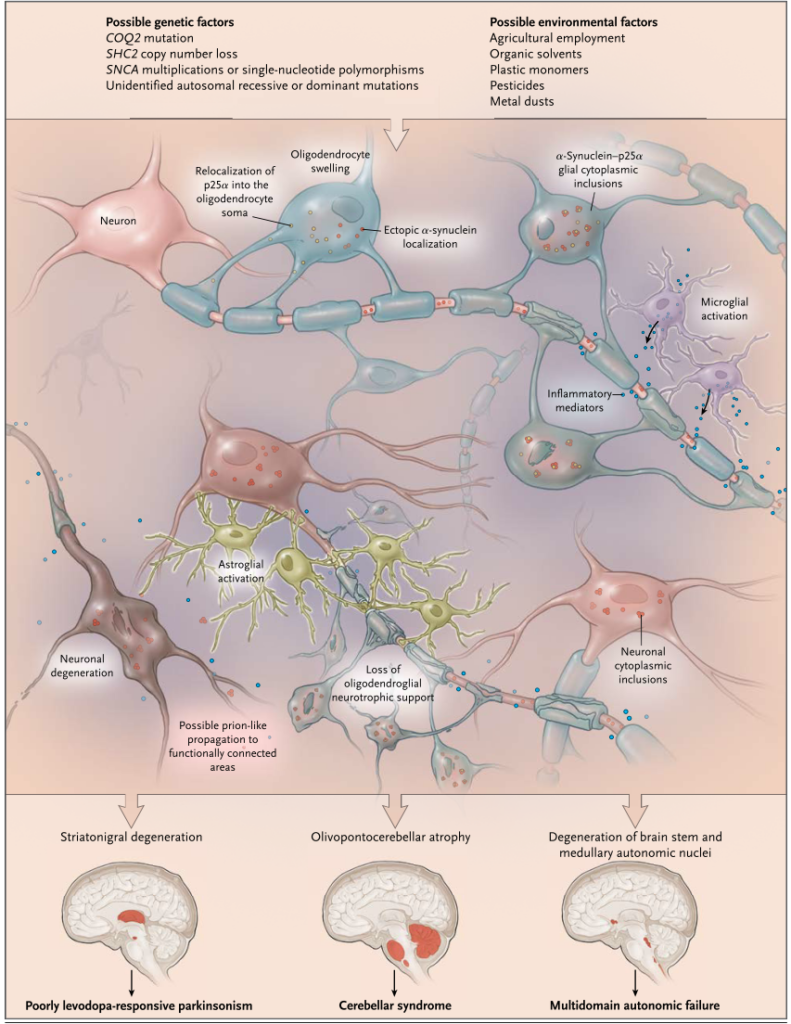
病変分布によってパーキンソニズム主体、小脳失調主体、自律神経症状主体のものに分かれますが、最終的にはいずれも合わさる病態になります。自律神経主体のものに関してはこちらをご参照ください。
海外:MSA-P>MSA-C、日本:MSA-C>MSA-Pとされ日本ではMSA-Cが多いとされています(実臨床でもMSA-Cが多いと感じます)。
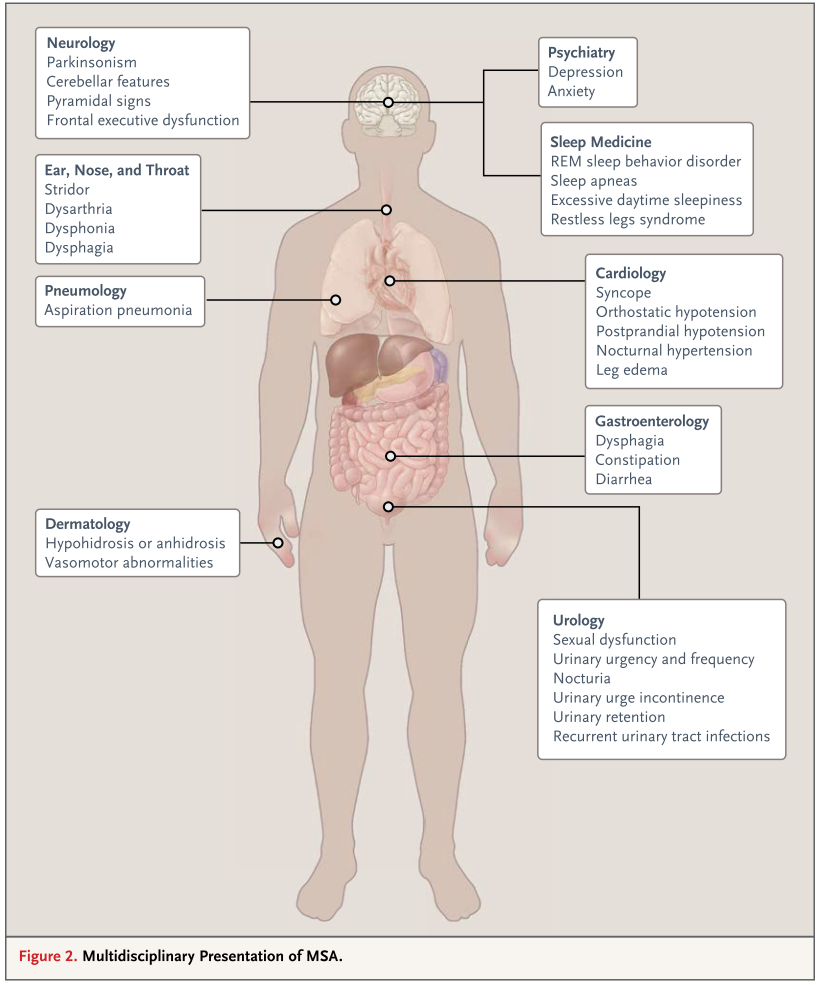
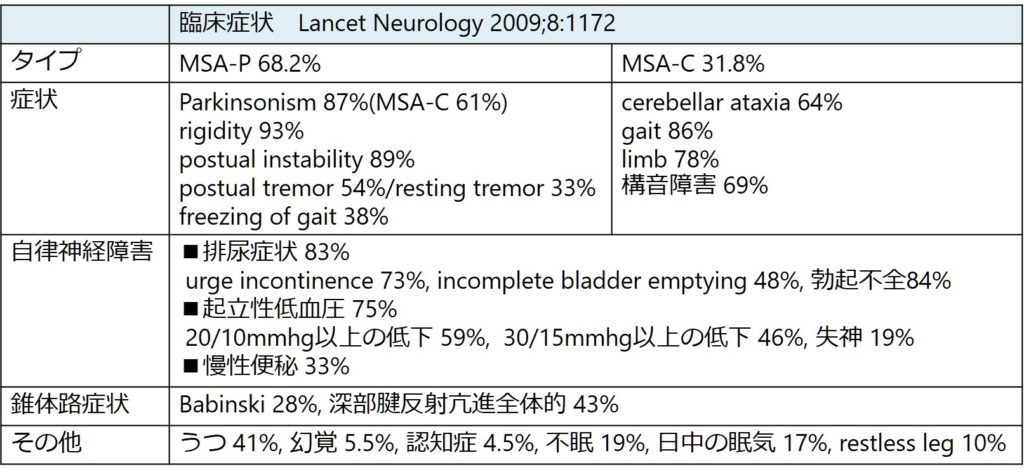
症状
■自律神経障害
膀胱直腸障害、勃起障害が運動症状に先行することが多いです。MSAの尿路症状は排尿障害が特徴で、PDは蓄尿障害が特徴的です(詳しくはこちらをご参照ください)。
起立性低血圧:症候性、無症候性いずれもありえます。症候性の場合は膀胱障害、勃起障害の後に出現することが多く。SBP30/DBP15mmhg以上の低下は通常求められる血圧低下よりも大きいです(通常起立性低血圧の診断基準はSBP20/DBP10mmHg以上の低下)。日常生活ADLにかなり支障をきたすため注意が必要です。起立性低血圧への対応に関してはこちらをご参照ください。
勃起障害:最も初期症状であることがあり、男性患者のほぼすべてを障害するとされています。逆に勃起障害がない場合は積極的には疑いにくいとも記載があります。
消化管障害:便秘症状を随伴することが多いとされています。
*MSAでは交代性ホルネル症候群を呈する場合もあるとされています。自律神経障害全般に関してはこちらをご参照ください。
■Parkinsonism
ほとんどの患者がどこかの段階で、parkinsonism症状を発症します。パーキンソン病で典型的なpill rolling tremorは一般的ではありません。UPDRS3 score 20%/年程度で増悪し(PDの場合は10%/年くらいであるが)、進行が早いです。30%程度は有意な改善を示すが基本はL-DOPA反応性不良が特徴です。元々MSA-Cの病型で発症した患者さんにparkinsonismが途中から加わるとADLが一気にがくんと悪くなる印象があります。
■小脳失調
歩行障害、構音障害>歩行障害となることが多いとされています。小脳失調発症から5年程度で車いす生活となることが多いようです。
画像所見
MRI撮影方法:T2 axial,T1 sagittal,FLAIR coronal
■MSA-C
・小脳萎縮
・橋横走線維の萎縮:縦(midline liner hyperintensity)→十字にT2高信号(hot cross bun sign)
*余談:”hot cross bun”はイギリスの菓子パンで十字の飾りがあることが特徴です(下の画像はwikipediaより引用)。この十字模様がMRI画像と似ていることが名前が付いています。
*hot cross bun signはMSAに以外の疾患も呈する場合があり注意(その他SCA2などでも認めるとされています)

・中小脳脚萎縮、変性:T2WI高信号(SCAでは認めないことが多い)
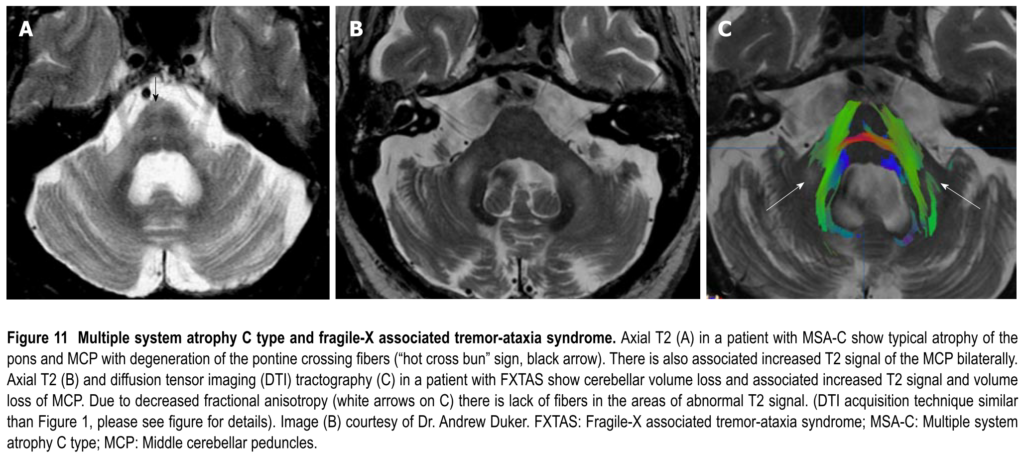
*発症2年以内に上記所見を認める場合はMSA-Cの可能性が高い
*皮質性小脳萎縮症では橋横線維の変性を認めない
*中小脳脚病変に関してはこちらをご参照ください。
*参考:橋横走線維の変性T2高信号を認める疾患
・MSA:縦、十字(cross sign)どちらもありうる
・SCA3>1=2>7=8:縦のことが多い、正中部のみに認めることが多い、変性の程度が軽い、中小脳脚まで変性がおよぶことは少ない 臨床経過がMSAよりも緩徐である
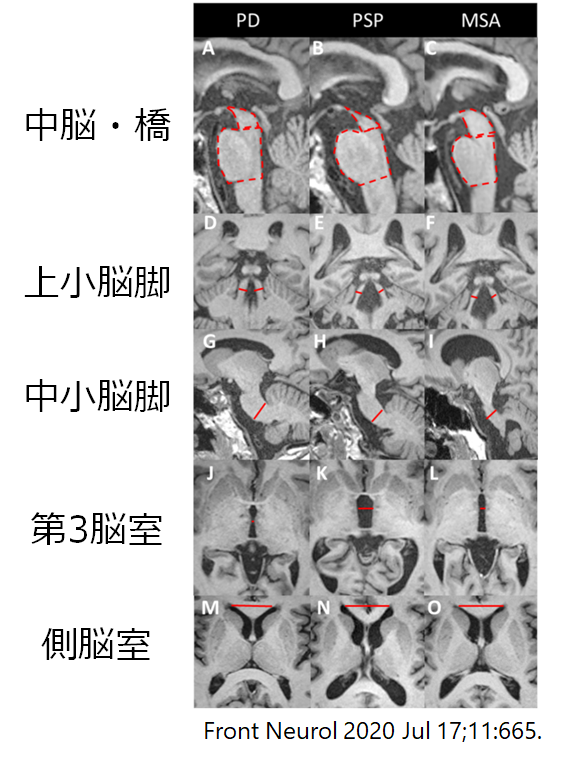
*脳幹部病変に関して:PD、PSP、MSAの脳幹部病変の比較は以下の通りです。MSAは橋底部(腹側)萎縮を呈することが特徴。
・橋底部(腹側):繊維・橋核が存在・MSAで萎縮
・橋被蓋部(背側):脳神経核・網様体が存在 PSPで萎縮
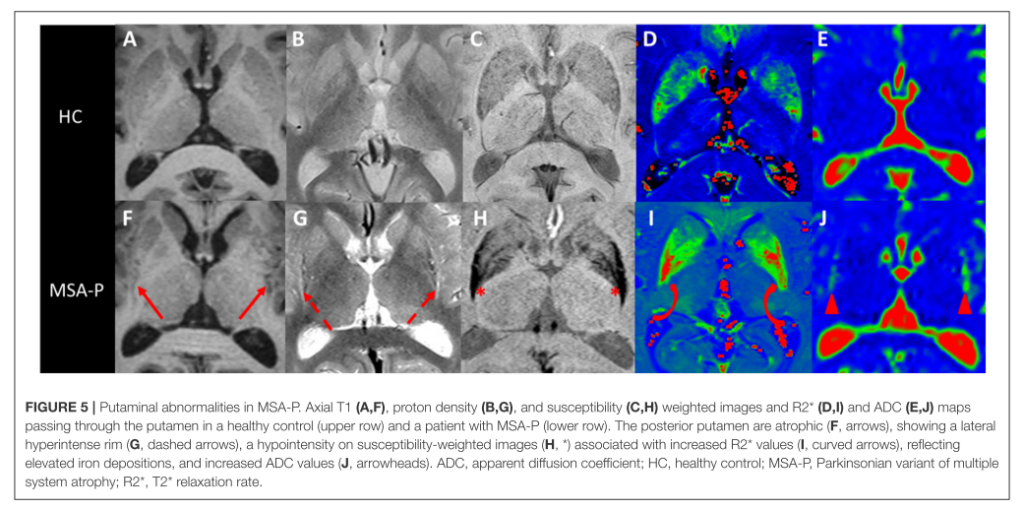
■MSA-P
・MSA-Pの初期には片側の被殻にのみ変性が起こり(病理学的には被殻背側外側の変性・鉄沈着)、外側髄板には変性をきたさない。萎縮により被殻外側に凸でなくなるため、被殻の外側が直線状になる(”FLAIR coronal像”が観察しやすい!)
・外側背側T2WIにて高信号
・被殻自体がT2にて低信号になる(それ自体は加齢でも認める所見であるが、萎縮を伴うとMSAに特徴的な所見となる)
*鉄沈着:T2*にて低信号
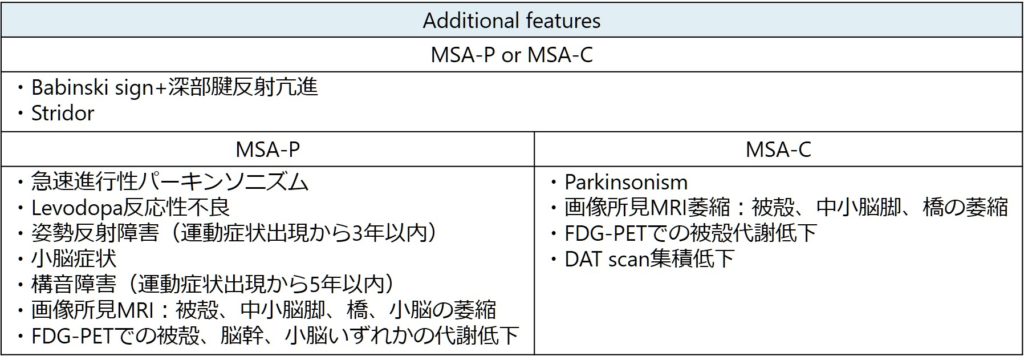
診断基準
1969年にMSAの概念が導入され、現在の最新の診断基準は2008年のものです(Neurology 2008;71:670より参照)。definite MSAは病理診断なので、生前には不可能なので、基本は”probable MSA”を目指す形になります。
■definite MSA:病理学的に証明 *このため生前診断は不可能。
■probable MSA 1 + 2 or 3
1:自律神経障害:排尿障害、勃起障害 or起立性低血圧(起立後3分いないにSBP30mmhg/DBP15mmhg以上の低下)
2:Parkinsonism(levodopa反応性悪い)
3:小脳症状(gait ataxia+構音障害、limb ataxia or 眼球運動障害)
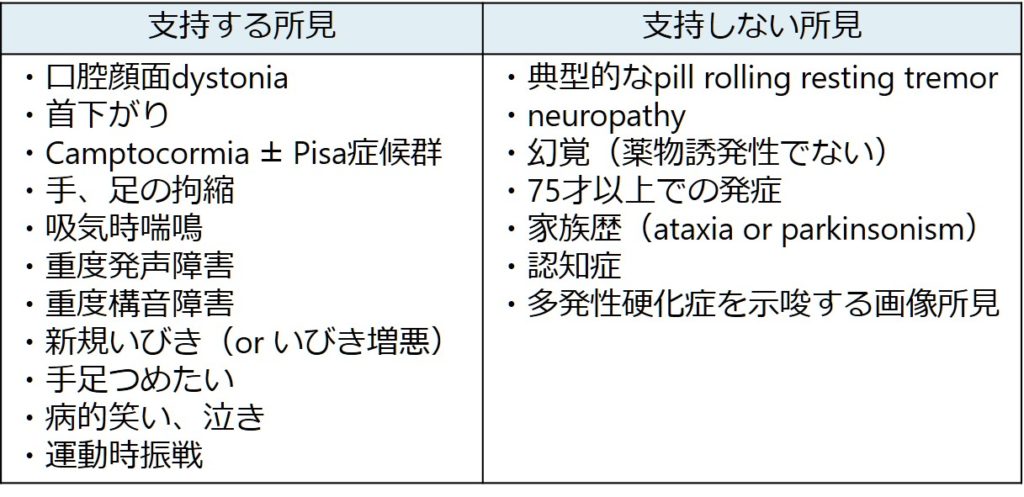
支持する所見、支持しない所見は下記の通りにまとめられます。
*非常にまれですが若年発症のMSAに関してYOMSA(young-onset MSA)という概念が提唱されています。こちらもご参照いただければと思います。
予後
運動症状(Parkinsonism or 小脳失調)もしくは自律神経障害(勃起不全を除く)が出現したと時を発症点とします。予後に関して余命:平均6-10年とされていますが、実際には~3年の場合や、15年以上の場合もあるため画一的に指摘することは難しいです。 “counseling patients on life expectancy can be challenging for the treating physician”と記載されています。
・予後不良因子:パーキンソン型、発症高齢、自律神経症状早期からの出現
・予後良好因子:小脳型、自律神経症状出現後期
一般的な経過(下図参照) 杖:3年以内50% 車いす:5年以内60% 寝たきり:6~8年
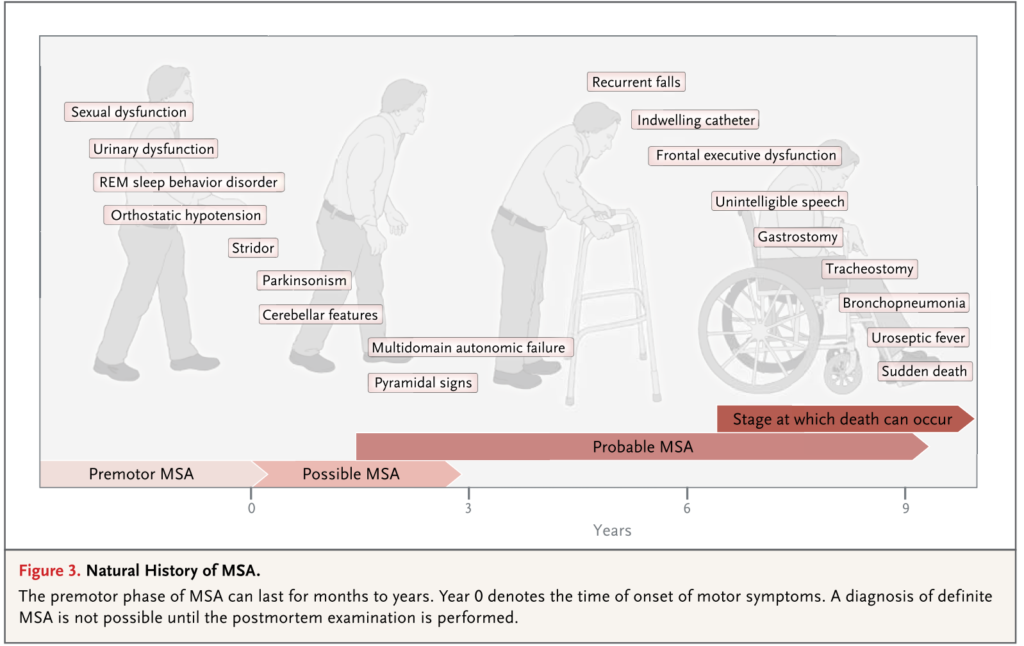
下記にPD, PSP, MSAの発症時期、診断時期、車いす、予後に関しての比較まとめを掲載します。MSAは比較的若年発症で変性疾患としては経過が速いことが特徴的と思います。
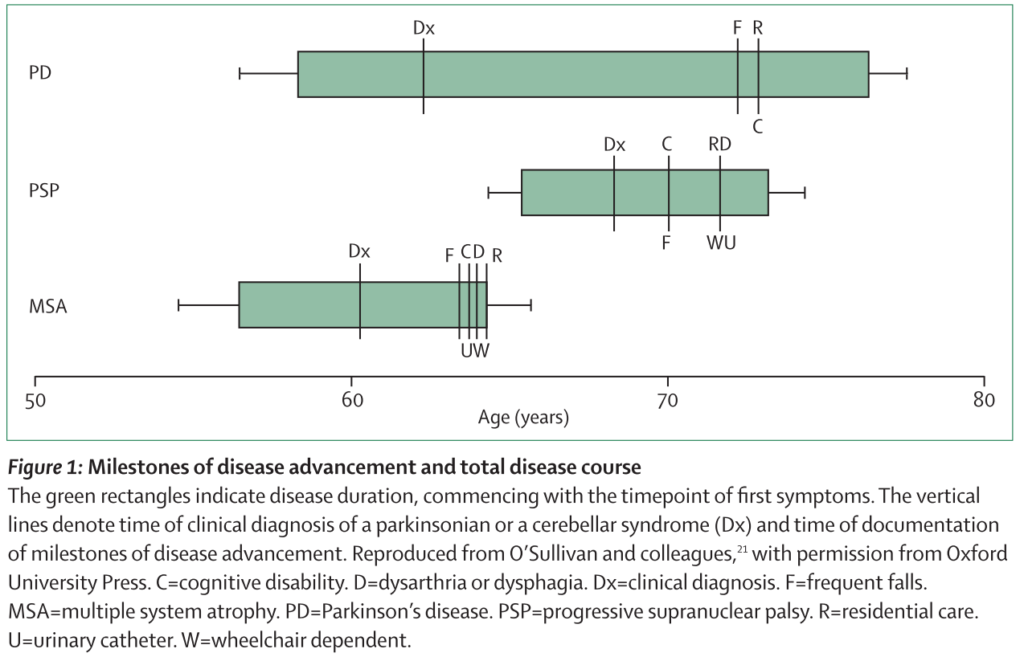
■死亡原因
以下が代表的なMSA患者さんでの死亡原因となります。突然死に関しては上気道閉塞の問題の場合もあれば、呼吸中枢の問題の場合もあり事前のICがとても重要です。
1:感染症(肺炎、尿路感染)
2:突然死
・両側の声帯麻痺(外転障害・開大障害)による上気道閉塞 *声帯開大は後輪状披裂筋が担う
・brain-stem cardiorespiratory driveの障害(このため気管切開をしていても呼吸停止をきたしてしまう場合があります。気管切開により防ぐことができるのは上記の物理的な上気道閉塞のみです。)
■喉頭軟化症に関して
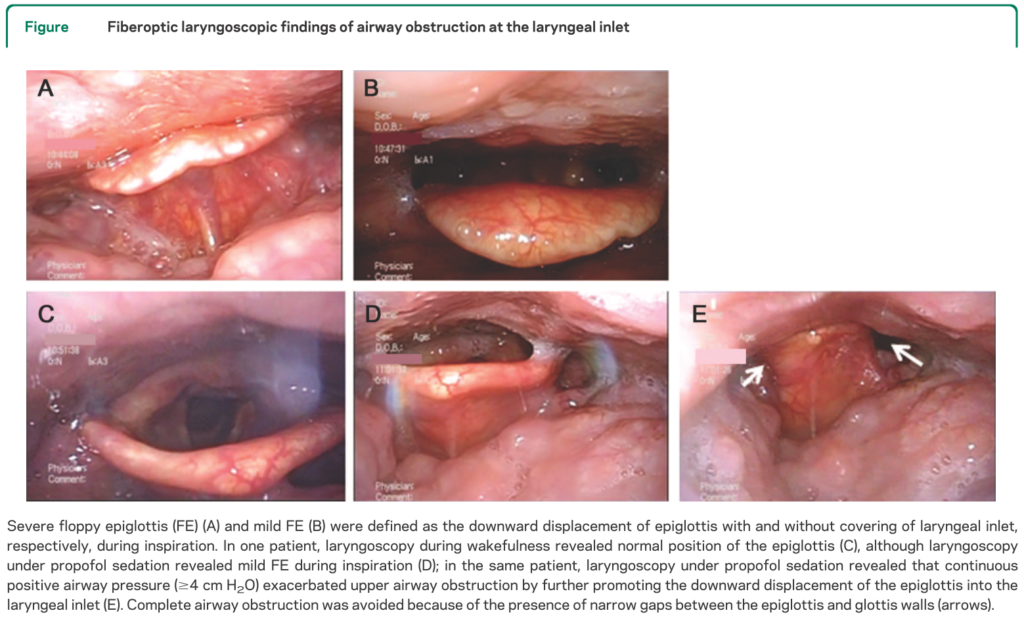
・MSAの患者さんでは睡眠関連の呼吸障害を認める場合多くあります。ここで注意が必要なのはMSA患者さんに認める場合がある喉頭軟化症(floppy epiglottis)です。喉頭軟化症がある状態で睡眠時の呼吸障害に対してCPAPを導入すると、喉頭蓋を気管側に押し込んでしまい上気道閉塞を悪化させてしまうため禁忌となります(下図を含めてNeurology 2011;76 1841-1842より引用させていただきました。この論文では17例のMSA患者さん(MSA-C14例、MSA-P3例)のうちにプロポフォールで鎮静を導入したところ12例(71%)に喉頭軟化症を認めています)。
・鎮静下での喉頭内視鏡できちんと喉頭軟化症の評価を行うことがMSA患者さんでは重要なことがわかります。
参考文献
・Neurology 2008;71:670:2008年のMSA診断基準
・Lancet Neurology 2009;8:1172 同じくMSAのreview
・NEJM 2015;372:249:MSAのreview