病態
結核性髄膜炎は全結核の約1%を占め、全年齢に起こりますが特に小児やHIV未治療の患者さんに多いとされています。結核性髄膜炎ではCSF内の菌量は100~1000コロニー/mLを超えることはまれで、菌量ではなく宿主の免疫反応が組織障害の程度を規定するとされています。
結核性髄膜炎がどのように引き起こされるか?その機序はいまだ完全には解明されていません。結核菌は血液からBBBを超えて、ミクログリアに回収され、細胞内で増殖し、サイトカインが分泌される機序(下図Nature reviews neurologyより引用)も推定されています。

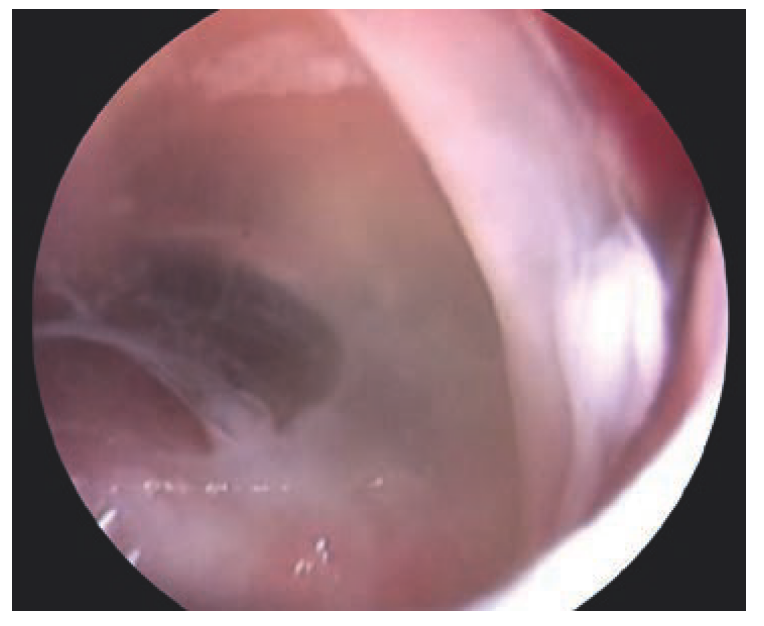
下図は第三脳室のくも膜下腔を内視鏡で観察したものです。結核性髄膜炎による滲出物が覆っており、正常の構造物が明瞭ではなっている様子が良く分かります(引用:Nature reviews neurology 2017;13:581)。
臨床症状
経過は基本的には亜急性~慢性であることが特徴ですが、急性経過の場合もあるため注意が必要です。非特異的な食欲低下、倦怠感、微熱といった症状のみから発症することもあり、なかなか病初期に診断することは難しい場合もあります。成人では倦怠感と食思不振が頭痛増悪や嘔吐に先行するとされています。なかなかこういう症状だったら結核性髄膜炎を疑うという特異的な所見には乏しいため、積極的に疑う姿勢が求められます。以下に160例の結核性髄膜炎の臨床像をまとめたreviewを載せます。
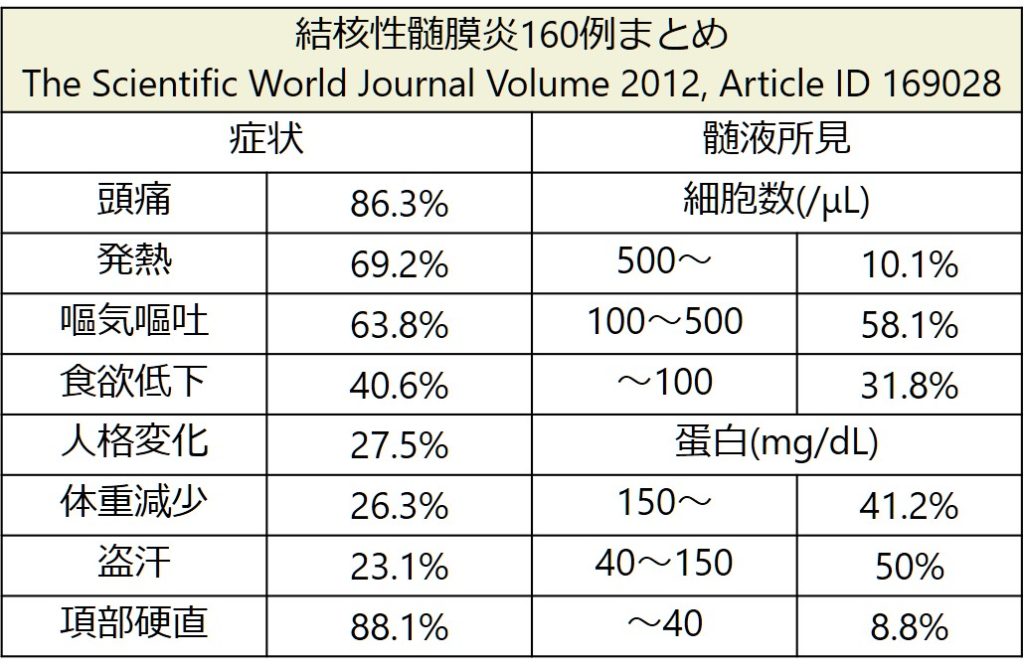
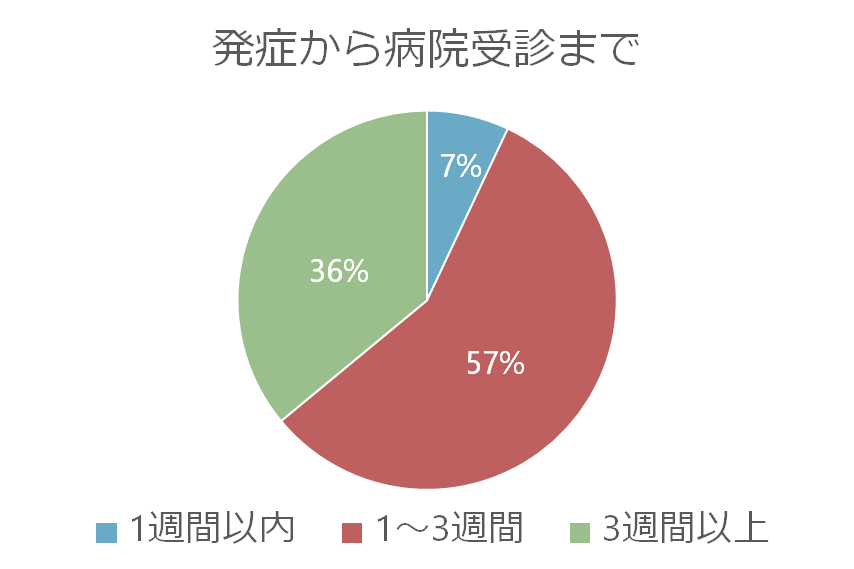
病態のところでも解説しましたが、病像・組織障害は宿主の免疫反応に依存します。特に1歳未満の小児、HIV共感染の場合は急激に進行する場合(comaまで至る)と報告されているものもありますが、HIV共感染は病状に変化を与えないという報告もあります。先ほどの160例の臨床像まとめでは発症から病院受診までの期間が1週間以内が7%、1~3週間が57%、3週間以上が36%という結果でした。
項部硬直は病初期にはどの年齢でも通常認めにくいとされています。
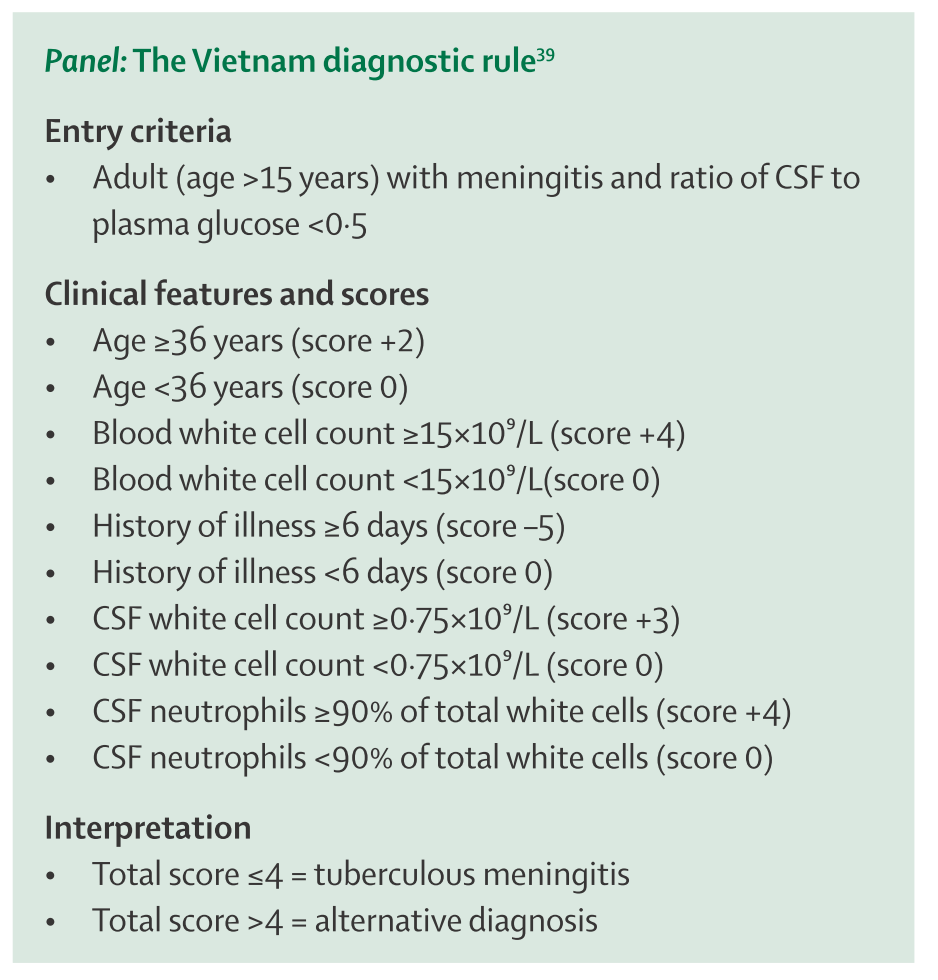
結核性髄膜炎を予測するスコアが提唱されていますが、いずれも東南アジアでのものが多く日本と検査前確率がかなり違う印象があります。このため、このスコアをそのまま日本で適応してよいかどうかは個人的に疑問が残ります。参考までに”The Vietnam diagnostic rule”を下に載せます。
神経学的合併症
■脳神経麻痺
1/3に認める比較的頻度の多い神経合併症です。脳底部の炎症性滲出物による核下性の脳神経障害の機序が推定されます。158人の結核性髄膜炎を後ろ向きにまとめた報告では脳神経麻痺は38%に認め、外転神経(Ⅵ)に最も多かったとされています(European Journal of Internal Medicine 22 (2011) 289–295)。どの脳神経が障害されるかは報告によってまちまちですが、Ⅲ(動眼神経)、Ⅴ(三叉神経)の障害が多いという報告もあるようです。多発脳神経麻痺を呈する場合もあるため、多発脳神経麻痺の鑑別としても重要です(多発脳神経麻痺の鑑別はこちら)。
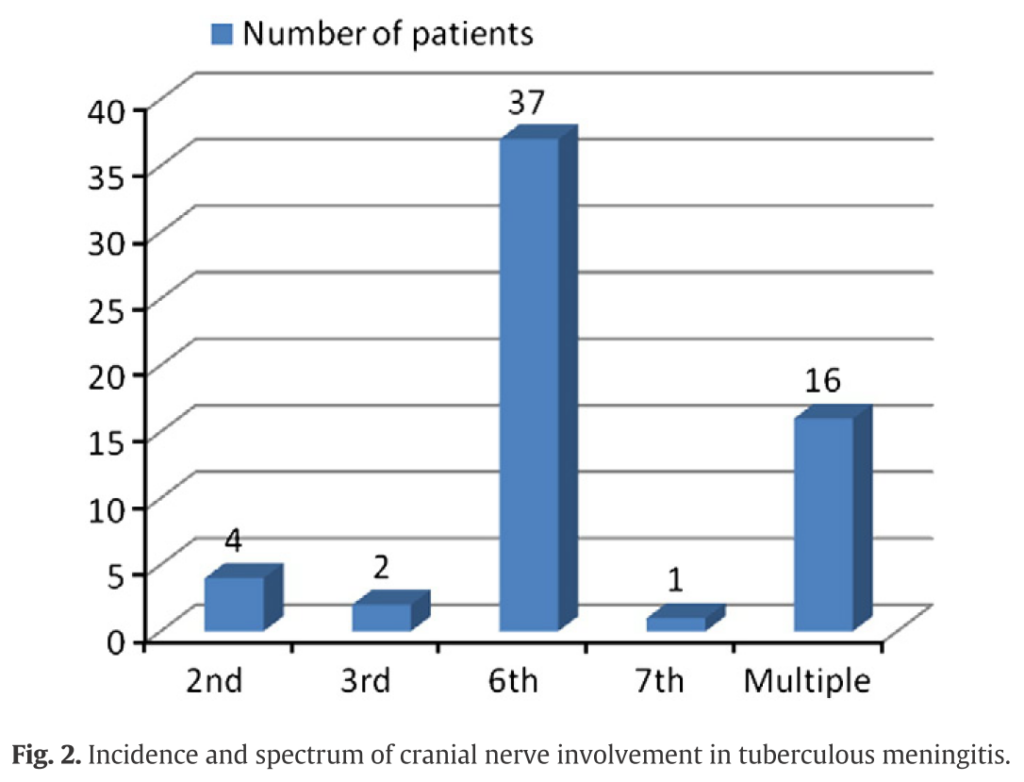
■水頭症
結核性髄膜炎の最も多い合併症で2/3程度に認めます。上記に第三脳室くも膜下腔の写真を載せましたが、このように非常に粘度の高い滲出物があるため多くの場合髄液を回収するくも膜顆粒が目詰まりを起こすことで髄液が回収できず、結果水頭症をきたします(交通性水頭症)。
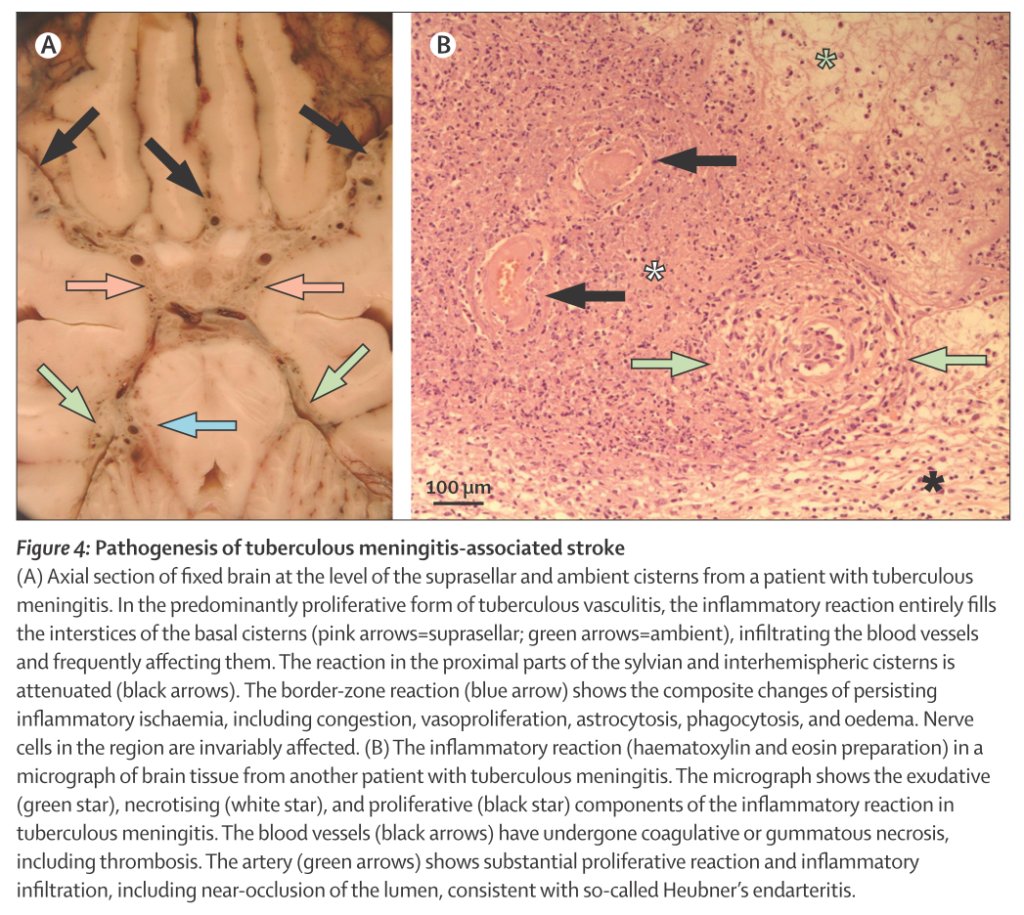
■脳血管障害
脳底部の炎症性浸出物が血管炎、血栓形成、血管攣縮、血管の蛇行を引き起こすことで(特に脳底部において)虚血を起こすとされています。特に脳底部のWillis動脈輪領域が障害されるため、内頚動脈遠位、前・中大脳動脈近位・中大脳動脈穿通枝領域が関係しているとされます。(下図はJournal of Infection (2012) 64, 565より引用・内頚動脈遠位が狭窄して梗塞に至っている。)
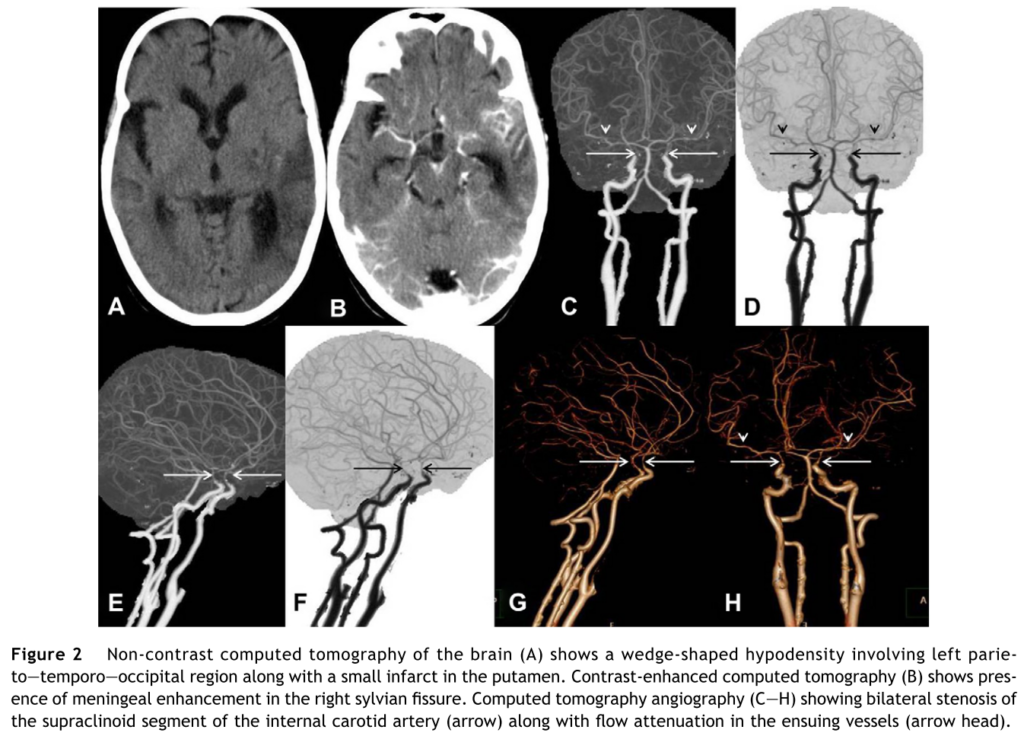
559例の結核性髄膜炎と脳梗塞の関係をretrospectiveに調べた研究(Stroke 2018;49:2288)では、全体の約1/4にあたる26%に脳血管障害合併を認め、73%は急性~亜急性期脳梗塞、梗塞部位としては皮質下白質(46.4%)>基底核、視床(20.9%)>脳幹、小脳(19.8%)の順に障害の頻度が多い結果でした。古典的には“tuberculosis zone”と呼ばれる基底核、内包後脚、視床が障害されやすいとされていますが、この研究では皮質下白質が多い結果でした。また脳血管障害合併は高齢(>40歳)、高血圧、脂質異常症、糖尿病がリスク因子となり、脳梗塞の並存時代が結核性髄膜炎の独立した予後悪化因子となることが指摘されています。
ステロイドは結核性髄膜炎の死亡を抑制することは知られていますが、ステロイドにより脳血管障害合併を抑制出来ないとされています。アスピリン併用により脳梗塞合併を抑制できるか?に関しては、118人の結核性髄膜炎患者をアスピリン群とプラセボ群に分けて行われたopen-label RCTがあり、3か月後の脳梗塞合併で有意差はないもののアスピリン併用で少ない傾向(24% vs 43%、有意差なし)にあり、死亡は有意に抑制する結果(21.7% vs 43.0%, P=0.02)でした(Journal of the Neurological Sciences 293 (2010) 12)。現状は絶対的に使用するべきとまではいかず、使用を考慮するくらいの推奨度かと思います。
検査
髄液検査
髄液所見で「単核球有意の細胞数上昇+髄液糖低下」を認めた場合は、基本全例結核性髄膜炎を鑑別に入れるべきです。結核性髄膜炎は相手から「結核ですよー」と教えてくれることは決してなく、こちらから積極的に疑いに行く姿勢が求められるため、基本的な髄液検査の結果解釈も慎重に行う必要があります。
個人的には結核性髄膜炎は髄液蛋白がかなり上昇する印象があります。
髄液糖低下は重要な点なのでここで鑑別をまとめます。髄液糖低下では細菌性・真菌性・癌性・結核性を必ず考慮します。

■髄液ADA
ADAはアデノシンをイノシンに変換する酵素で、特にT細胞に多く認めます。このため、ADA高値はT細胞が活性化している病態を反映するとされており、結核の診断において補助的役割を担うことが知られています。このことからも分かるように、結核と1対1対応の検査ではありません。ここでは髄液ADAの検査特性に関してまとめます(以下単位はIU/Lです)。
以下は”Scandinavian Journal of Infectious Diseases, 2010; 42: 198–207″より参照します。ここでは、髄液ADA値と結核性髄膜炎における感度、特異度が以下の様に指摘されています。
1以下:Sn100%, Sp6%
8以上:Sn59%,Sp96%
20以上:Sn16%, Sp100%
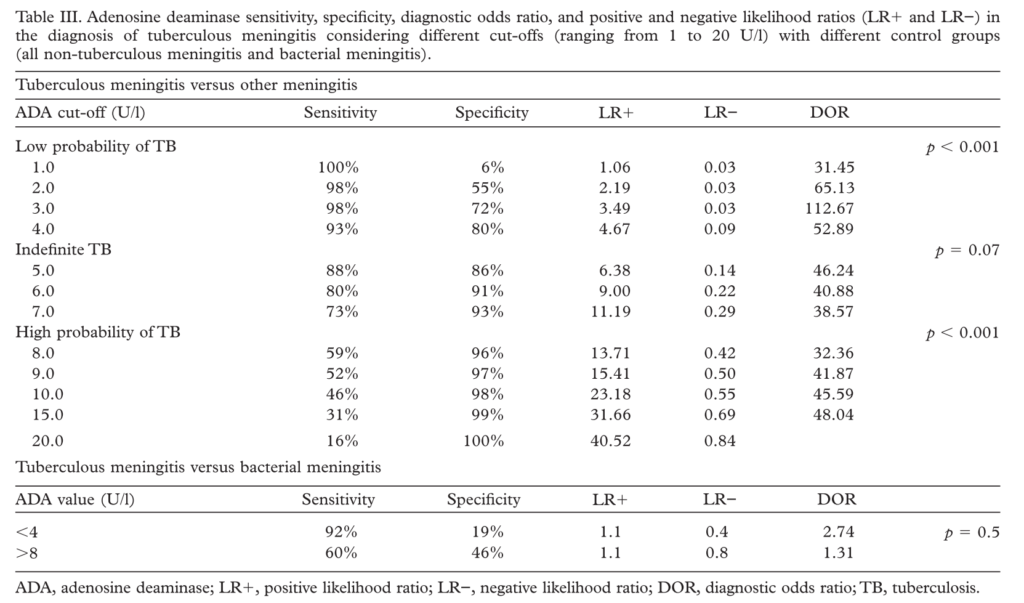
しかし、実際には髄液ADA>20となる結核性髄膜炎以外の疾患の症例報告もあります。具体的には、リステリア髄膜炎、ブルセラ髄膜炎、低γグロブリン血症に伴うエンテロウイルス髄膜炎、神経サルコイドーシス、中枢神経原発悪性リンパ腫、無菌性髄膜炎(CID 1997;25:1275)、ヘルペス脳炎(CID 2003;37:147)などが挙げられます。
その他のsystematic reviewではADA=9 or 10をcut offとして感度79%、特異度91%と報告されています(Int J Tuberc Lung Dis. 2010 Nov;14(11):1382-7.)。
明確なカットオフ値の設定は難しいですが、ADA>10IU/L周辺から特異度が高くなることがわかります。結核はとにかく「水」関係の培養検査で生えにくいので診断に本当に苦慮します。髄液ADAはあくまで補助的な検査ですが、実臨床では補助データをかき集めて診断に結びつけるケースも多いため補助データ1つ1つの検査特性をしっかり把握して、解釈を正確に行いたいです。
*要注意:GFAP astrocytopathy
・GFAP astrocytopathyは髄液所見で「単核球優位の細胞数上昇+糖低下+ADA上昇」を認める場合があり、結核性髄膜炎との鑑別に難渋した症例報告が多くあります。これはかなり注意が必要です。
・こちらにまとめがありますのでもしこちらをご参照ください。
■結核菌PCR・培養検査
結核はとにかく水での培養がはえにくい傾向にあります。髄液も培養がはえにくく、また培養検査の結果が出るまでに時間がかかってしまう点が問題です。感度は報告によってかなり幅があります。PCR検査といった遺伝子検査を併用しますが通常のPCR検査は感度が低く、後述の”nested PCR”検査が優れた方法です。
*重要:”nested PCR”に関して
・通常の髄液TB-PCR検査は上記の通り感度が低いことが問題であり、より感度を高めた”nested PCR”が感度90%, 特異度100%と報告されています。
・通常のPCR検査では10,000/2μL copy必要なところが、nested PCRでは1~10/2μL copy必要とされており、1000~10000倍の感度を誇るとされています。9例の結核性髄膜炎疑いの症例では通常のPCR検査は2/9例で陽性でしたが、nested PCR検査は9/9例陽性であり、またcontrolの非結核性髄膜炎患者20例の髄液検査は全例nested PCR検査陰性と報告されています。Neurology 2005;64:1789–1793
・保険収載は2022年現在まだされていないですが、現在「保健科学研究所」で外注検査が可能なようです。
画像検査
結核性髄膜炎は特徴的な画像所見があるため診断を補助する上で重要です。tuberculoma(40%)、脳梗塞(27%)、脳底部髄膜造影効果(41%)、水頭症(26%)が代表的な画像所見です(カッコ内の頻度は結核性髄膜炎559例をまとめた論文より引用J Neuroimaging 2019;29:657-668.)。水頭症と脳梗塞に関しては既に記載したので、ここでは省略します。
■髄膜造影効果(特に脳底部)
造影MRI検査が検出に優れています。脳底部の造影効果が特徴的で、結節状の造影効果を持つ場合もあります。
■tuberculoma
脳実質内に認める結節状、リング状造影効果を持つ腫瘤性病変です。3か月以内は治療が奏功していても形成される場合があり、これが出来るからといって治療抵抗性と解釈しないことが重要です。
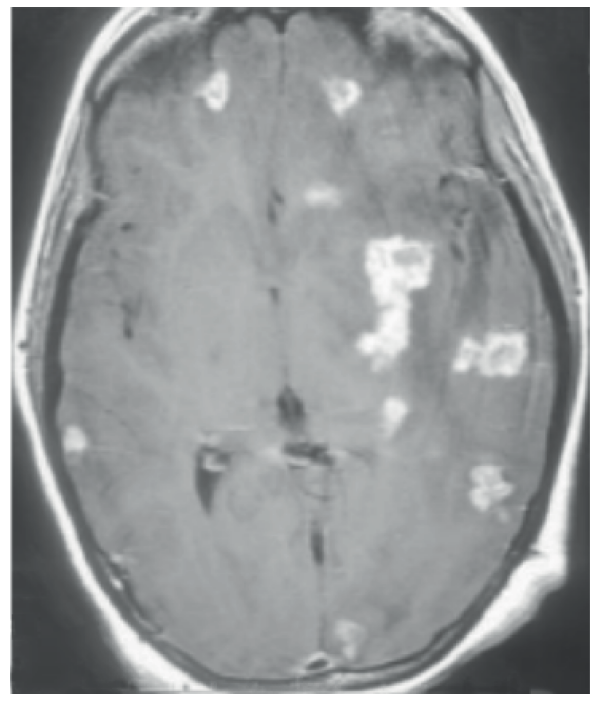
神経放射線の代表的な教科書の”Diagnostic Imaging: Brain”には”combination of meningitis and parenchymal lesions suggests TB.”と記載されており、髄膜炎+実質内の結節状、リング状造影効果をもつ腫瘤は結核性髄膜炎を示唆する所見です。このようにこれらの画像所見はそれぞれ単独では他の疾患でも認めますが、このように組み合わせると結核性髄膜炎の診断に有用です。
“optochiasmatic arachnoiditis(視交叉くも膜炎)”は失明につながるリスクがあるため注意が必要です(下図参照)。
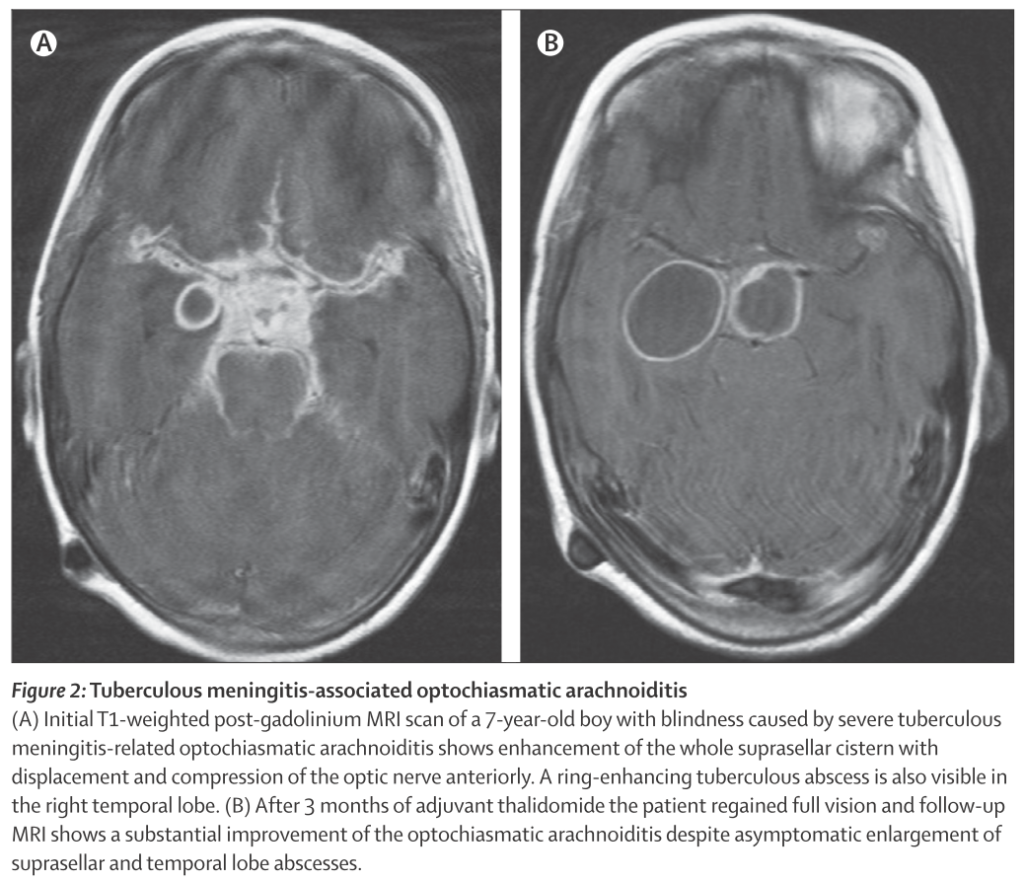
治療
■抗結核薬
結核性髄膜炎における抗結核薬のレジメン、投与量、投与期間がどれが最適なのかはわかっていません。WHOの推奨は2か月4剤併用、残り2か月をリファンピシン、イソニアジドの2剤というレジメンです。結核性髄膜炎での問題は、抗結核薬の髄液移行性です。特に結核においてのkey drugのリファンピシンは髄液移行性が10~20%程度しません(エタンブトールは髄液での炎症下でも通過しないとされています)。以下に抗結核薬の投与量と期間、髄液への透過性、副作用をまとめた図を載せます。
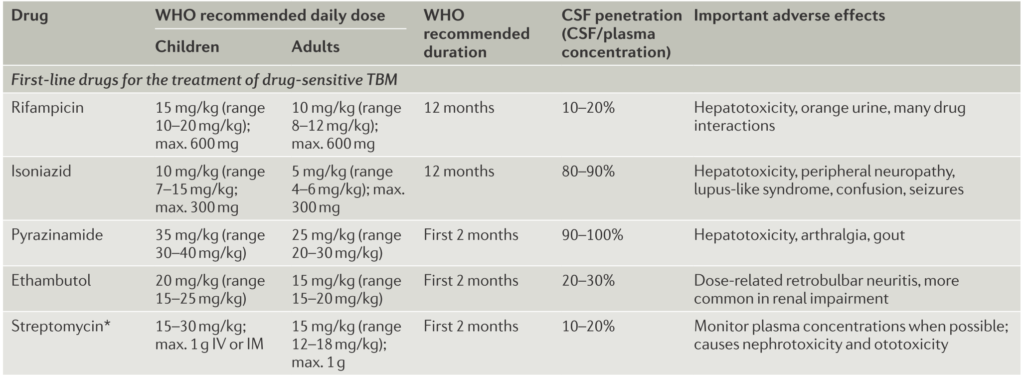
■ステロイド
死亡を30%程度減少することが分かっており、基本的に全例ステロイドを併用することが推奨されます。下にレジメンを載せますが、正確にどの期間投与すればよいかが分かっている訳ではありません。デキサメタゾンを最初の1週間:0.4mg/kg/日、2週目:0.3mg/kg/日、3週目:0.2mg/kg/日、4週目:0.1mg/kg/日と減少し、3~4週間かけて漸減していく方法があります。
*注意点:リファンピシン併用下ではCYP3A4誘導の関係でステロイド投与量を増量する必要があります。プレドニゾロンは2倍量を使用します。この相互作用に関してはこちらをご参照ください。

参考文献
・Lancet Neurol 2013;12:999 比較的新しい結核性髄膜炎のreivew
・Nature reviews neurologyの結核性髄膜炎


