myelin oligodendrocyte glycoprotein antibody-associated disease
病態
・ミエリンオリゴデンドロサイト糖蛋白(myelin oligodendrocyte glycoprotein:MOG)は,中枢神経髄鞘の最外層を構成するタンパク質で、同タンパク質に対する自己抗体(IgG1)が中枢神経脱髄疾患で検出されることから一連の疾患群として認識されています。表現型としては視神経炎、脊髄炎、視神経脊髄炎、ADEM、脳炎(特に「皮質性脳炎」)などを呈し、小児ではADEM、成人では視神経炎の臨床像を呈することが最も多いとされています。
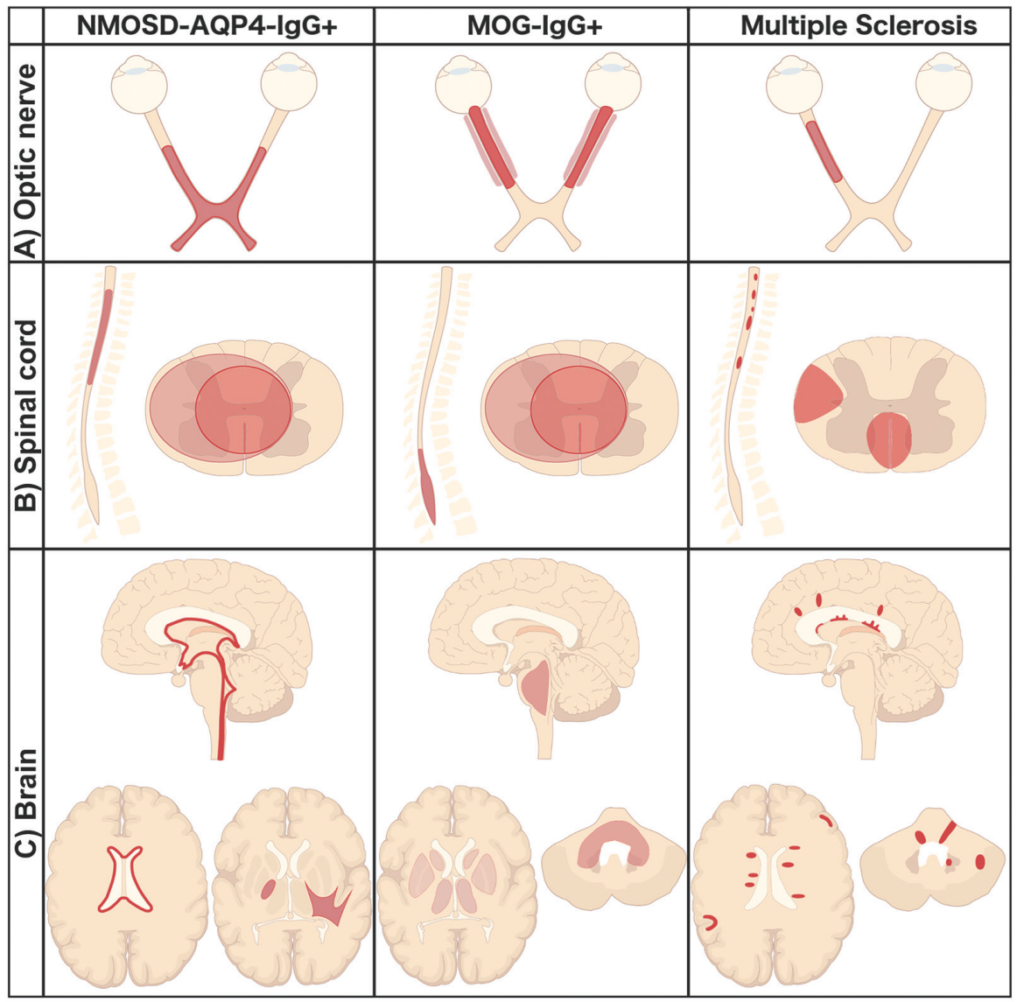
・下図はMS、AQP4抗体関連とMOG抗体関連で視神経病変、脊髄病変、脳病変の違いをシェーマでまとめたものです(RadioGraphics 2018; 38:169–193より引用)。
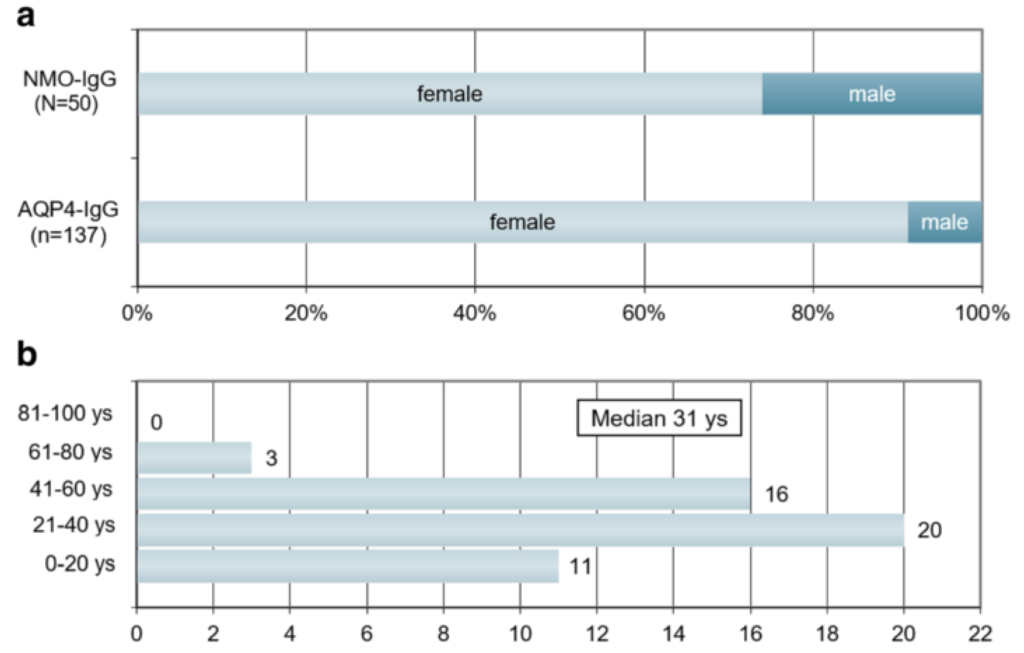
■50例計276例の発作MOG抗体関連疾患のまとめ Journal of Neuroinflammation (2016) 13:280
・疫学:男女比1:2.8、発症時年齢中央値31歳(6-70歳、視神経炎単独は35.5歳、その他は28.5歳)、観察期間75±46.5ヶ月(1-507ヶ月)
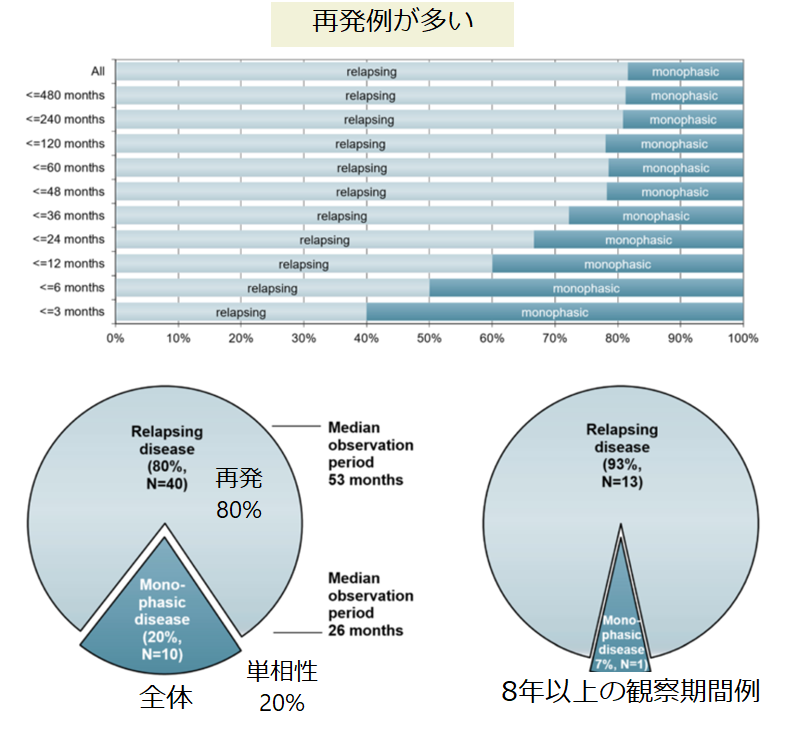
・臨床経過:再発80%、単相性20%(あたり前ではあるが観察期間が長期になるにつれて再発が93%と多い)
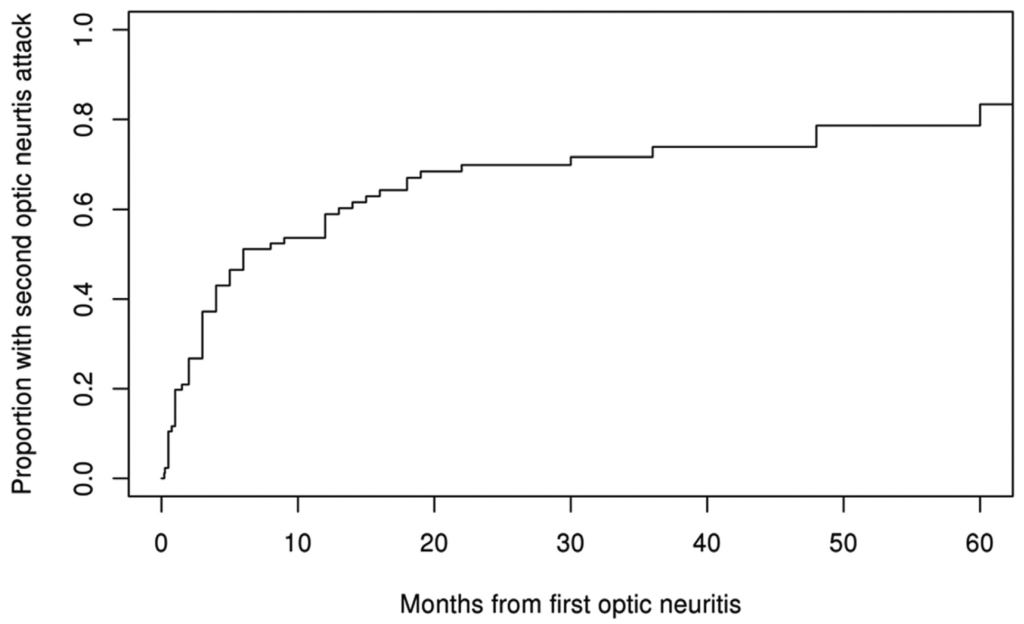
・再発までの期間(初回から再発):中央値5ヶ月
・ARR(anualized relapse rate):0.83(0.05-6.92) ≧12ヶ月以上の観察期間の症例

・初発症状:視神経炎単独64%>脊髄炎単独18%>視神経炎+脊髄炎10%>その他8%
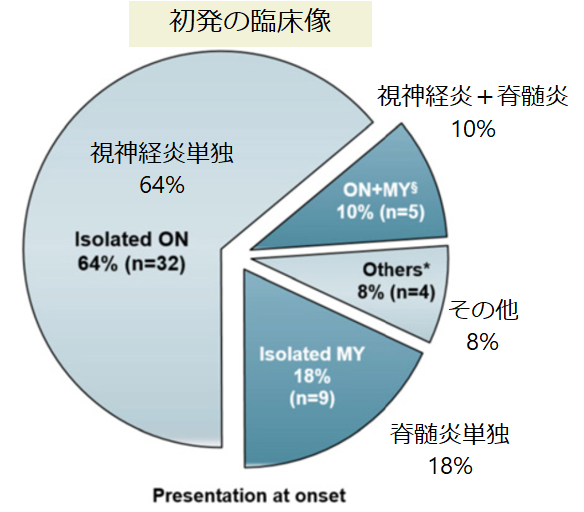
・髄液検査:細胞数上昇>5/μL 69.6%(上昇例の中央値33: 6-303 ≧100/μL:28.1%細胞数が上昇している患者のうち)、QAlb上昇:32.4%(視神経炎単独は13.3%、脊髄炎、脳炎など47.6%)、OCB陽性13.3%(6/45)
・VEP:P100延長72.3%(34/47)(別の12.8%は視神経障害が強く波形同定困難)
・SEP:延長46.2%(19/39)、臨床的に脊髄炎の症例66.7%(16/24)
・自己免疫疾患の合併:8.5%(4/47) RA2例、橋本病1例、バセドウ病1例
・感染症の先行:11例 全ての発作を考慮すると感染が1回でも先行したものは40.5%(15/37)
視神経炎
・MOG抗体関連疾患の表現型として最も多いものが視神経炎です。MOG抗体関連視神経炎の特徴を以下に列挙します。視神経炎の一般論に関してはこちらをご参照ください。
・視神経炎全体でMOG抗体陽性例は約5%。
・再発性の経過をたどるが経過で視力は保たれやすい。
・視神経の前部(眼窩内・乳頭部まで)を障害するため(MSは視神経後部、AQP4抗体関連は視交叉までの長い病変)、視神経乳頭浮腫を認める場合が多く(MSでは球後性視神経炎)、また長い病変を呈する。
・両側性の視神経障害を認める場合も多い。
・画像検査では視神経周囲の造影増強効果を認めることが多い(MS、AQP4抗体関連では認めない 視神経周囲炎に関してはこちらのまとめをご参照ください)。造影効果は視神経周囲の脂肪の信号異常を伴う場合もあります。また”tilting and twisting”と呼ばれる視神経の蛇行や屈曲を認める場合もあります。
・MS, AQP4, MOGそろぞれの特徴をまとめたものが下図になります。
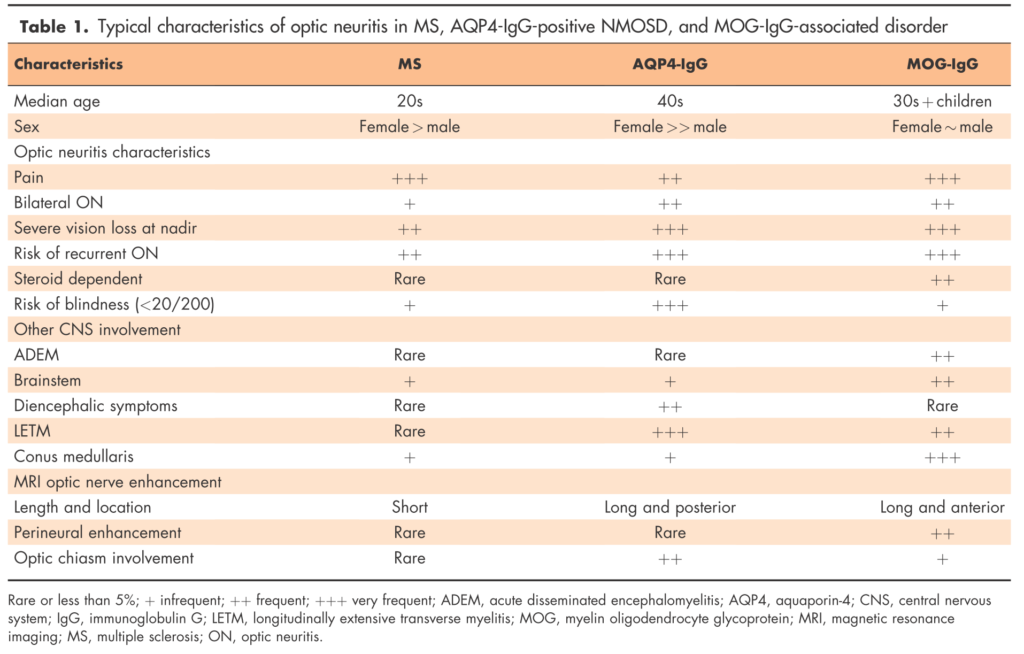
以下が視神経乳頭浮腫の具体例と造影MRI検査の具体例になります。
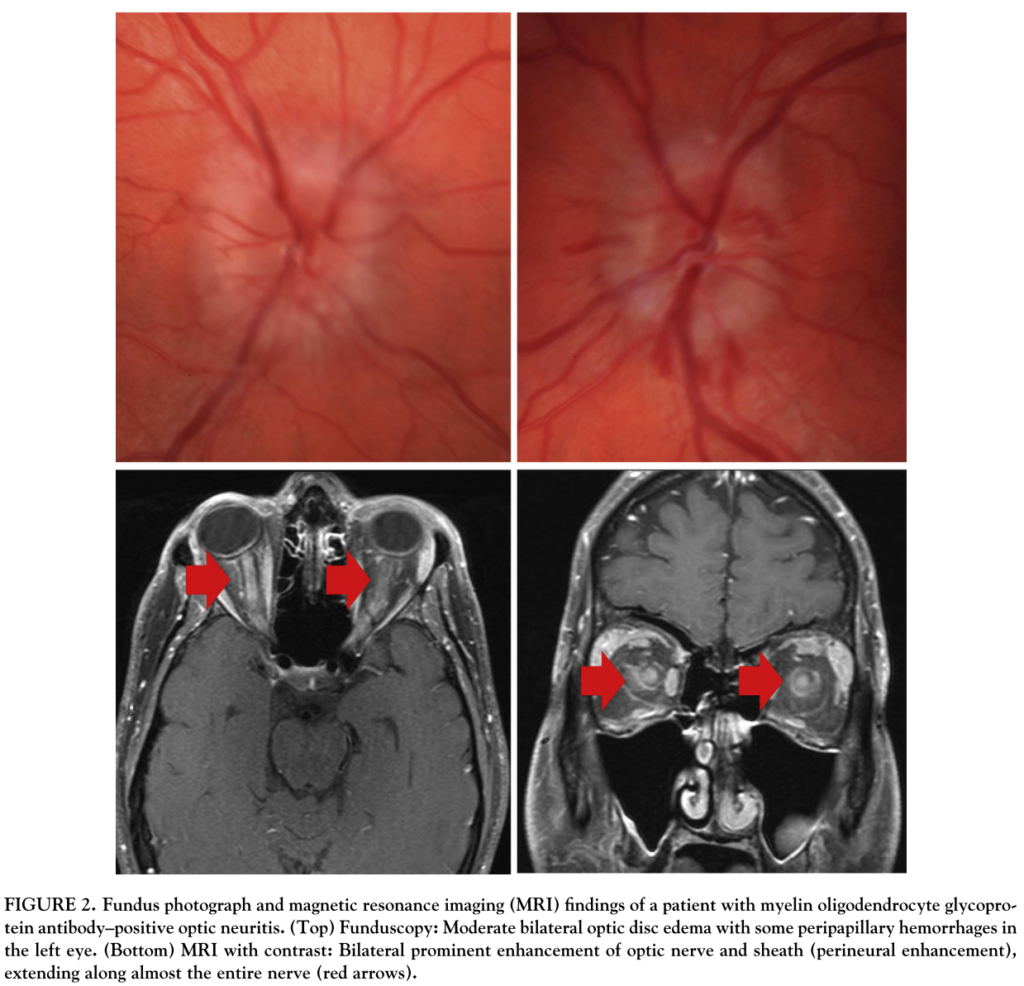
・MRI画像の例は下にも提示します。
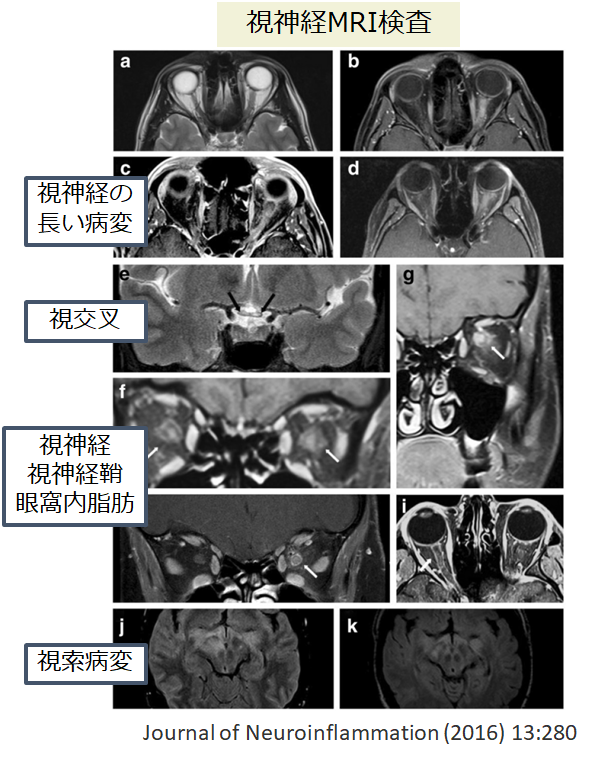
■MOG抗体関連視神経炎87例の検討 Am J Ophthalmol 2018;195:8–15.
・疫学:女性57%、発症時年齢中央値31歳(2-79歳 66%は18歳以上)、視神経炎の回数は中央値3回(1-8回 80%は2回以上の発作)、フォローアップ期間は2.9年(0.5-24年)、初発と再発の期間中央値4ヶ月(1-408ヶ月)、ARR=0.8です。、視神経炎が初発症状82%(視神経炎以外の神経症候を伴わない69%)、その他の神経症状を伴わない再発30%、単相性の視神経炎のみの経過(clinically isolated syndrome)12%
・臨床症状:眼痛(眼球運動に伴う)86%、視神経乳頭浮腫86%、両側同時の障害37%
・その他の神経症状:横断性脊髄炎などのその他の神経症候43%、横断性脊髄炎36%(うち64%は長大病変)
・髄液所見:細胞数増多>5/μL 44%(細胞数≧50/μL 25%)、蛋白上昇>50mg/dL 42%、OCB陽性例なし
・画像所見:造影増強効果100%、perineural enhancement50%、視神経長の半分以上の障害80%、眼窩部92%、頭蓋内72%、視交叉12%、視索2%
・治療内容:IVMP単独83%、IVMP+PE併用9%、IVMP+IVIG併用3%、IVIG単独1%、治療なし3%
脊髄炎
・視神経炎の次に表現型として多いとされています。先の視神経炎はMOG抗体関連らしい所見というものが明確に提唱されていますが(前述の通り)、脊髄炎に関してはMOG抗体関連に特異的な所見というものははっきりしていません。脊髄疾患全般に関してはこちらをご参照ください。
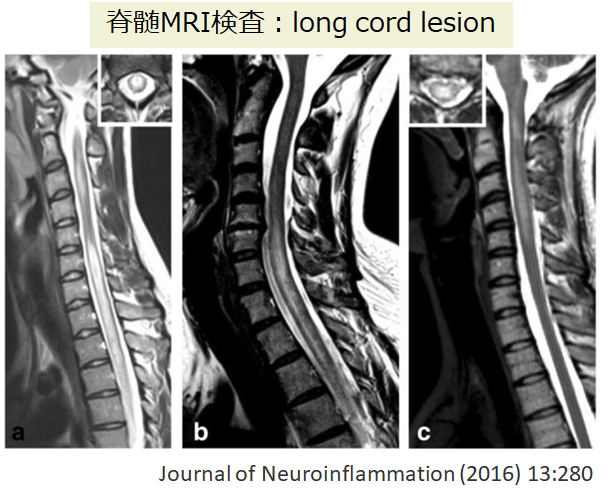
・長軸方向ではlong cord lesionが多いとされていますが、short cord lesionを呈する場合もあります。
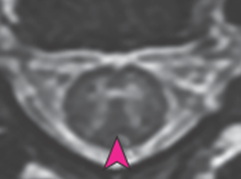
・短軸では灰白質部分に高信号をH字型に認めることが特徴として報告されています。
・部位:胸髄下部~円錐部が障害されやすいという報告(16例のNMOSDのMOG抗体陽性例:MRI病変頸髄16.7%、胸髄100%、腰髄66.7%:Neurology ® 2014;82:474–481)や頸髄病変が多いとする報告もあります。もともとは円錐部に特徴的であると報告されていました。
・先程も紹介した文献(50例のまとめ:Journal of Neuroinflammation 2016;13:280)では、初発時のlong cord lesion64.7%、脊髄腫脹70.4%(19/27)、造影増強効果67.9%、病変分布は頸髄54.3%、胸髄38.3%、腰髄4.9%、円錐部3.7%と報告されており、この報告では決して円錐部病変が多い訳ではありません。
脳炎
・MSやAQP4抗体関連疾患と異なり「皮質性脳炎」を呈することがMOG抗体関連疾患の特徴として挙げられます。皮質性脳炎に関してはこちらのまとめをご参照ください。
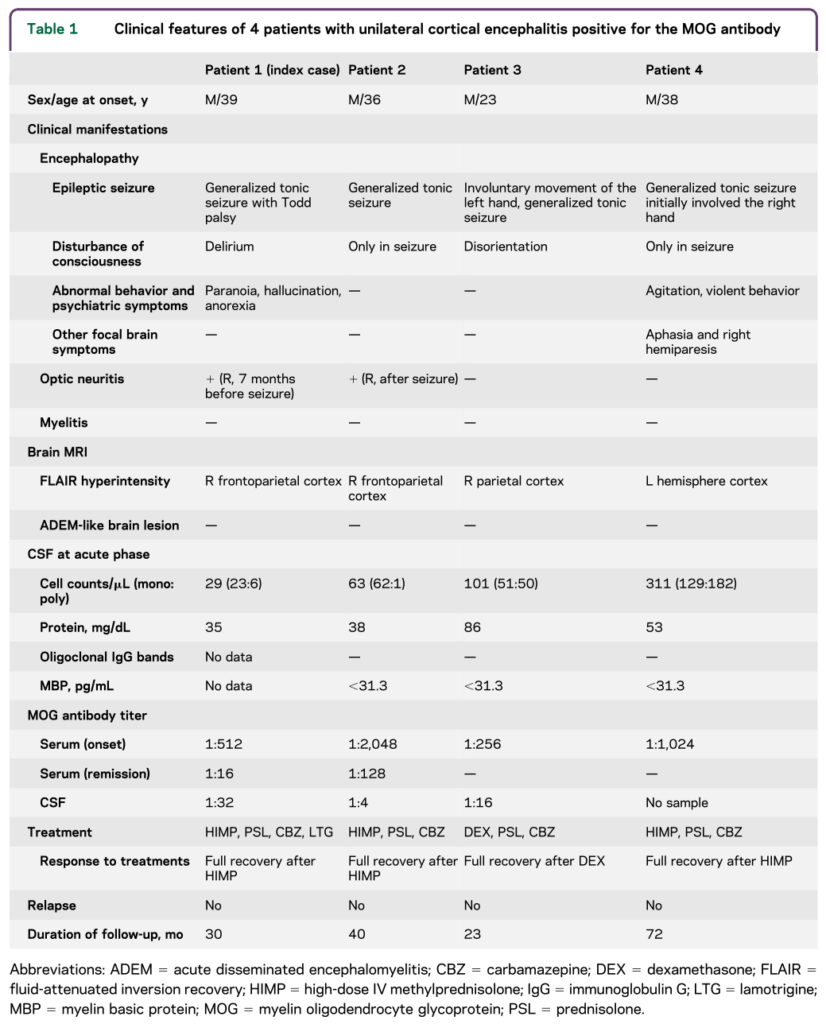
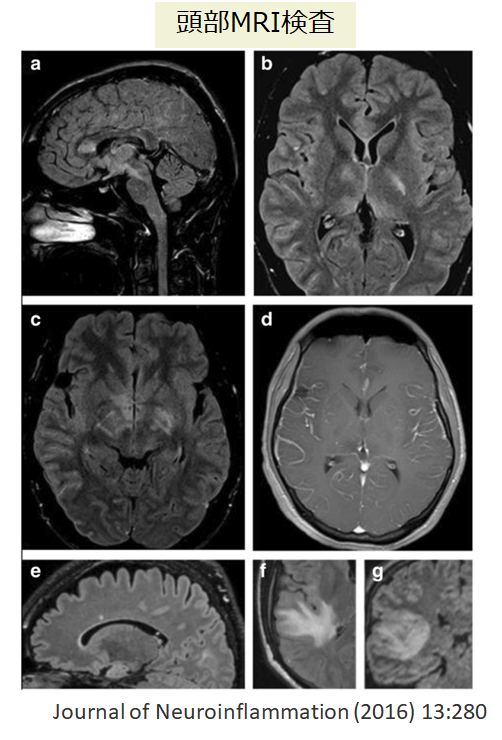
■皮質性脳炎の4例初回報告 Neurol Neuroimmunol Neuroinflamm 2017;4:e322
・患者は23-39歳、全て男性でてんかん発作を発症しています。臨床像は下図の通りで、全例画像ではFLAIRで片側皮質に高信号を認め(DWIやADCよりもFLAIRが明瞭な点がてんかん重積後の画像と異なる)、SPECTでは同部位の血流増加を認めています(日本の東北大学からのご報告です)。
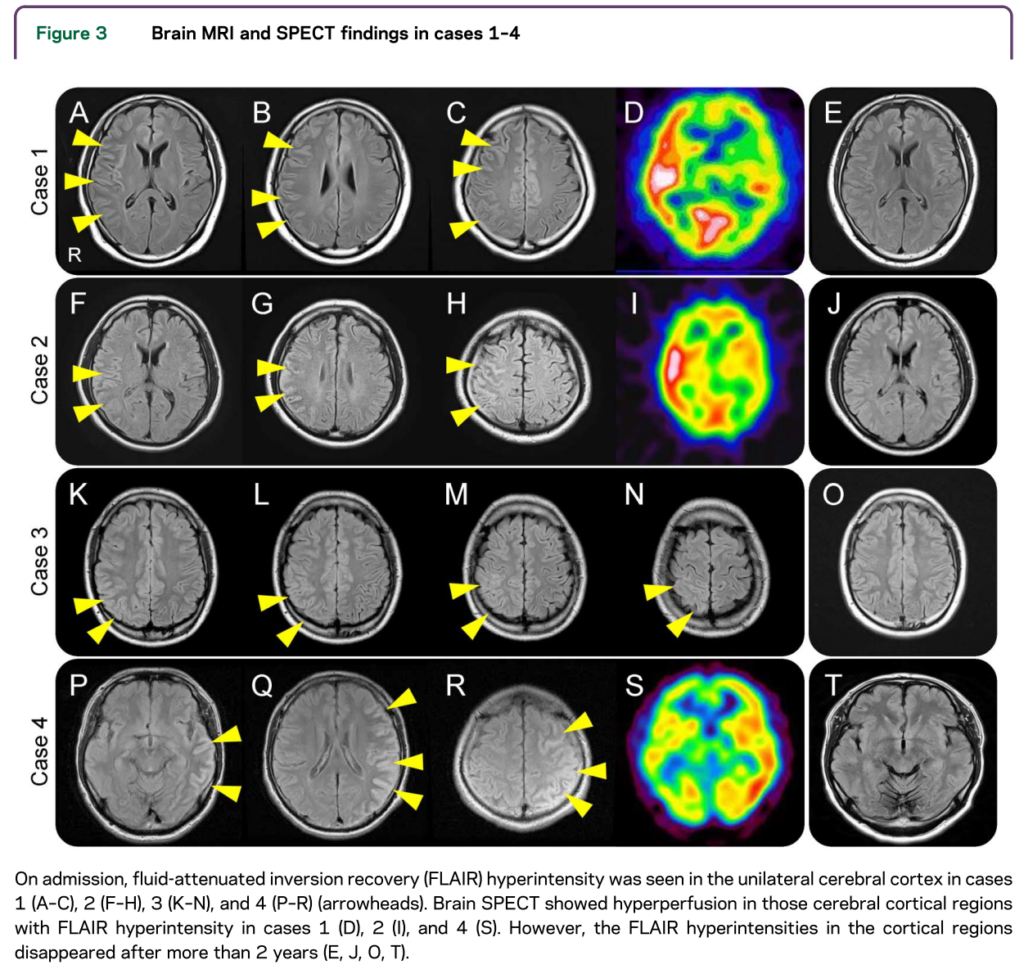
・先程も紹介した文献(50例のまとめ:Journal of Neuroinflammation 2016;13:280)では、発症時のMRIではテント上病変は35.4%、テント下病変は14.6%で認め、経過ではテント上46.8%、脳幹29.2%、小脳12.5%とされています。
診断基準 Lancet Neurol 2023; 22: 268–82.
“Diagnosis of myelin oligodendrocyte glycoprotein antibody-associated disease: International MOGAD Panel proposed criteria” Lancet Neurol 2023; 22: 268–82.
以下A, B, Cを満たす。
A:中核となる臨床的脱髄イベント
・視神経炎
・脊髄炎
・ADEM
・大脳多巣性脱落症状
・脳幹または小脳障害
・皮質性脳炎
B:MOG-IgG抗体(CBA法)
①clear positiveの場合: 追加検査不要
②次いずれかの場合low positive, positive titireなし, 血清陰性で髄液陽性: AQP4抗体陰性+1つ以上の支持的臨床またはMRI所見
*指示的臨床またはMRI所見
・視神経炎:両側性同時の障害、視神経>50%の長い病変、視神経鞘周囲の造影効果、視神経乳頭浮腫
・脊髄炎:長大病変、中心部病変またはH-sign、円錐病変
・脳幹または大脳症候群:複数の境界不明瞭なT2高信号病変
・深部灰白質病変
・境界不明瞭なT2高信号病変で橋、中小脳脚、延髄
・皮質病変と造影効果
C:他疾患の除外(多発性硬化症を含む)
red flags
・発作が無い期間も進行性の障害を認める(MSを意識している)
・数分~数時間以内にnadirに達する急激な増悪
・高用量ステロイド投与にも関わらず改善を認めない
・MRIでの境界明瞭なT2高信号病変、空間的分布パターンがMSに合致する(特にOCB陽性と伴い、新規病変の増加)
・造影効果が6か月以上持続する
MOG-IgG抗体に関して
・血清CBA法かつ定量の測定を推奨
・ELISA法は感度、特異度いずれも不十分でありCBA(cell-based assay)法が望ましい
・診断基準記載の通り低力価の場合は偽陽性の可能性がある(カットオフ値上限の2倍以上)
・髄液MOG抗体の意義に関してはまだ不明点が多い(髄液のみ陽性の場合は偽陽性の可能性がある)
・発症時のMOG抗体力価は予後や再発との相関関係なし
・持続性のMOG抗体陽性は再発リスク上昇する
・典型的なMS画像を呈するMOGADが一部存在する→high efficacy DMDの効果がなければ、診断が間違っている可能性を考慮する
・OCB陽性は~20%で認めるが、MSらしさを上げる(MOGADを除外する訳ではない)
・中枢神経炎症性脱髄疾患においてスクリーニングとしてMOG抗体を提出することを推奨しない
→臨床的にMOGADに合致しない場合は抗体の解釈注意が必要(特に抗体価が低い場合は偽陽性の可能性も充分にありうる) このように抗体陽性のみで診断している訳ではない
・臨床的にclinically definite MSの0.3-2.5%はMOG抗体陽性
*参考:MOG-IgGが陰性でもMOG-IgAが陽性になる症例の報告がある JAMA Neurol 2023;80(9):989-995.
*参考:AQP4とMOGの共陽性は稀→共陽性の場合はAQP4+が高力価で、MOGが低力価、AQP4+NMOSDに準じた臨床像を呈する(そもそもAQP4+の場合MOGを提出する意義に乏しい)
治療
・急性期治療としては一般的にステロイドパルス療法(IVMP)3-5日間を行うことが多いですが、報告では血漿交換療法や免疫グロブリン療法(IVIG)を行うこともあるようです。治療の前向き研究はなく、エビデンスレベルはいずれも高くないため基本はNMOSDに準じます。
・ステロイドはtaperしていき(1-3ヶ月)、その後再発がなければステロイドが必要なくなる場合もときどきあります(漸減OFFもトライします)。ステロイド10mg/日以下、発症2か月以内中止例での再発が多いとされているため注意です。
・ステロイド依存性になる場合はsteroid-sparing agentが必要となる場合もあります。以下が治療アルゴリズムの1例です(Curr Opin Neurol 2020, 33:47–54より引用)。
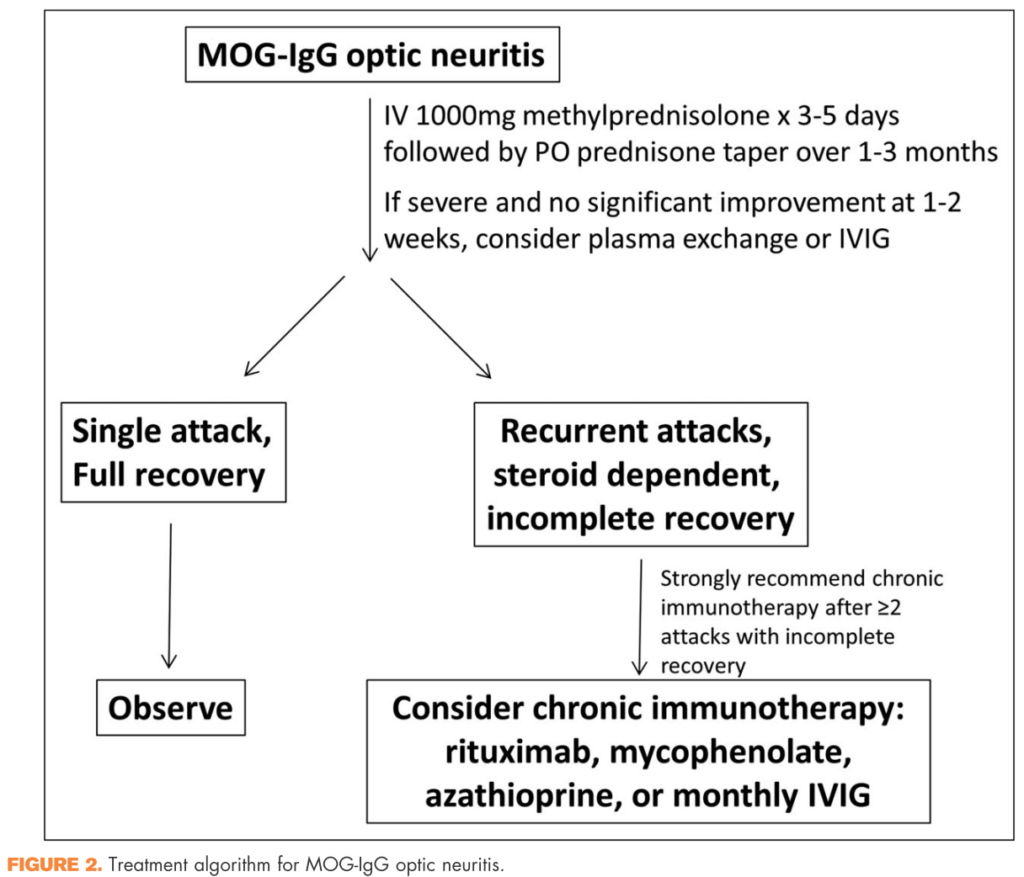
また別のJournal of Neurology (2019) 266:1280–1286では以下のアルゴリズムが掲載されています。
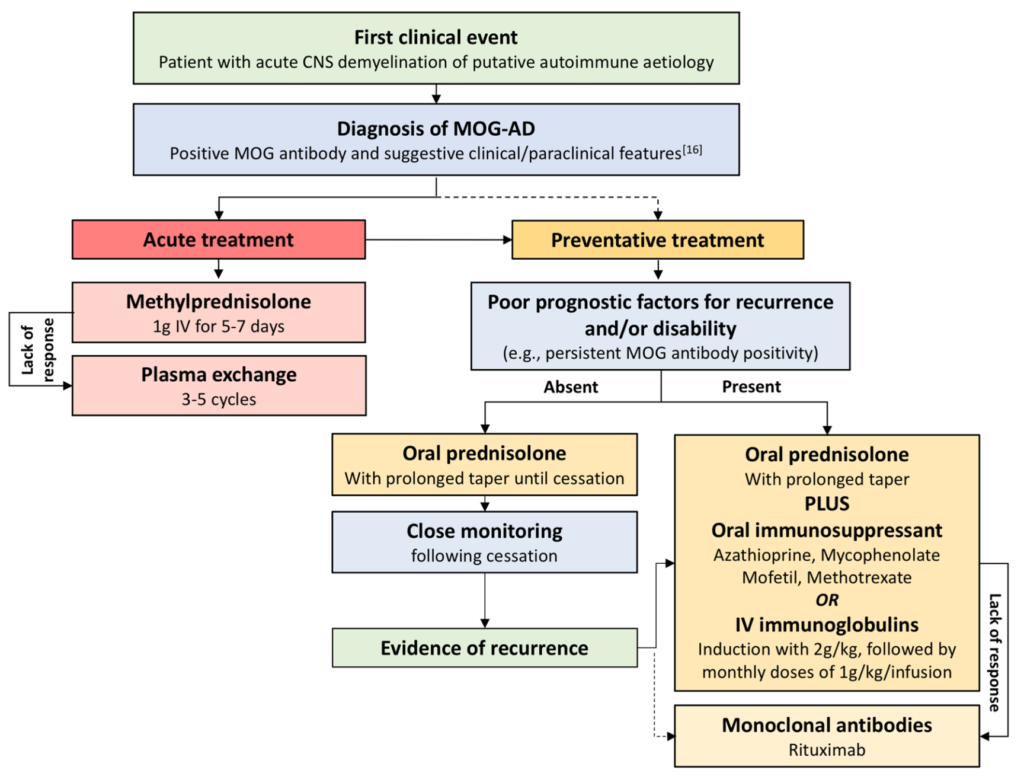
以下では長期(慢性期)の免疫治療に関してまとめた内容を記載します。免疫抑制剤としてはアザチオプリン、MMF、定期IVIG、リツキシマブなどが使用されることがあり、一方でMSで使用されるDMTは効果がないことが指摘されています。
■免疫抑制剤ごとの比較検討 Neurology ® 2020;95:e111-e120
・70例MOG抗体関連疾患:発症年齢29歳 3-61歳、18歳未満は33%、AQP4+は0%、発症時の臨床病型:単独視神経炎47%、横断性脊髄炎11%、NMOSD10%、ADEM31%、再発時の臨床病型:視神経炎96%、横断性脊髄炎49%、ADEM40%、NMOSD37%、再発回数中央値5回、フォロー期間4.5年、ARR=1.6(治療導入前)
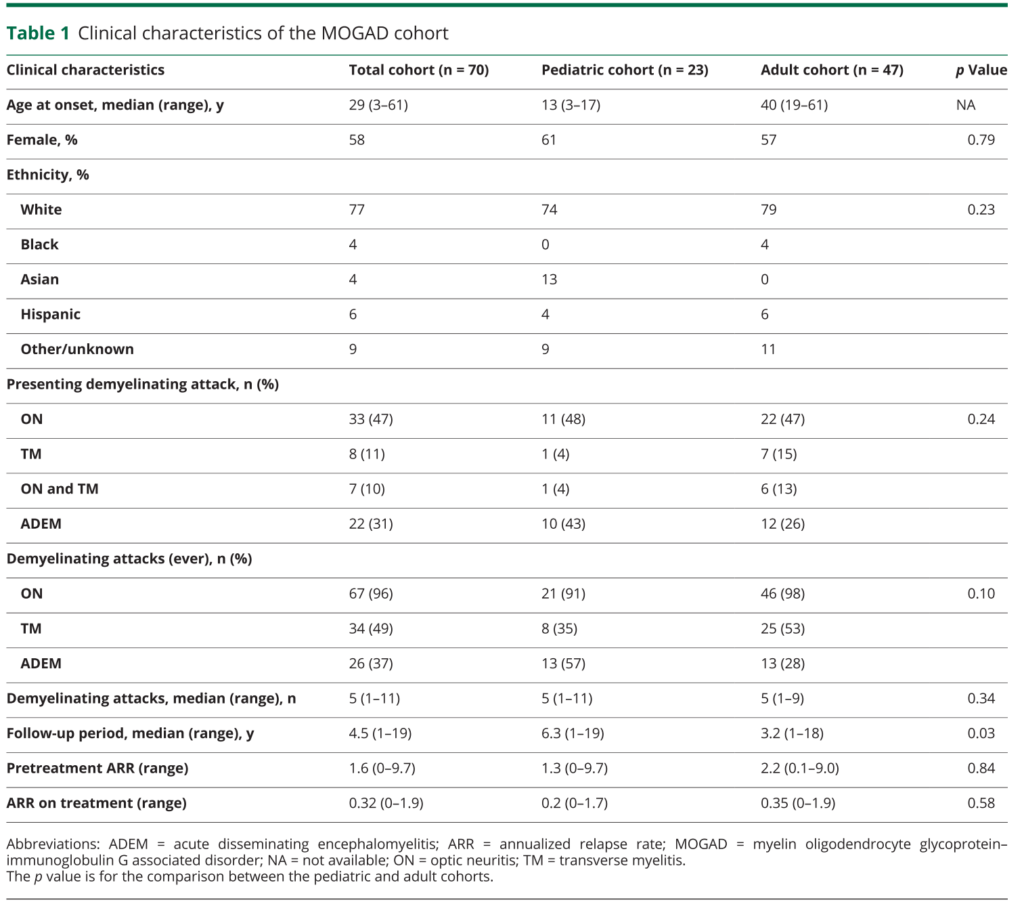
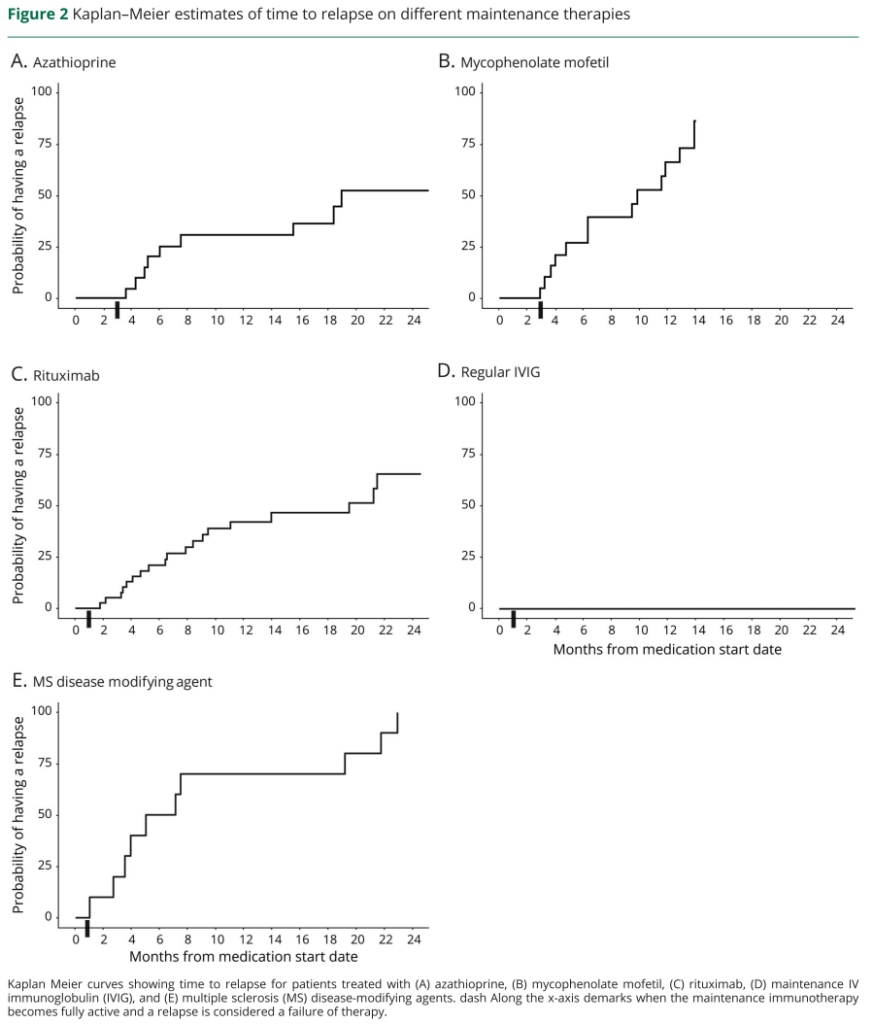
・再発1回以上、免疫抑制剤使用6か月以上を後ろ向きに検討し、各免疫抑制剤ごとにMMF(再発率74% 14/19人・ARR=0.67)、リツキシマブ(再発率61% 22/36人・ARR=0.59)、アザチオプリン(再発率59% 13/22人・ARR=0.2)、IVIg維持3~4週間あけて(再発率20% 2/10人・ARR=0)*内訳は小児5例、成人5例、3例は3週間おき、7例は1ヶ月おき(容量が何gか?に関しては記載なし)、MS疾患修飾薬(再発率100% 9/9人・ARR=1.5)となっています。
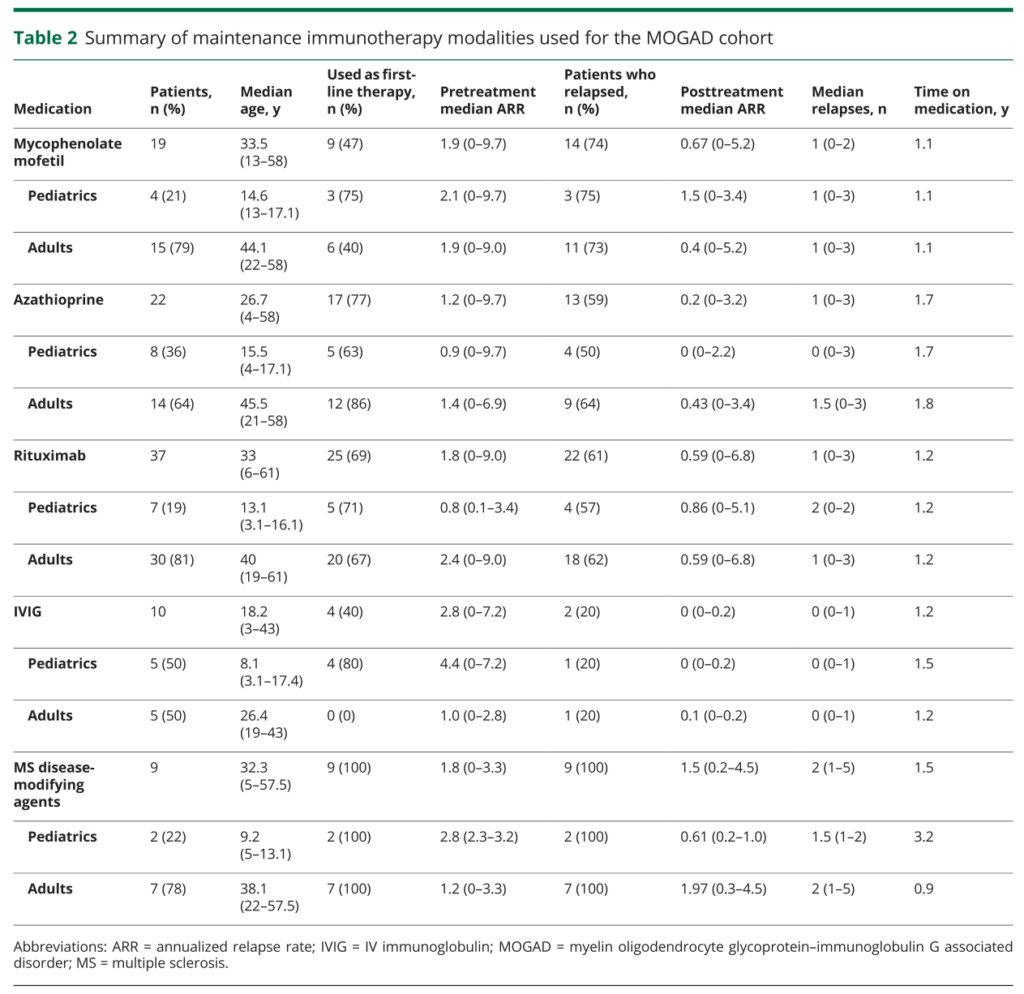
・もちろん後ろ向き研究なので限界はありますが、非常に参考になる結果です。IVIg維持が非常に効果がある点が個人的には意外でした(皆さまの施設はMOG関連疾患の維持としてIVIgをされていらっしゃいますでしょうか?)。次に優秀な結果だったのはアザチオプリンで、実際に使用されている先生も多いのではないかと思います。
■小児例での免疫抑制剤の検討 JAMA Neurol. 2018;75(4):478-487.
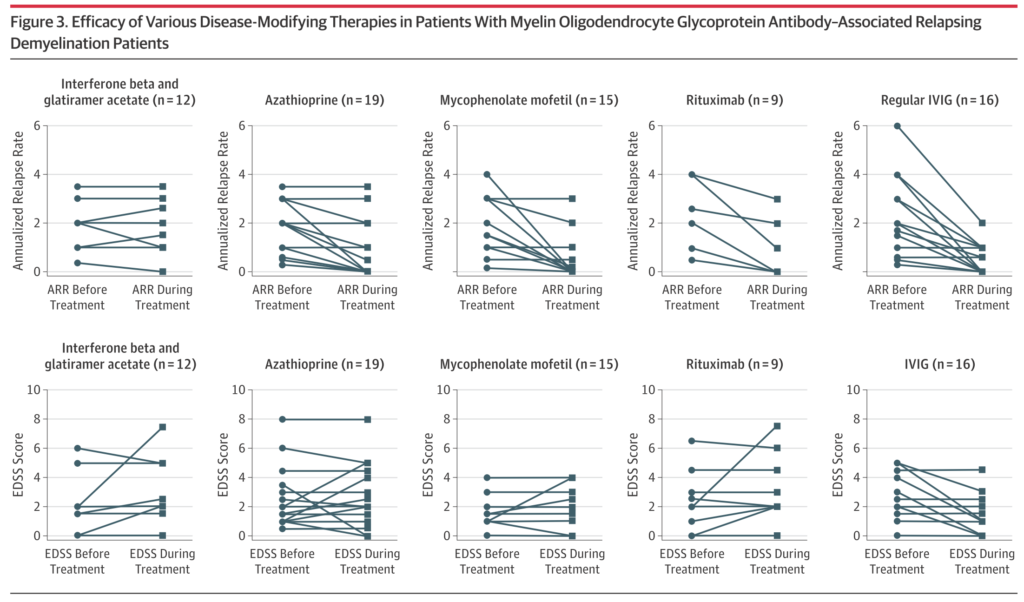
・小児102例(464回の発作)に関してDMD治療介入前後のARRとEDSS scoreを検討した研究です。年齢中央値は7歳、男女比は1.0:1.8、当初の診断はNMOSD43.1%>MDEM19.6%>ADEM-ON19.6%>ROM17.6%(再発性視神経炎)、臨床病型はADEM52.0%>ON40.2%となっています。DMDを投与されたのは51.0%(52例)(内訳:1種類53.8%、2種類32.7%、3種類以上13.5%)で、経過中に再発は127回報告されています。ARRは治療を6ヶ月以上投与された患者のみで検討されています(治療期間が短い時期に再発すると、治療効果を十分に判断出来ないため)。
・IFN-β、GA(n=12)は治療前後でARR、EDSS scoreの変化はありませんでした。
・アザチオプリン(n=20)はARRは1.84→1.0、MMF(n=15)はARR=1.79→0.52、リツキシマブ(n=9)はARR=2.12→0.67へ減少を認めていますが、EDSS scoreは変化していません。
・IVIGを4週間おきに投与された群(n=12)ではARRは2.16→0.51(P<0.01)、EDSS scoreは2.2→1.2(P<0.01)と報告されています。
・まとめ:(小児例に限定されるが)MSのDMTは治療効果がなく、免疫抑制剤(特にIVIG、その他アザチオプリン、MMF、リツキシマブ)は再発予防効果があることが示された(IVIGのはEDSSも)。
参考文献
・Curr Opin Neurol 2020, 33:47–54 MOG抗体関連視神経炎に関する優れたreviewです。
・Journal of Neurology (2019) 266:1280–1286 こちらもわかりやすいreview。
・画像診断 2019 Vol.39 No.3 p:293特集「炎症性脱髄性疾患update」抗MOG抗体関連疾患