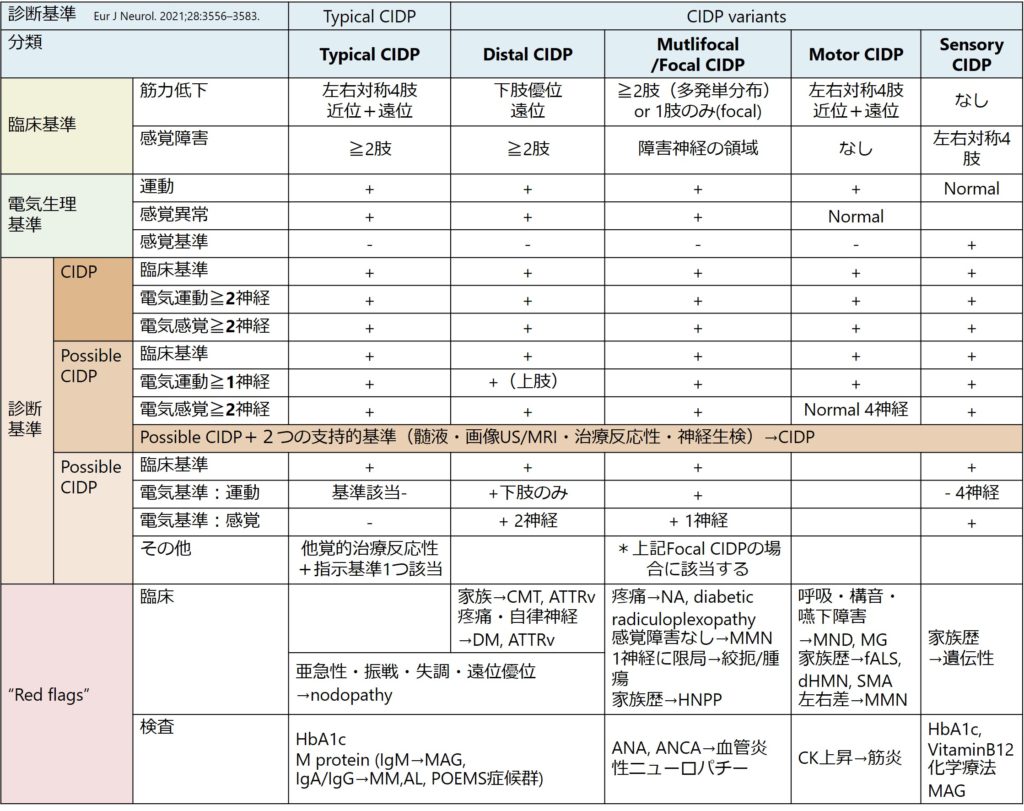
「もう2022年の夏だよ!今更記事作っても遅いよ!」と言われてしまいそうですが・・・、1年遅れでCIDPの新ガイドラインについて簡単にまとめたいです(完全に自分の理解のためです・・・)。CIDPに関しては過去こちらにまとめていますのでご参照ください。前の記事に書き加えると収集がつかなくなるため前の記事とは別に新しい記事にしています。この記事は全体をただ訳すことが目的ではなく、一部私の意訳やコメントが入りますので、「正確な原著が読みたい」という方は元文献(Eur J Neurol. 2021;28:3556–3583. PMID: 34327760.)をご覧になってくださりますようにお願い申し上げます。まずは診断のところで力尽きたので、治療もまた追加していきます。
臨床基準 Clinical criteria for CIDP
Typical CIDP
以下の全てを満たす
・進行性または再発性, 左右対称性, 近位+遠位, 上下肢, 筋力低下+最低2肢の感覚障害
・最低8週間以上かけての進行性経過
・四肢の腱反射低下もしくは消失
・これは元々1976年にDyck先生が提唱していたもので, “proximal=distal, symmetric, motor-dominant”という点がポイントです。”typical”は「近位筋も遠位筋も障害される」という点がポイントでこれは末梢神経障害では特にCIDPとAIDPに特徴的なものです。
・この典型的なCIDPは臨床像と電気生理の実施と解釈がきちんとできればある程度それこそ「典型的」と思います。亜急性の経過で近位筋が障害されるともちろんmyopathyやNMJの障害(MGやLEMS)なども鑑別に挙がりますが、感覚障害を伴う点と腱反射、またその他の随伴所見から(もちろん神経伝導検査の結果からも)鑑別が可能です。
・GBSと違う点としては脳神経障害は少なく、自律神経や呼吸筋障害は例外的であるという点が挙げられます。
・Typical CIDPは急性期でくる場合もありこれをA-CIDP(acute-CIDP)と表現し最大13%程度CIDPを占めるとされています。この鑑別は難しく(こちらの記事参照)、GBSと診断された患者さんのうち約5%がのちにA-CIDPと診断されたとも報告されています。
・個人的には「近位筋の筋力低下+遠位の感覚障害」を伴う場合にこの特異的な分布は “typical CIDP”じゃない?と疑うようにしています(あくまでも個人的な経験論です・つまりmyopathyやNMJの障害なら感覚障害はないし、length-dependent neuropathyなら近位筋力低下はないためです)。
鑑別診断
・ALアミロイドーシス・ATTRv polyneuropathy
・CANOMAD “chronic ataxic neuropathy ophthalmoplegia M-protein agglutination disialosyl antibodies”
・Guillain Barre症候群
・Hepatic neuropathy
・HIV-related neuropathy
・Osteosclerotic myeloma
・POEMS症候群
・Uremic neuropathy
・ビタミンB12欠乏
CIDP variants
・Distal CIDP:遠位の感覚消失+運動障害, 特に下肢優位
・Multifocal CIDP:多発単の分布での感覚運動障害, 通常左右非対称, 上肢優位, 1肢以上の関与
・Focal CIDP:1肢での運動感覚障害
・Motor CIDP:運動症状のみ(感覚障害なし)
・Sensory CIDP:感覚障害のみ(運土症状なし)
・旧名は”atypical CIDP”となっていましたが、別に非典型的な訳ではなくそれぞれの病型に特徴があるということで”variant”という表現に変更となった経緯があります。
・診断上問題なのは圧倒的にこの”CIDP variants”です。
Distal CIDP 旧名:DADS(distal acquired demyelinating symmetric neuropathy)
・特に抗MAG抗体関連ニューロパチー(こちら)との鑑別が問題で、distal CIDPのうち約2/3は抗MAG抗体関連ニューロパチーとされています。
・DADSは”CIDP variants”の中でも特に他の疾患との誤診に注意が必要と思います(下記鑑別が重要)。
・余談:私の所属している医局の教授はよく「DADSは存在しない」と仰っており、カンファレンスで”DADS”という言葉を出すと必ず炎上する風潮があったのですが、文献を調べる限りそんなこともないのではないかと思います。
鑑別診断
・抗MAG IgM抗体ニューロパチー
・糖尿病性ニューロパチー
・遺伝性ニューロパチー:CMT・metachromatic leukodystrophy, Refsum病, adrenomyeloneuropathy, ATTRvポリニューロパチー
・POEMS症候群
・血管炎性ニューロパチー
Multifocal CIDP 旧名:MADSAM
・糖尿病性radiculopathy/plexopathy
・絞扼性末梢神経障害
・HNPP (hereditary neuropathy with liability to pressure palsies)
・MMN (multifocal motor neuropathy)
・Neuralgic amyotrophy
・Peripheral nerve tumors(例: lymphoma, perineurioma, schwannoma, neurofibroma)
motor CIDP, sensory CIDP
・この点に関しては「そもそも存在するの?(motor predominantはあるけど、少なくともpure motorはないんじゃないの?)」という議論があります。
鑑別上のポイント
・疼痛:CIDPはradiculoneuropathyなので疼痛が出ることも多いですがそこまで前景に立たないという点が重要で、血管炎性ニューロパチーは疼痛が目立ちますし(麻薬が必要なことも)、糖尿病性ニューロパチーも疼痛から始まることが多い点に注意が必要です
・自律神経症状:CIDPは自律神経障害の合併が少なく、自律神経障害を伴う場合は特にアミロイドーシスに注意が必要です
・家族歴:成人でも遺伝性の脱髄疾患除外は十分に必要です。また出身地の確認も重要で、集積地ではATTRv polyneuropathy(こちら)も重要な鑑別です。
・電気生理検査:伝導ブロックはまず最大上刺激になっていない”technical error”ではないか?を確認します。伝導ブロックがある場合は同部位に必ず筋力低下を伴うので、筋力低下がないのに伝導ブロック所見を認める場合はまずtechnicalな問題を考慮する必要があります。脱髄疾患は刺激閾値も高くなるので、最大上刺激を十分に得るのに刺激強度がかなり必要となることもあるので十分に注意が必要です。
・Paraprotein:後天性脱髄疾患でまず注目するのが”paraprotein”で全例「免疫固定法」までやって確認する必要があります。こちらのまとめもご覧ください。
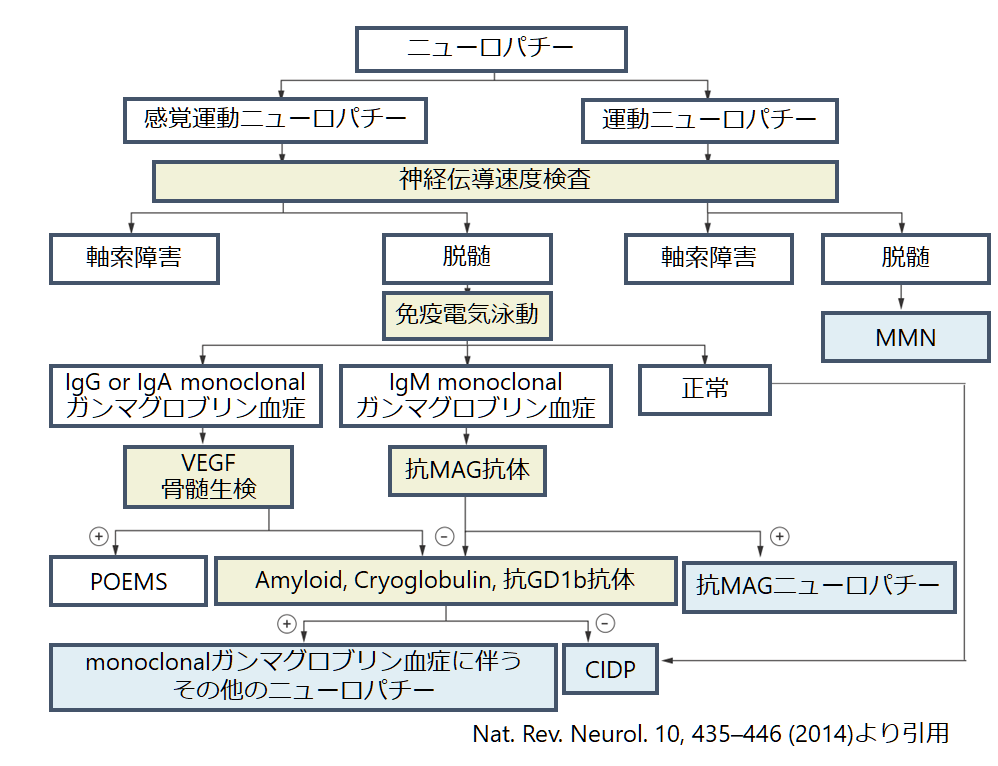
電気診断基準
・これらは病型ごとに別々の基準を設けている訳ではないです。
・過去の診断基準との違いは伝導ブロック(CB: conduction block)の基準が過去はCMAP amplitude “50%”以上の減衰を条件としていましたが、今回は”30%”になっている点です(脛骨神経は生理的にCMAP ampが近位刺激で低下しうるためこの基準から除外している)。
・過去の記事でも取りあげているためそちらも参照いただきたいですが、”AMNS(=abnormal median normal sural)”のパターンはCIDPとAIDPに特異的なので(Suralは神経終末を含まないため神経終末や神経根の病変では障害されない)重要です。神経終末や神経根の障害は神経の長さに関係しないため”non length-dependent”な障害になる訳です。
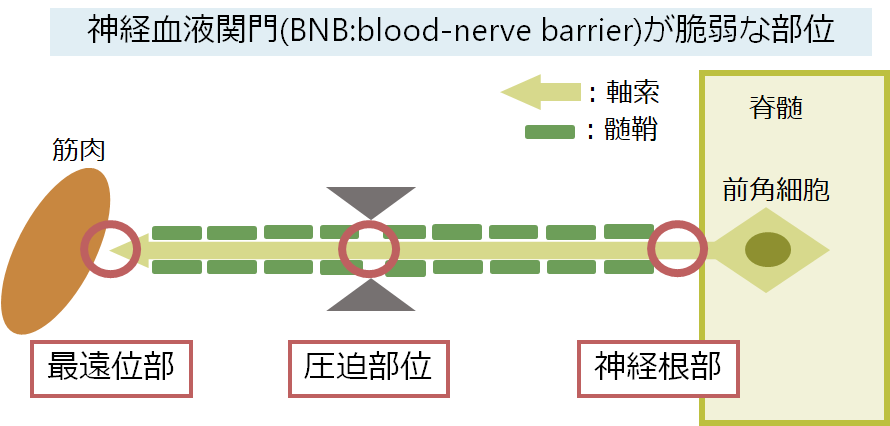
・細かい基準を全て書き出すのが大変すぎるので掲載します。具体的には施設ごとにlow cut filterにより更に色々な記載があるのですが、細かくてややこしいのでここでは省略させていただきます。

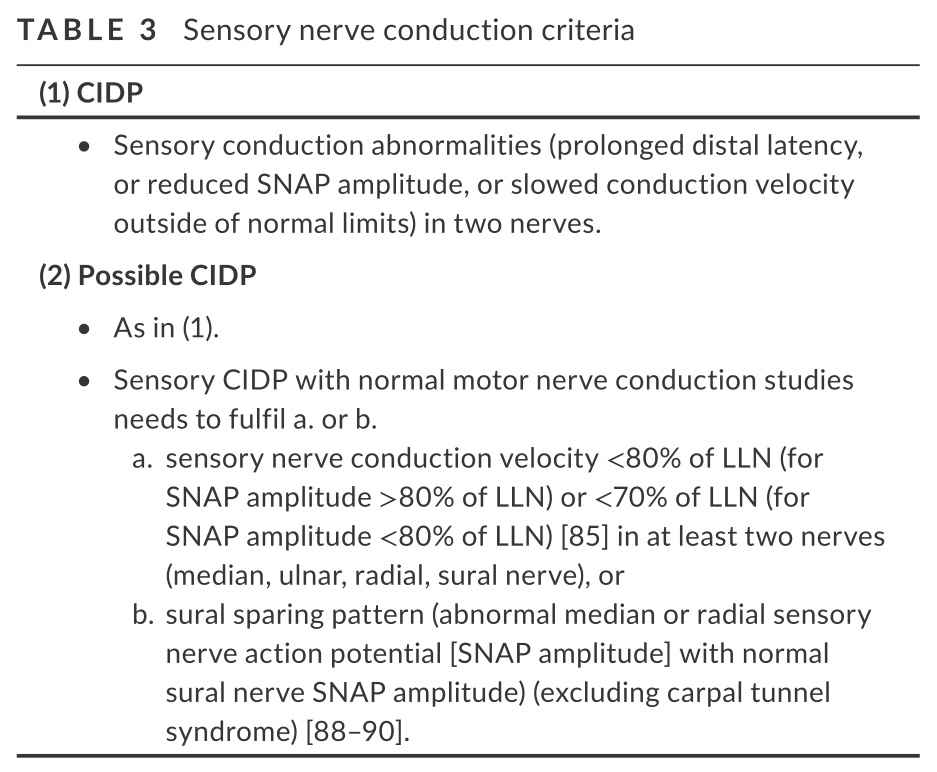
その他の検査所見
採血検査
・paraprotein(M蛋白・免疫固定法):何が何でも必須です。より感度を高めるために免疫固定法を用いるべきです(私の所属している施設で過去に免疫固定法で初めてM proteinが同定された例が実際にありました)。特に”distal CIDP”では上述しましたが、IgM paraproteinが検出される場合は抗MAG抗体の提出をするべきです。またPOEMS症候群を疑う場合は追加で“VEGF”提出を検討します。
・paranodal関連抗体(NF155, CNTN1, Caspr1):ガイドラインでは”suggested to consider testing for nodal and paranodal natibodies in all patients with clinical suspiction of CIDP”とあり、特に以下の項目に該当する場合に推奨されるとされています。
・IVIgやステロイドの治療に抵抗性である場合
・急性もしくは亜急性の経過(GBSやacute-CIDPの診断)
・感覚障害に比して振戦や深部感覚失調が目立つ or その他小脳失調または遠位の筋力低下を伴う場合
・呼吸不全や脳神経障害を伴う場合
・ネフローゼ症候群を伴う場合
・髄液蛋白が著明に高い値の場合
画像
エコー
・ガイドライン上は「超音波検査を実施することを推奨しています(possible CIDPの場合)」
MRI
・ガイドライン上は「MRIを使う事を推奨しない( “・・・suggested not to use MRI in adult patients”」となっています。
髄液
・ガイドライン上は”suggested no to perform CSF analysis if diagnostic criteria are already met”と記載がありますが、さすがに実際は必ず採取することが多いと思います。
・髄液蛋白の解釈は特に糖尿病患者や高齢者では注意が必要です(高齢者での具体的なcut-off値は確立していない)。またCIDPの診断における髄液蛋白上昇の特異度は分かっていません。特に電気生理検査で診断が確定的ではない状況で髄液検査の蛋白上昇に頼ってCIDPの診断をすると誤診するリスクがあるため注意が必要です。
・髄液細胞数上昇は感染症や腫瘍、サルコイドーシスといった他疾患の除外に有用なので、やはり重要と思います。
*50歳以上を60m/dLのカットオフとする報告や、50歳以上を50mg/dL, 60歳以上を60mg/dLとする報告もあります。
神経生検
・神経生検をルーチンで行うことを推奨せず、特殊な状況のみで考慮することを推奨しています。
・他疾患としてアミロイドーシスやサルコイドーシス、CMT,neurofibromatosisなどが考慮される場合に実施を検討します。
診断基準