病態
・JCVは多くの場合(日本は70%以上)既感染(腎臓・脾臓・骨髄)で、免疫低下に伴いウイルスが増殖すると脳へ血行性感染をきたし、中枢神経に脱髄をきたし、不可逆的な障害をきたす病態です(その他JCVによる中枢神経障害にはJCV髄膜炎、JCV 脳症、JCV小脳顆粒細胞障害がありますがここではPMLのみを取り上げます)。免疫抑制を扱うすべての科で重要なテーマです。
原因
・HIV感染症による免疫不全
・血液疾患/悪性腫瘍
・臓器移植後
・自己免疫疾患:SLEが原因として最も多く報告されている
・モノクローナル抗体:ナタリズマブ、リツキシマブ
・その他:特発性 CD4 陽性リンパ球減少症(ICL)、免疫正常例でも報告はある
*参考:PML発症の報告がある薬剤まとめ Clin Exp Neuroimmunol 9(Suppl 1): 37-47, 2018
・経口糖質コルチコイド:すべて
・アルキル化薬:シクロホスファミド,ダカルバジン,camstine
・プリン代謝拮抗薬:フルダラビン,アザチオプリン,クラドリビン
・葉酸代謝拮抗薬:メトトレキサート
・抗体医薬品:ナタリズマブ,リツキシマブ,エファリズマブ,アレムツズマブ,ベリムマブなど
・免疫抑制剤:シクロスポリン,シロリムス,ミコフェノール酸モフェチル,タクロリムス,ミトキサントロン
・その他:ジアフェニルスルホン,フマル酸(BG-12),フィンゴリモド,ビンクリスチンなど
臨床像
・通常発熱や髄膜刺激徴候は認めません(血液検査では炎症反応上昇も認めない)。亜急性の経過で病変を呈する部位のfocal neurological signを呈しますが、PMLに特異的な神経所見はなく、臨床像だけから他疾患と鑑別することは困難です(唯一「失語」に関してはMS患者さんが呈することはまれであり、PMLに特徴的な症状であり注意)。ただ進行性の病態であることは重要です(つまりある疾患を想定して治療しているにもかかわらず増悪する経過の場合立ち止まって本疾患を考慮する必要があります)。このためリスクのある患者では後述の画像検査から積極的に本疾患を拾い上げて疑うことが重要です。
・認知機能障害44.8%、構音障害41.8%、片麻痺32.8%、小脳失調22.4%、失語20.7%、視力障害20.7%、精神症状20.7%、脳幹症状19%、深部腱反射亢進17.2%、不随意運動13.8%、嚥下障害13.2%、無言性無動12.1%(PML診療ガイドライン2017より)
画像
・臨床像だけから診断することは困難でJCVを提出するにあたってリスク因子と画像検査の解釈(+他疾患の除外)が何より重要です。画像検査の果たす役割は本疾患ではかなり大きいと思います。
■PML画像上の鑑別ポイント(神経内科疾患の画像診断 著:柳下章先生 より引用させいただきました)
1:皮質下白質が障害される(一部は拡散強調像で高信号を呈する)*皮質は障害されない
2:T1強調像で低信号(最重要)
3:造影効果, mass effectはいずれも認めない
・皮質下白質病変:初期は脳室周囲~深部白質ではなく、皮質下白質(scalloped appearance)から障害される点がポイントです(白質病変へのアプローチに関してはこちらにまとめがあるのでご参照ください)。部位としては頭頂葉>前頭葉、両側性で多巣性、皮質は障害を免れます。
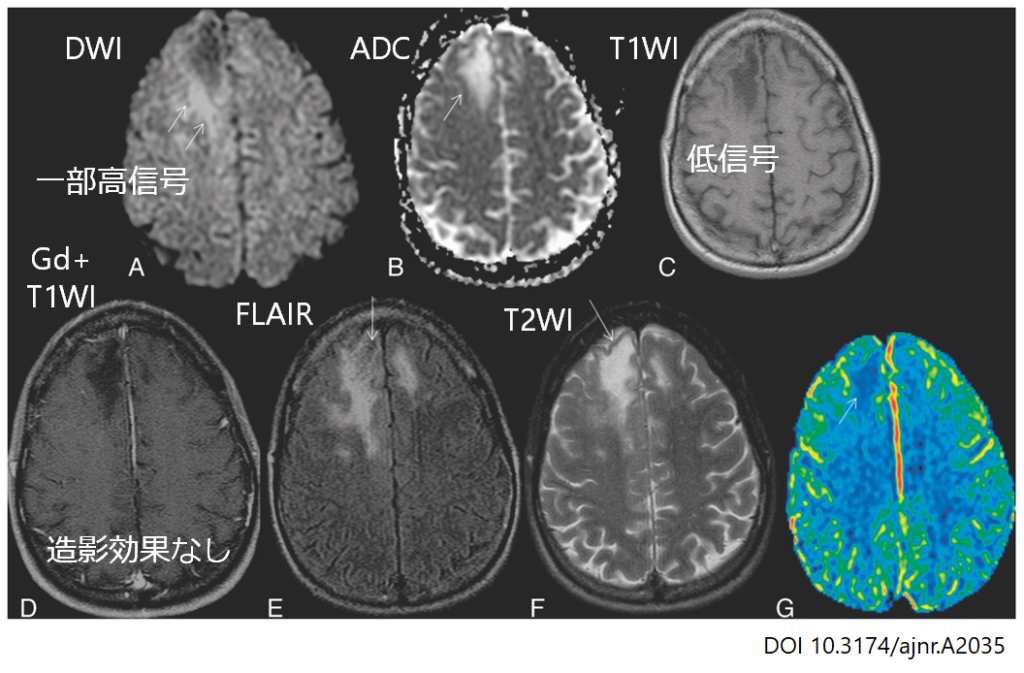
・後頭蓋窩(脳幹・小脳病変):小脳白質を障害し(三日月状: crescent-shaped)、進行すると中小脳脚病変を呈する(中小脳脚病変に関するまとめはこちらをご参照ください)。
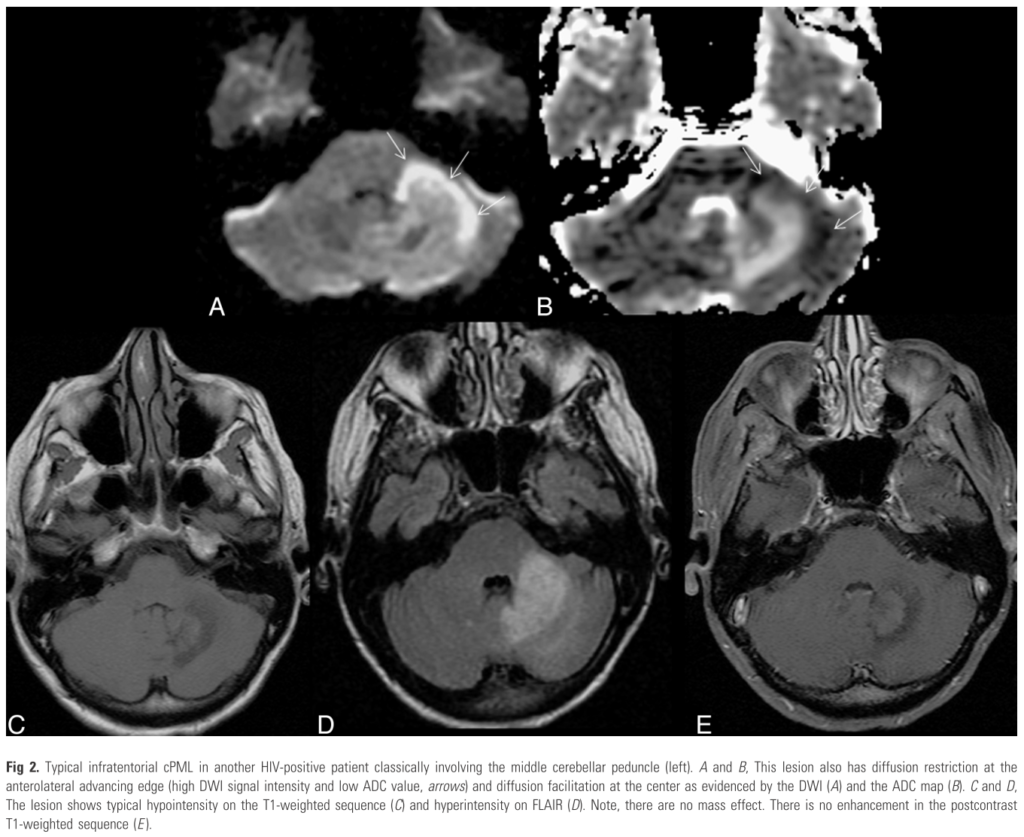
・脊髄病変:呈さない(脊髄病変を有する場合は他疾患を考慮する) *視神経も通常障害されない
*治療に伴うIRISでは造影効果、mass effectを認める点がポイント。
髄液ウイルス検査
・髄液中JCV-DNA検査:感度 72~92%,特異度 92~100%
*取り扱っていただいている医療機関に関して
脳脊髄液 JC ウイルス DNA 遺伝子検査 ホームページ:https://www.niid.go.jp/niid/ja/from-vir1/9458-vir1-div3.html
国立感染症研究所ウイルス第一部第三室(神経系ウイルス室)
・繰り返しJCV-DNAを提出して診断に至った例も報告されており、初回陰性であったとしても臨床像の進展と画像所見から疑う場合は繰り返し提出を検討します(4回目で初めて陽性となった症例報告:臨床神経 2016;56:481-485)。
・複数回提出しても陰性の場合は脳生検を検討します(特発性 CD4 陽性リンパ球減少症が背景にあり、髄液中JCV-DNAが結局4回陰性でその後脳生検で診断に至った症例報告があります:臨床神経 2018;58:750-755)
*髄液検査で炎症所見(細胞数上昇や蛋白上昇など)は通常認めない場合が多いです。
治療
JCVに対する特異的な抗ウイルス薬は存在せず、免疫状態を元に戻すことが治療になります。
1:HIV-PMLの場合:ART
2:non-HIV-PMLの場合
・生物学的製剤使用あり:生物学的製剤中止+単純血漿交換
・生物学的製剤使用なし:誘発薬剤の中止
±上記いずれの場合も重篤なIRIS:ステロイドパルス療法
・多発性硬化症患者におけるナタリズマブ関連PMLでは血漿交換とともにミルタザピン投与も検討。メフロキン(Mefloquine:元々抗マラリア薬)の投与も考慮される。
・その他の非 HIV―PML ではメフロキン,ミルタザピンいずれかの単剤投与を考慮してもよい。
また,メフロキン,ミルタザピン,シドフォビルのうち 2 種以上の併用療法を考慮してもよい。
*5HT2A セロトニン受容体拮抗薬(ミルタザピン,リスペリドン,オランザピンなど)はJCV のオリゴデンドログリアへの侵入を抑制する機序が想定されている。
*その他の抗ウイルス薬(シタラビン,cidofovir など)あるいはIFNαはいずれもin vitroでの有用性であり実臨床での有用性は証明されていない(シタラビン:N Engl J Med 1998;338:1345-1351. /cidofovir:J Neurol 2008;255:526-531. AIDS 2008;22:1759-1767./IFNα: J NeuroAIDS 1996;1:79-88.)。
ナタリズマブ関連PML
■リスク因子の評価(下図引用元:https://www.ema.europa.eu/en/documents/variation-report/tysabri-h-c-603-a20-1416-epar-assessment-report-article-20_en.pdf)
*リスク因子3点 (N Engl J Med 2012;366:1870-80.)
1:抗JCV抗体陽性
2:2年以上のナタリズマブ投与歴(下図縦軸)
3:過去の免疫抑制剤使用歴(下図横軸のIS)
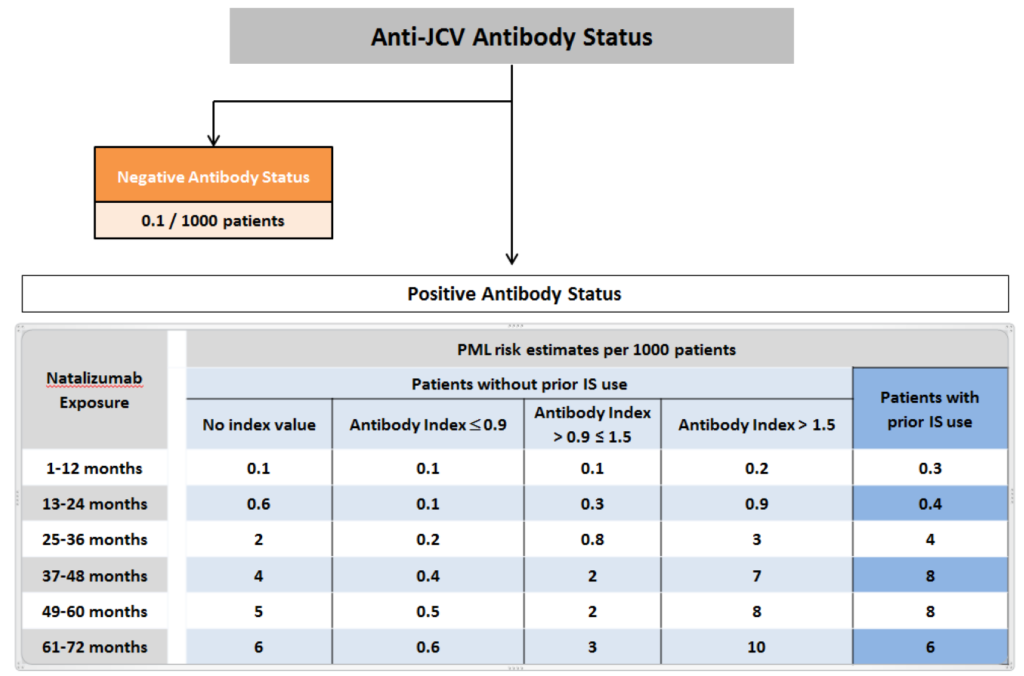
■画像上の特徴:皮質下白質病変が多い。Gd造影効果を認める場合が多い(約40%)点が特徴(通常のPMLとの違い)。*画像は非典型的で多彩な場合もあるため注意が必要。
*natalizumab-associated PMLで特徴的な”punctate pattern”について
・点状のT2高信号病変が病初期の無症候の状態で検出される。これに注意するべき!(私が先日受けたレクチャーでは講師の先生が「これに気が付けないのであればnatalizumabは使用するべきではない」と話されておりかなり自分の診療が不安になりました・・・。髄液DNAもなかなか検出されない場合があるため画像はとても重要です。
→natalizmab使用患者さんでは3~4か月おきにMRI、半年おきに採血でJCV indexをチェックするべき。
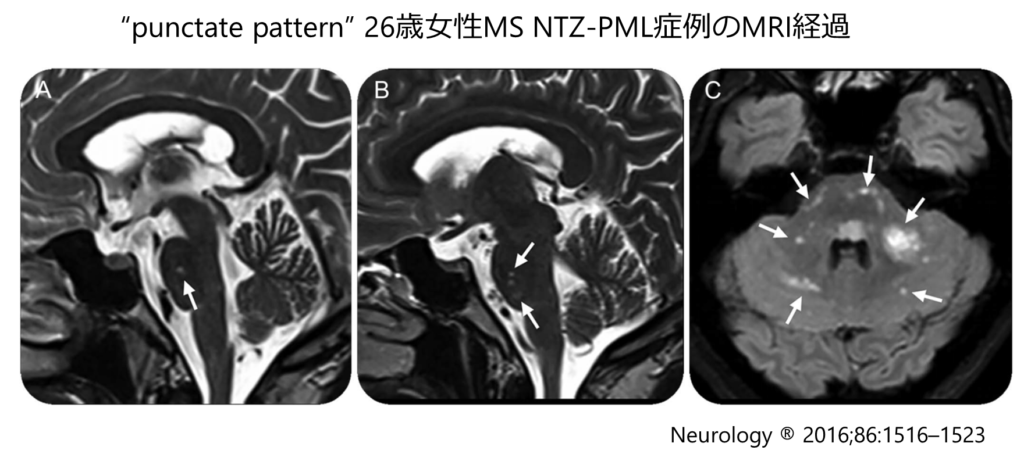
■asymptomatic PML:臨床像が出る前に画像上変化があり髄液からJCV-DNAが検出されることで診断される病態。asymptomatic PMLの段階で治療介入をしたい。
■治療:MS治療薬の中止±血漿交換(ナタリズマブの半減期が非常に長いため)
*IRIS発症が他の原因によるPMLよりも多いため注意が必要
*致死率は約10-20%と他のPMLの原因よりは低い(純粋に治療薬による影響であり、原病自体によるわけではないため)
参考文献
・進行性多巣性白質脳症(Progressive Multifocal Leukoencephalopathy: PML)診療ガイドライン 2017
・臨床神経 2011;51:1051-1057


