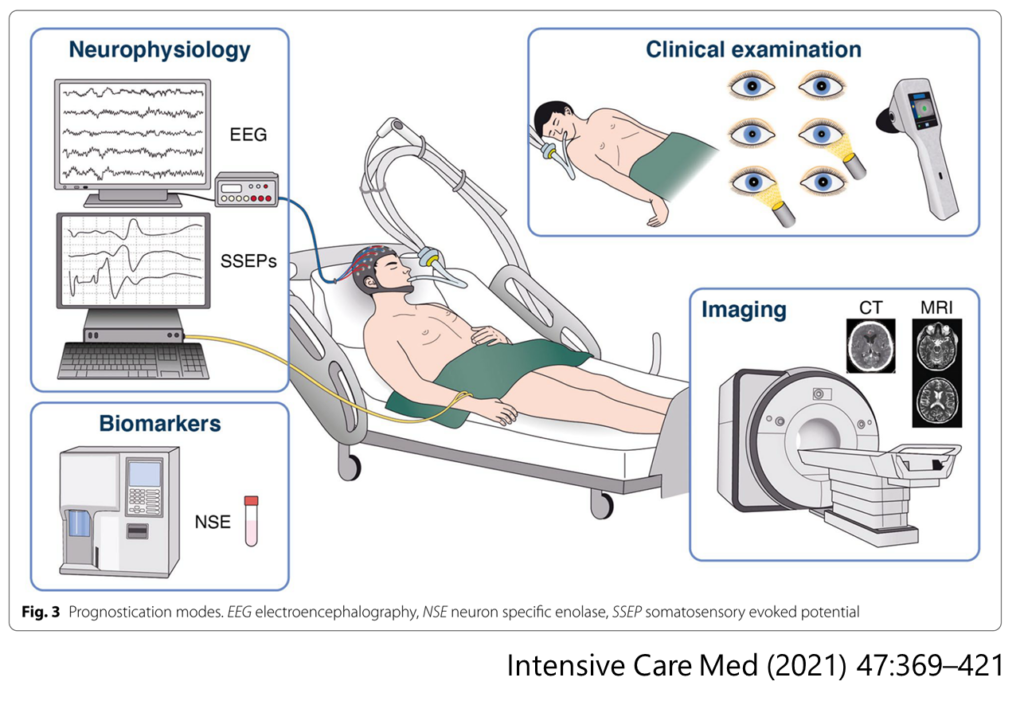
これは倫理的な意思決定支援などにおいて極めて重要かつ慎重な判断が要求されるテーマです。Neurologistがコンサルタントとして関わることも多い領域だと思います。以下ガイドラインを元にして内容をまとめます。”European Resuscitation Council and European Society of Intensive Care Medicine guidelines 2021: post-resuscitation care” Intensive Care Med (2021) 47:369–421
原則・判定方法
・単一の指標で特異度100%ということはありえず、必ず複数の要素を考慮する(multimodal neuroprognostication)必要がある
・評価の際には交絡因子(鎮静薬・筋弛緩薬・低体温・循環不全・低血糖・代謝障害・敗血症など)を除外した状態で評価する
・神経学的予後は純粋に客観的に評価するべきである。この議論に加えて年齢や併存疾患、全身状態や元々の患者さんの希望などを総合してWLST(withdrawal of life-sustaining therapy)をどうするか?を考えていくが、これらの議論を混ぜないことが重要である。WLSTを前提にして神経学的予後を判定すると解釈にbiasが生じるため十分に注意する必要がある(実際に混ざってしまうことは多い)。
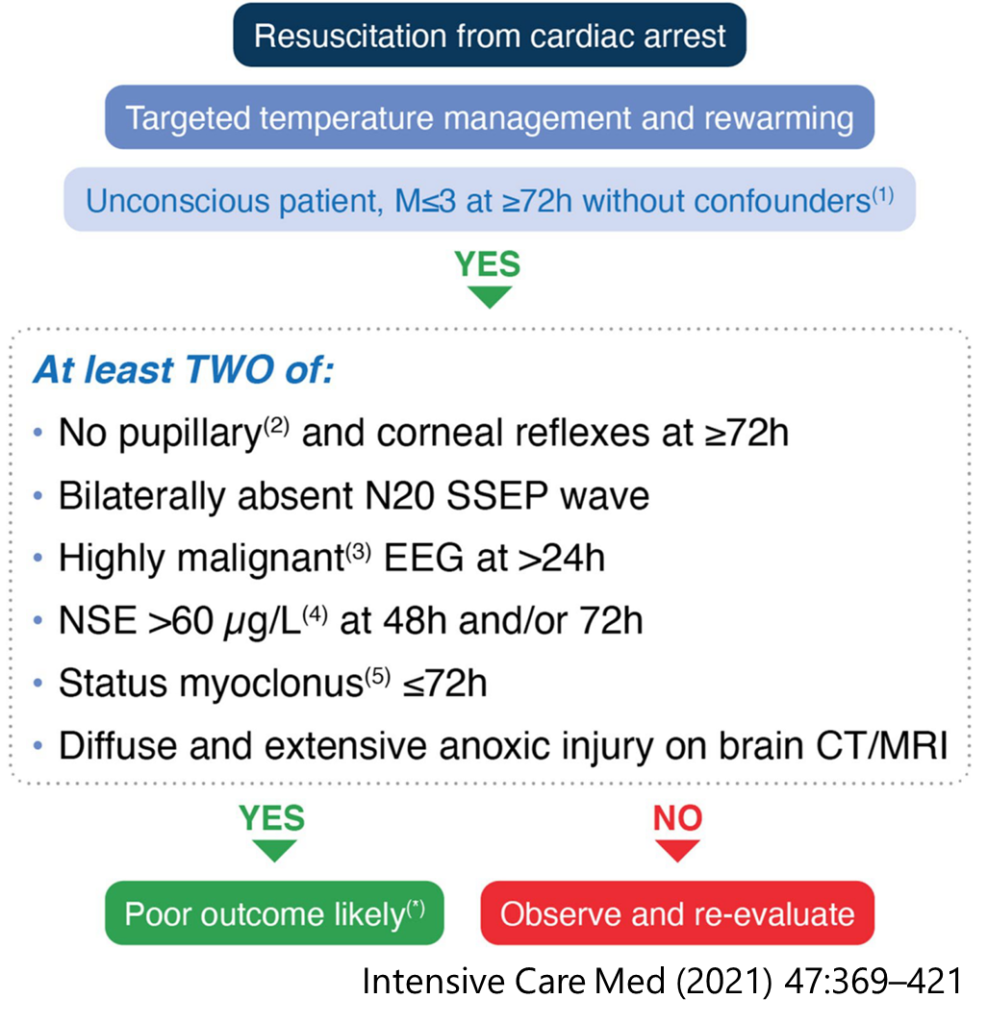
ROSC後昏睡状態・≧72時間交絡因子を排除・M3以下の前提条件を全て満たす+下記の要素2つ以上該当する場合は予後不良と判断する
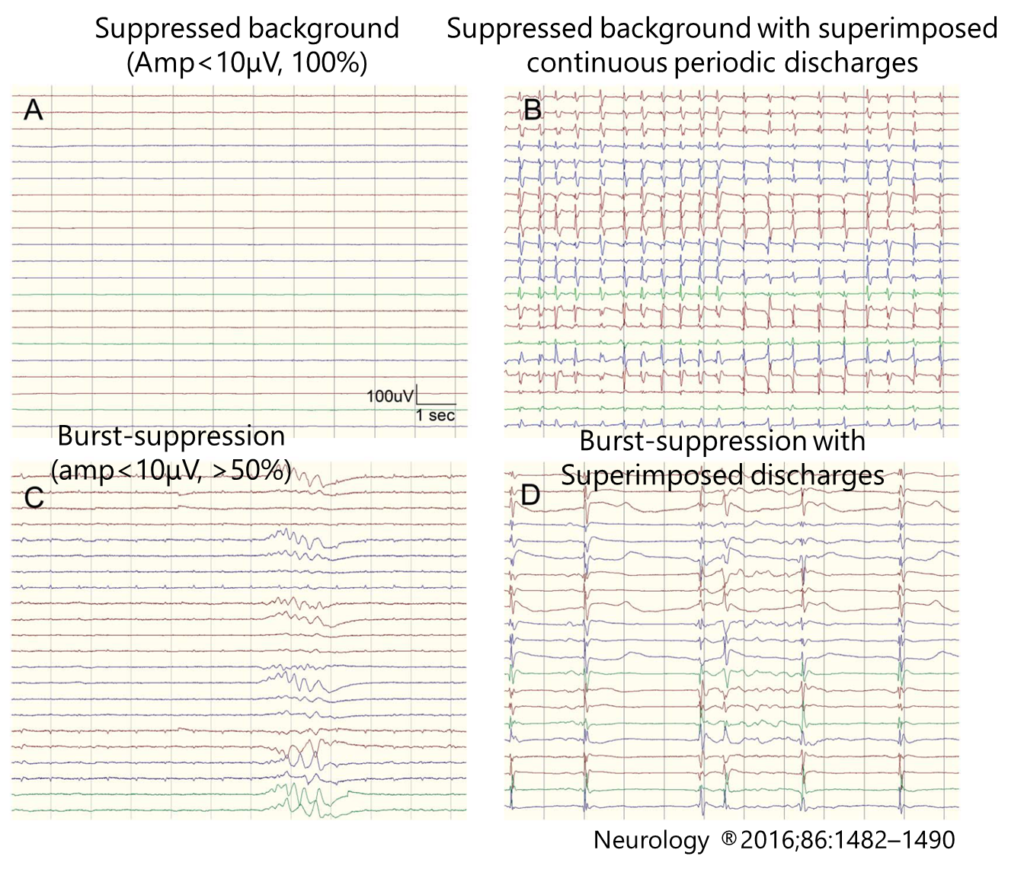
脳波
重要なポイント1:背景活動(background activity), 2:PDs(superimposed discharges), 3:反応性
*用語と定義を統一するためにANCSの用語を用いる
1:背景活動(background activity) *最重要
<分類>
・continuous
・discontinuous
・suppression burst 50-99% *burstの定義は文献により様々, ANCSの定義は”highly epileptiform bursts”で特別振幅などの制限はない
・suppression >99% *suppressed < 10μV
・心停止後脳波は通常suppressされるが、最終的に予後良好の患者では通常の脳波に最初の24時間でcontinuousへ戻ることが多い
・ただ通常心肺停止後は鎮静薬を使用している場合も多いため、それらの薬剤が背景活動に影響与える点に注意が必要
2:PDs periodic discharges
・GPDsは予後不良因子であるが、特異度は高くない
・PDs自体よりも「どのような背景活動にPDsがでているか?」の方が神経学的予後にとっては重要とされている
・また間欠的なてんかん性放電(epileptic discharges)は神経学的予後の良い指標ではない
3:反応性 reactivity
・外的な刺激を与えることで脳波の反応があるかどうか?を調べるものであるが、具体的な調べる方法の基準は存在せず、過去の研究でも様々である→このため現時点では神経学的予後にどのように使うべきかの推奨はない
上記を総合して脳波を”highly malignant”と”malingant”と分類することが多く, その元となった代表的な論文が以下 ”Standardized EEG interpretation accurately predicts prognosis after cardiac arrest” Neurology ®2016;86:1482–1490
脳波所見の分類
1:highly malignant EEG
・suppressed background without discharges
・suppressed background with continuous periodic discharges
・burst-suppression background with or without discharges
2:malignant EEG
・malignant periodic or rhythmic patterns (abundant periodic discharges; abundant rhythmic polyspike/spike/sharp and wave; unequivocal electrographic seizure)
・Malignant background (discontinuous background; low-voltage background; reversed anterior-posterior gradient)
・Unreactive EEG (absence of background reactivity or only stimulus-induced discharges)
3:benign EEG: malignantの所見なし
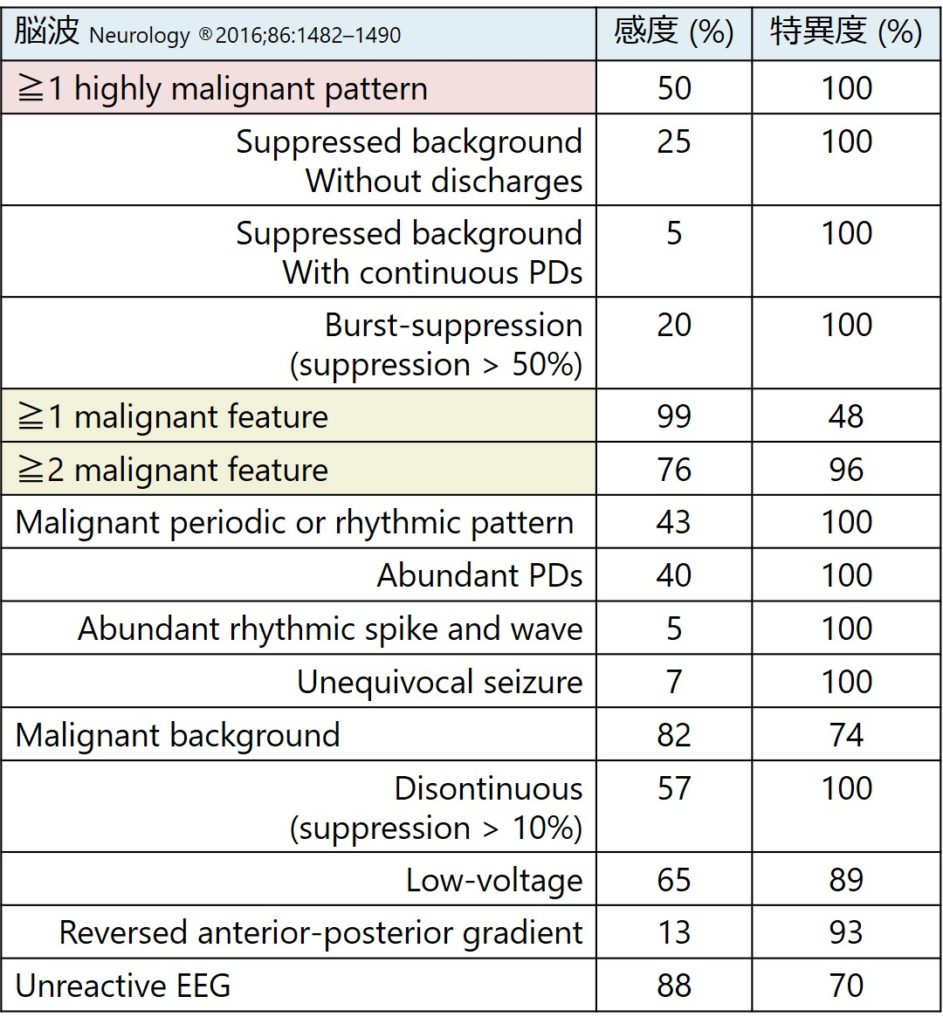
・患者:蘇生後脳症(TTM trial)
・予後不良判定:Cerebral Performance Category score 3-5/180日
*参考:CPC1:機能良好(就労可能), CPC2: 中等度障害(解除無しで日常生活可能), CPC3:高度障害(意識あり日常生活解除必要・かなり幅がある) ,CPC4: 昏睡, CPC5: 死亡
・脳波所見103例の患者背景:目撃あり96%, ROSC 30分, 脳波実施心肺停止から77時間後
・highly malignant EEG: 全体の37% Sn 50%, Sp 100%
・malignant EEG 全体の86%(highly malignant EEGを含む): 1つ該当: Sn 99%, Sp 48%, 2つ該当 Sn 76%, Sp 96%
・benign EEG 全体の14%: 93%予後良好(予後不良の1%, 予後良好の48%に認めた)
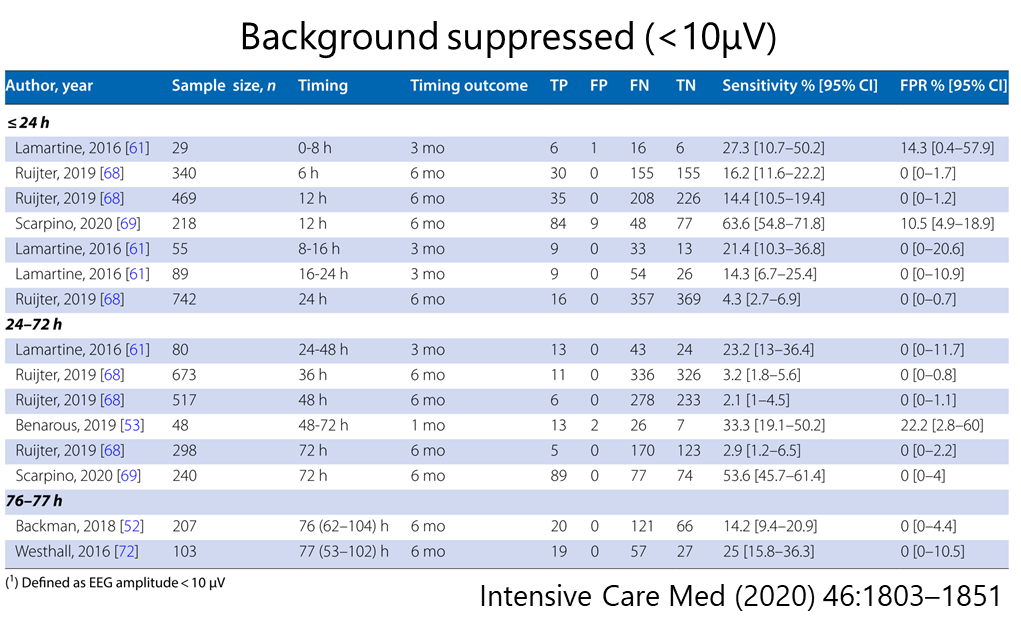
SSEP(somatsensory evoked potential)
・実際には実施することが難しい施設も多いと思います(私は先日初めて蘇生後脳症の患者さんにSEP実施しました)。
・方法:正中神経神経刺激、刺激部位と対側の体性感覚野での導出(電極:C-Fz)となります。解釈上最も問題となるのはアーチファクトであり、筋電図混入を防ぐため検査時に筋弛緩薬を使用するように推奨されています。
・基準:両側N20導出なしがガイドライン上の基準となっています。*プロポフォールやミダゾラムでは通常抑制されない(バルビツール系では抑制される可能性あり)
画像
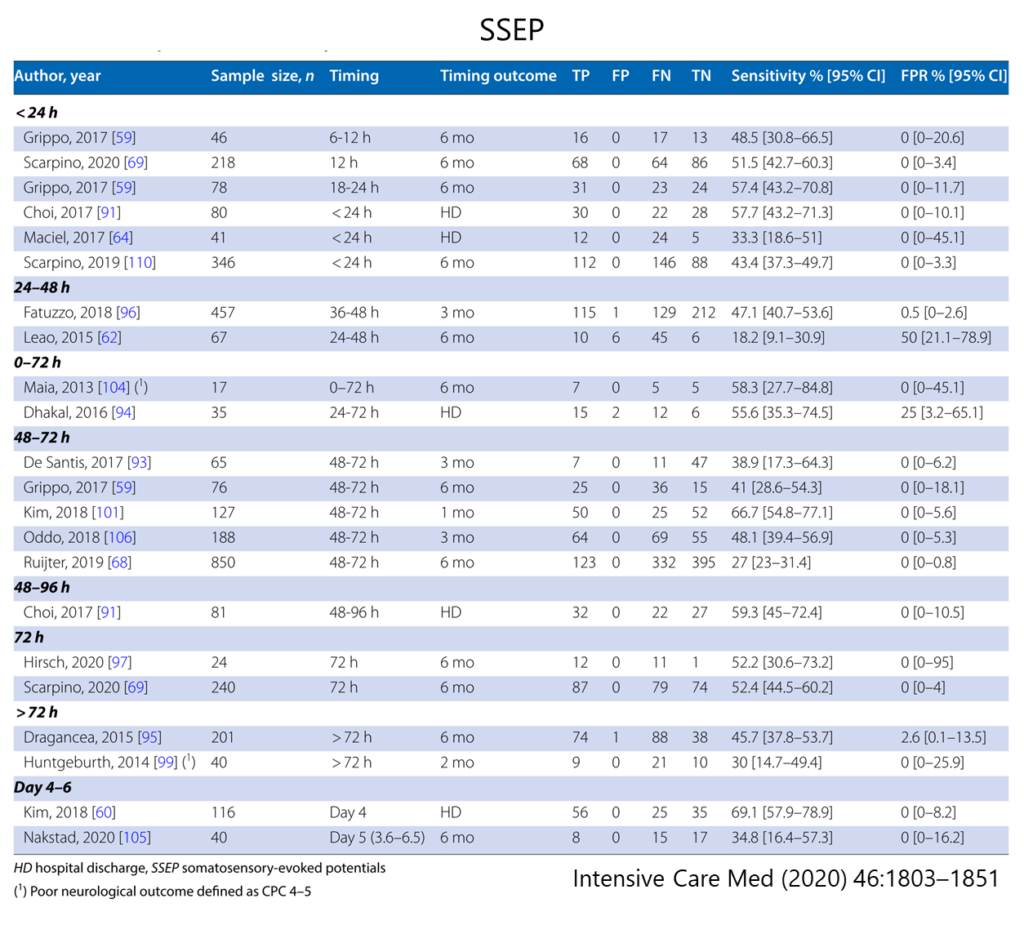
・基準:CT皮質髄質境界不明瞭 または MRI広範囲の拡散制限
・CT:灰白質(GM: gray matter)と白質(WM: white matter)の吸収値の比(GWR)が良く用いられる。正常ではGWRは1を超えるが値が低くなるほど脳浮腫を示唆する。場所は基底核>半卵円中心の高さなどが多いが、確立しておらず、GWRのthresholdも確立していない。
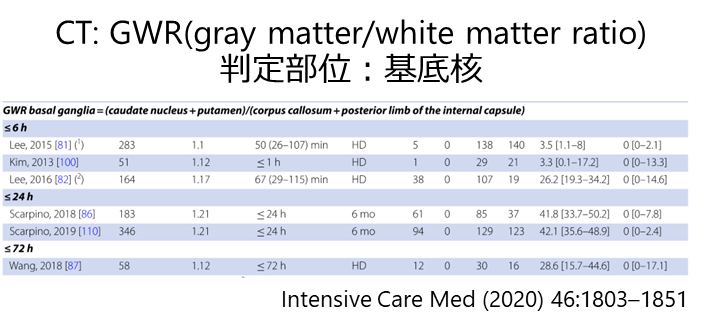
・MRI:拡散制限は細胞性浮腫を意味するため、予後推定に有用であるがこれも具体的な方法や閾値は確立していない。
・画像検査は鎮静薬などの影響を受けず客観的である利点があるが(神経所見や脳波と違い)、解釈の方法が確立していない点が欠点である。
バイオマーカー
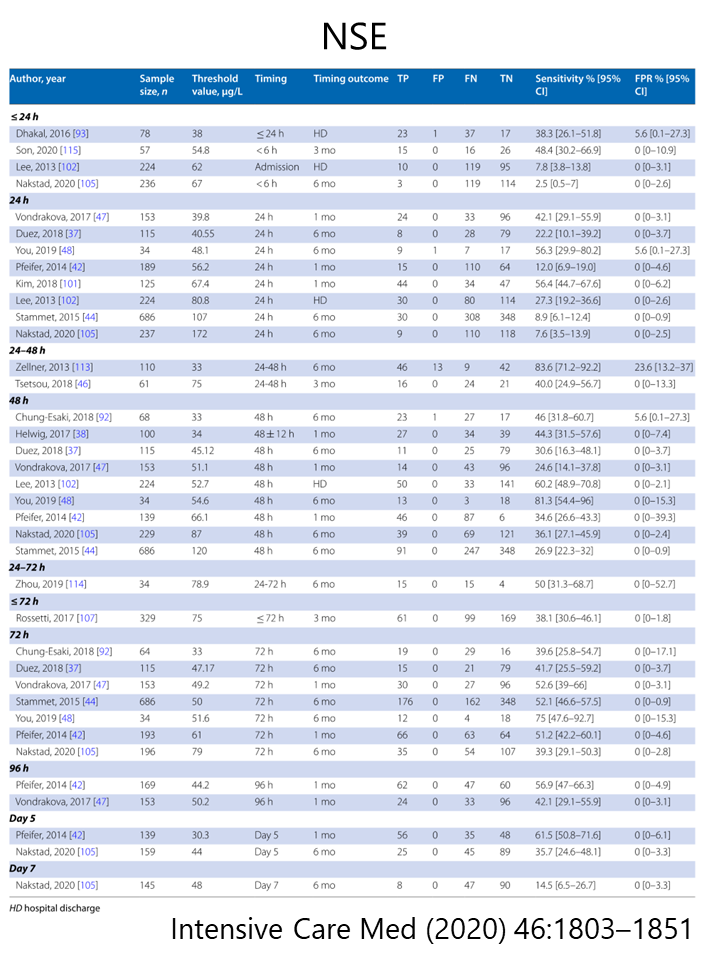
NSE(Neuron-specific enolase)
・神経細胞がダメージを受けたことを反映するbiomarkerとしてNSEは最も多く研究がされており、予後判定に有用とされています。利点としては鎮静薬の影響を受けず独立している点が画像検査と同様に挙げられます。
・ただ具体的に「どの時期に測定するべきか?」「閾値をどう設定するか?」という点は定まっていません。
・前者に関しては有用性が確立しているのは特にROSC後48~72時間です。
・後者に関しては赤血球がNSEを含んでいるため、溶血があると解釈が困難になります。またこういった連続値をとる検査で問題となるのが外れ値です。特異度を100%にする必要がなければ外れ値はそこまで大きな問題になりませんが、神経学的予後においては特異度100%を目指すため外れ値があるだけで閾値が大きく変化してしまうという問題を抱えています。このため特異度100%(偽陽性0%)を満たすのが極めて困難です。
神経所見
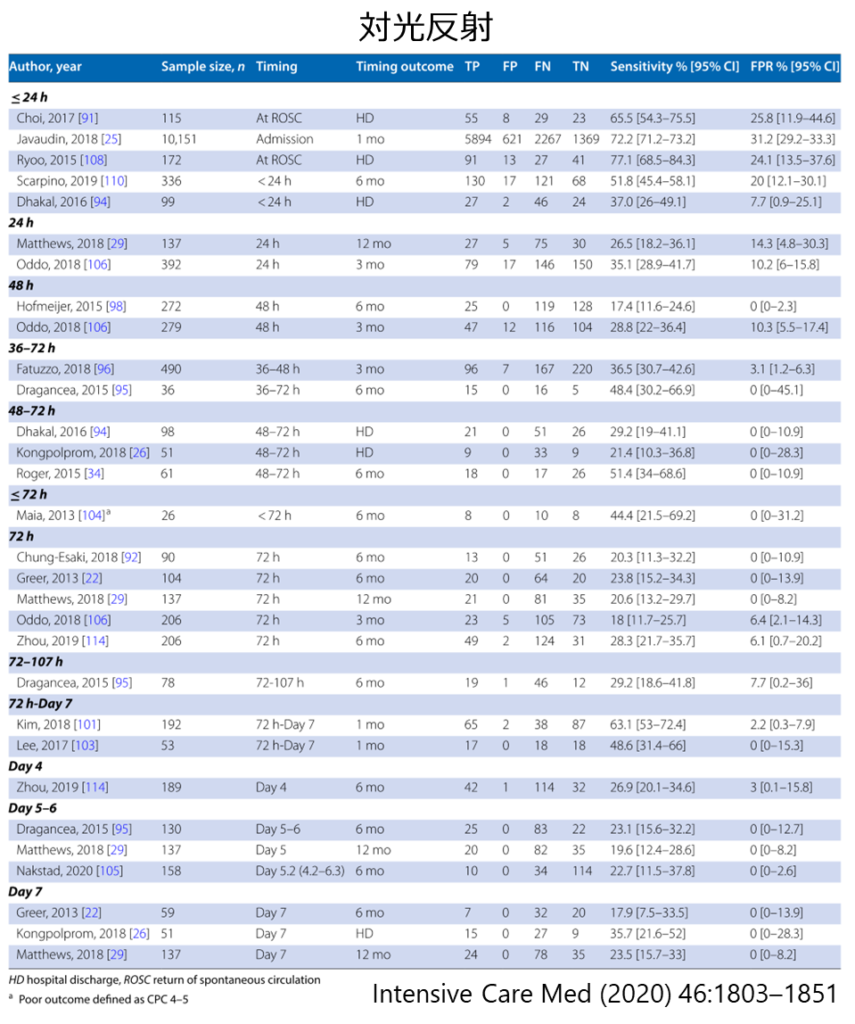
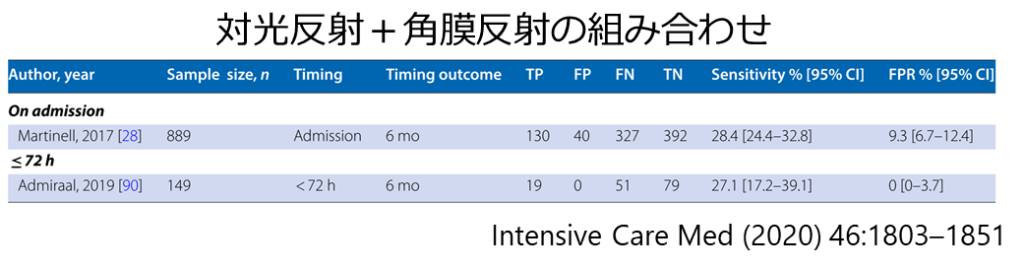
対光反射+角膜反射
・対光反射消失と角膜反射消失の「両者」を満たす必要があります
・対光反射の欠点としては1:瞳孔径が縮瞳している場合は判定が極めて難しい点と2:評価者によって判定が違う場合がある点(Neurocrit Care 2016;24:251)が挙げられます。
・自動瞳孔計は客観的に評価する上で有用なツールですが、実際にはない施設も多いと思います。
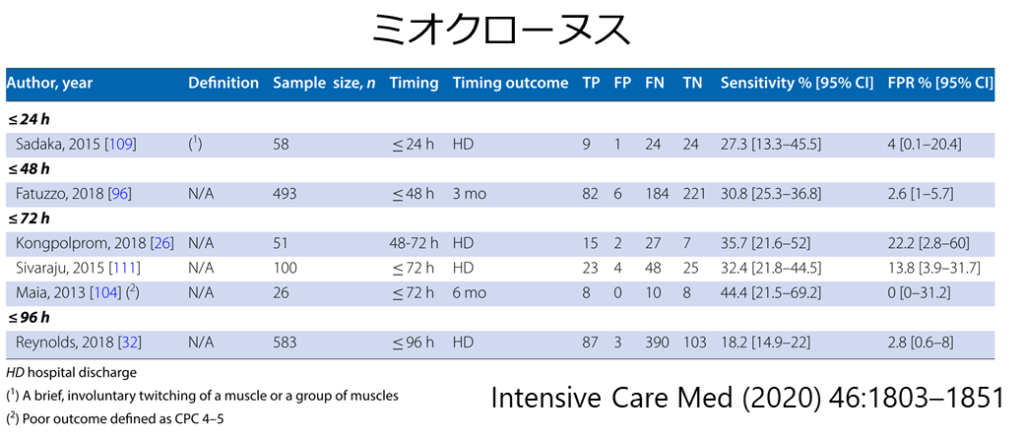
・対光反射消失はROSCの当初は予後判定として特異度は低いですが、時間経過とともに特異度が上昇していきROSC96時間では感度20-25%, 特異度100%と報告されています Intensive Care Med 2020; 46:1803–1851
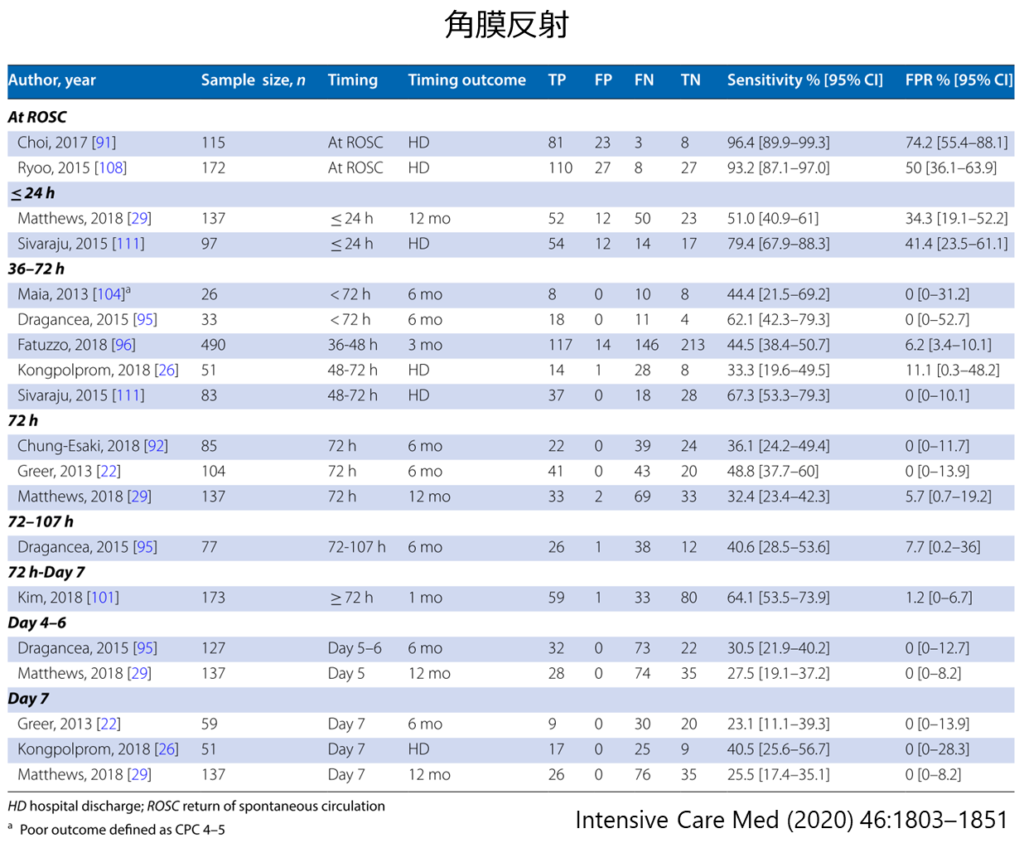
・角膜反射はROSC後72時間で感度25-40%, 特異度100%と報告されています
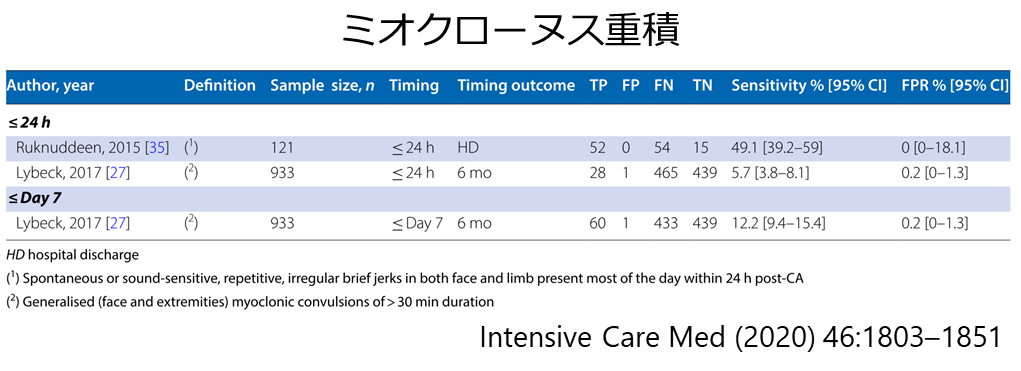
ミオクローヌス重積
・通常は30分以上持続する全般性のミオクローヌスをミオクローヌス重積(status myoclonus)と判定する(予後判定基準にも含まれている)
・多くの臨床研究ではミオクローヌスの具体的な持続時間や様式を定義していない点に注意(下図)
*Lance-Adams症候群:意識改善後もミオクローヌスを伴う
そもそも神経学的予後不良とは何か?
・一般的に心停止後の神経学的予後はCPC(Cerebral Performance Categories)によって評価する場合が多いです。これは1~5の5段階評価で以下の通りです。
CPC1:機能良好(就労可能), CPC2: 中等度障害(解除無しで日常生活可能), CPC3:高度障害(意識あり日常生活解除必要・かなり幅がある) ,CPC4: 昏睡, CPC5: 死亡
・しかし、CPCが「いくつか?」によって予後不良を決めるconsensusはありません。2006年までは臨床試験でCPC4-5が”poor” neurological outcomeとされていましたが、それ以降はCPC3も”poor” neurological outcomeに含むようになっています。
・これらはあくまでも臨床試験を組む上での客観的指標であり、患者さんご家族にICする場合にはきちんとこの背景を理解しておく必要があります。つまりただ「予後不良です」といっても患者さんご家族が知りたい内容は「どの程度まで改善する可能性が少しでもあるのか?」という点になるので、「神経学的予後不良」という言葉はかなり幅が広いものであり具体的に何を意味しているのか?を意識する必要があります。
参考文献
・Intensive Care Med (2020) 46:1803–1851 予後不良因子に関してのsystematic review


