病態
TOAST分類には記載がされていませんが(病変が15mm以上で「小血管病」(ラクナ梗塞)に該当しないと「分類不能」になります)、元々1989年にCaplanが提唱した概念(Neurology. 1989 Sep;39(9):1246-50.)でとても重要です。障害される血管はラクナ梗塞と同様に「穿通枝」ですが、穿通枝の入口部に「アテローム性病変(microatheroma)」をつくり閉塞することで穿通枝領域全体が障害されることが病態で、主幹動脈に狭窄がないにも関わらず症状が進行性で治療抵抗性であることが臨床的な特徴です。日常臨床では頻回に遭遇するものです。病態のイメージは下図です。
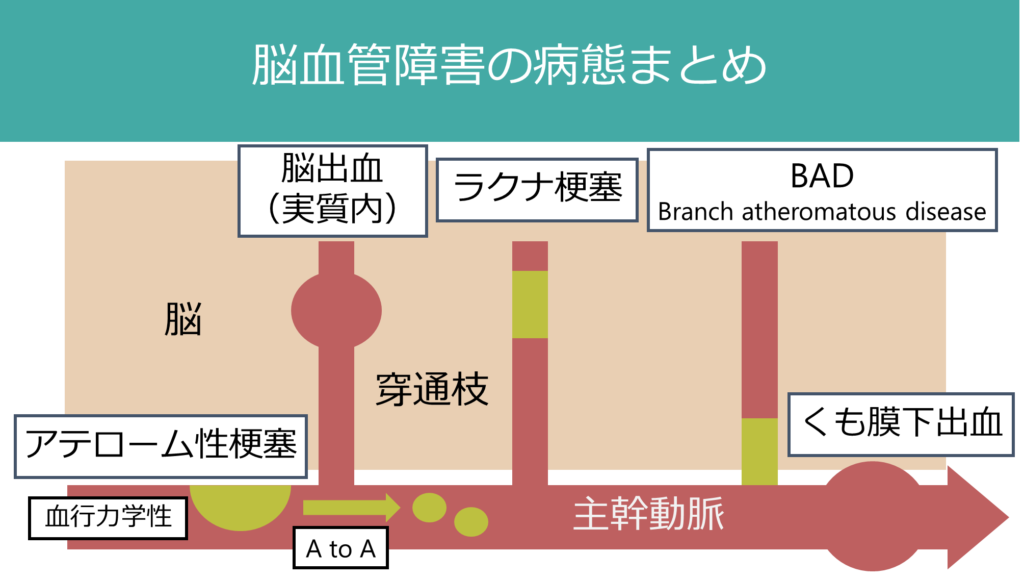
責任血管:レンズ核線条体動脈(LSA: lenticulostriate artery*別名:外側線条体動脈) or 傍正中橋動脈(PPA: parapontine artery)領域が原因として最多(下図参照) *外側線条体動脈はレンズ核線条体動脈(lenticulo-striate artery)とも表現されます
*その他の責任血管:視床膝状体動脈、前脈絡叢動脈、Heubner反回動脈、視床穿通枝動脈
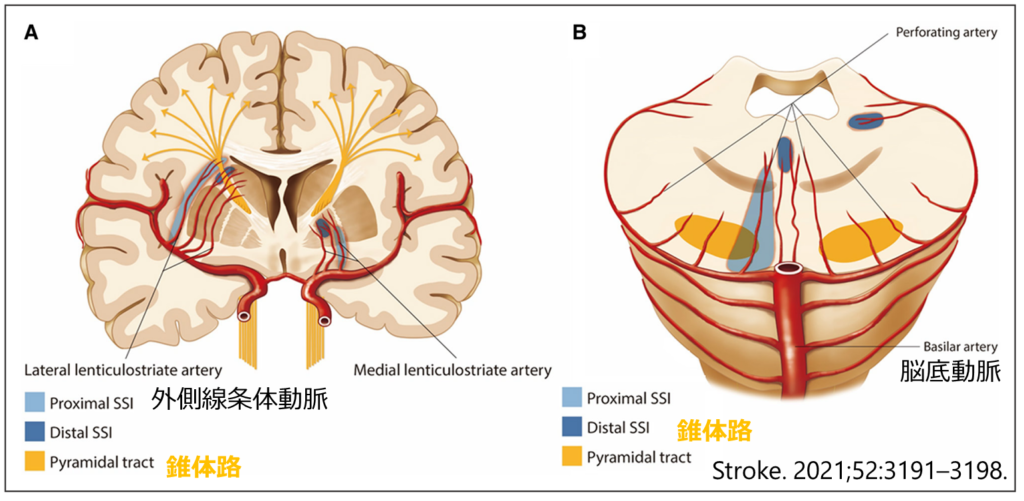
*これらの好発血管は主幹動脈に対して垂直に枝を出しているので、血流の流れが「がくっ」と変わる部位で物理的に圧負荷のかかりやすい血管であるため、アテローム性変化をきたしやすいことが機序として考察されます。
レンズ核線条体動脈(LSA: lenticulostriate artery*別名:外側線条体動脈 lateral striate artery)について
・線条体動脈を分類すると内側線条体動脈(MSA), 外側線条体動脈(LSA)という名称が用いられ、内側から起始するものは前方へ、外側から起始するものは後方へ分布する
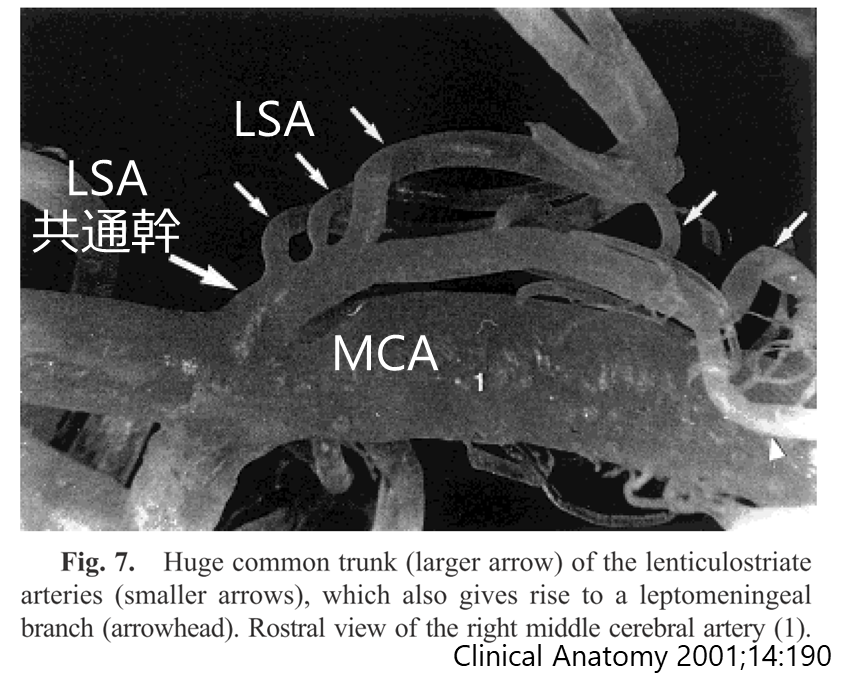
・レンズ核線条体動脈はMCAから分岐し、剖検例での検討ではLSAは2~12本(平均7.1本)、径は80-1400μmとされる(参考:Clinical Anatomy 2001;14:190)
・下図の様に共通幹を有する場合もある(同部位が梗塞に至ると広い範囲の虚血になる)
・血流支配:外側群→被殻・淡蒼球外側・尾状核・内包膝~前脚・内包後脚の上部・放線冠
画像所見・診断
これらの穿通枝は通常の1.5, 3TのMRAでは描出することが出来ないため, 梗塞巣からこれらの血管の根本が障害されたと推定するアプローチをとります。
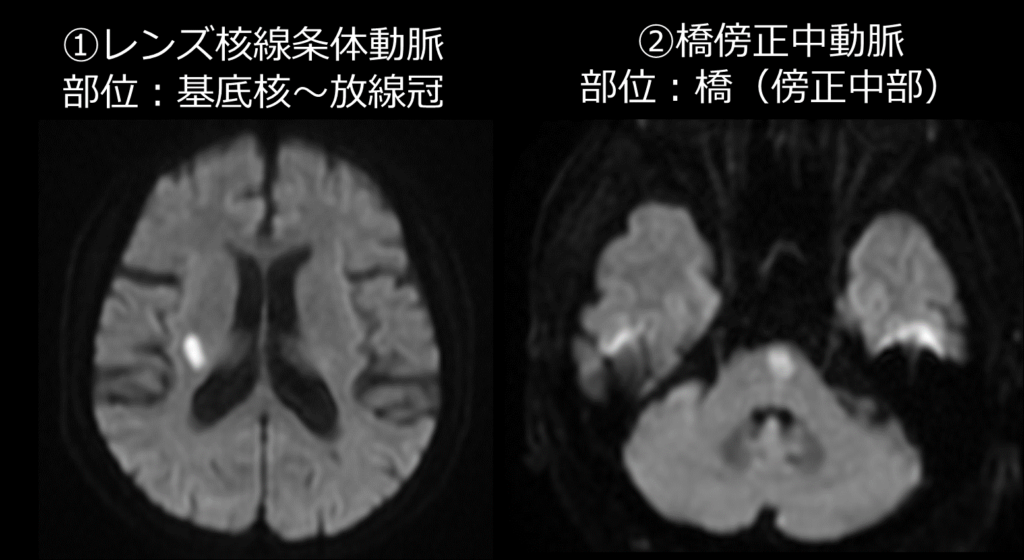
・LSA領域の場合:水平断3スライス以上
・PPA領域の場合:橋底面に達するような梗塞
・主幹動脈50%以上狭窄の病変を伴わない
上記の基準はどの文献もこちら(Annual Review 神経 2006 “Branch atheromatous disease” 中外医学社; 2006 p119-128)を引用されています。特にLSAに関してはMRIのDWI coronal画像を撮像するとより正確な評価がしやすくなります(LSAの走行に沿った病変分布を確認することができる)。
治療
私の知る限り現時点でBADの病型に絞った前向き臨床試験は存在せず、「BADはこの治療法」といった確立した治療戦略はないと思います。病態のところで説明した通り、障害される血管は「穿通枝」ですが、病態は「アテローム」なのでアテローム血栓性に準じた対応を行うことが実臨床では多いです。
ここはかなり病院によって治療方針が違うところで、アルガトロバンを併用する施設など様々です。私も色々な施設で経験していますが、確かにアルガトロバンを最初の2日間持続投与しますが、その後間欠投与に変えるタイミングで症状が悪化する例も経験があります。
rt-PAは有効なのか?
これもBADでのrt-PAに関してまとまった報告はまだないかもしれません。実臨床ではrt-PAはほぼ無効であり、むしろrt-PAの基準を満たすために血圧を下げると余計に悪化して矛盾した結果になってしまうケースなどもよく経験すると思います(おそらくここは脳卒中に関与する医師全てが同意するのではないかと思います)。
また今後調べた内容をupしていきたいと思います。
参考文献
・臨床神経 2014;54:289-297
・臨床神経 2020;00:000


