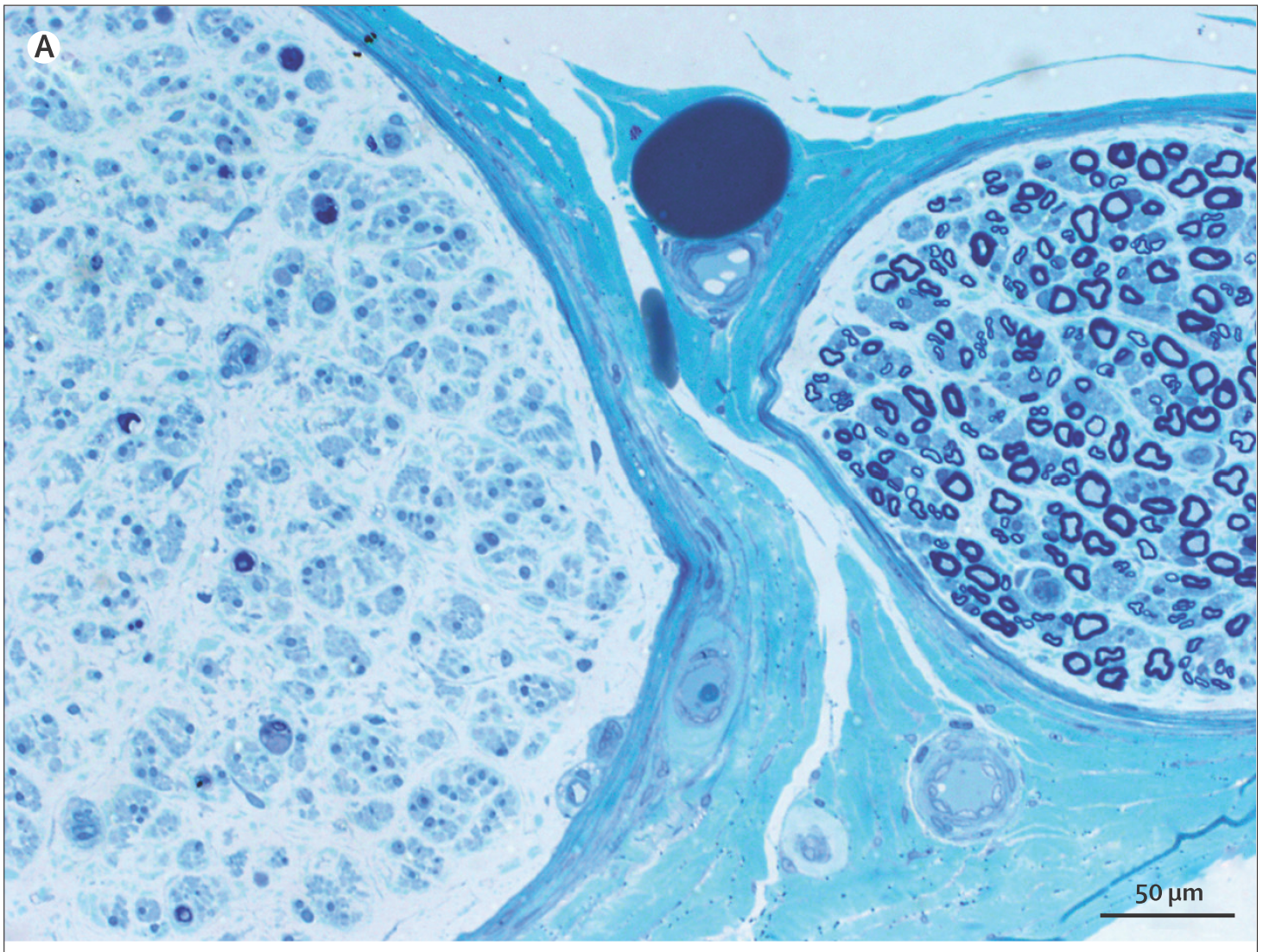
病態
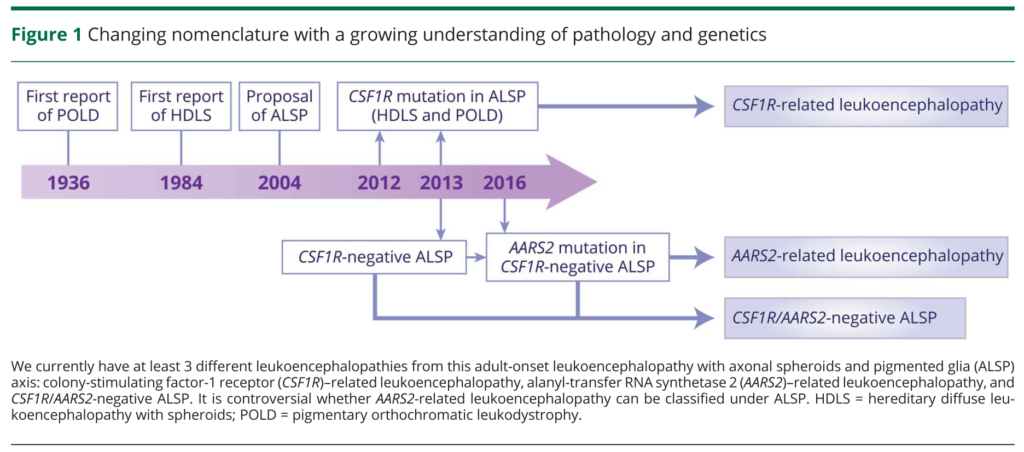
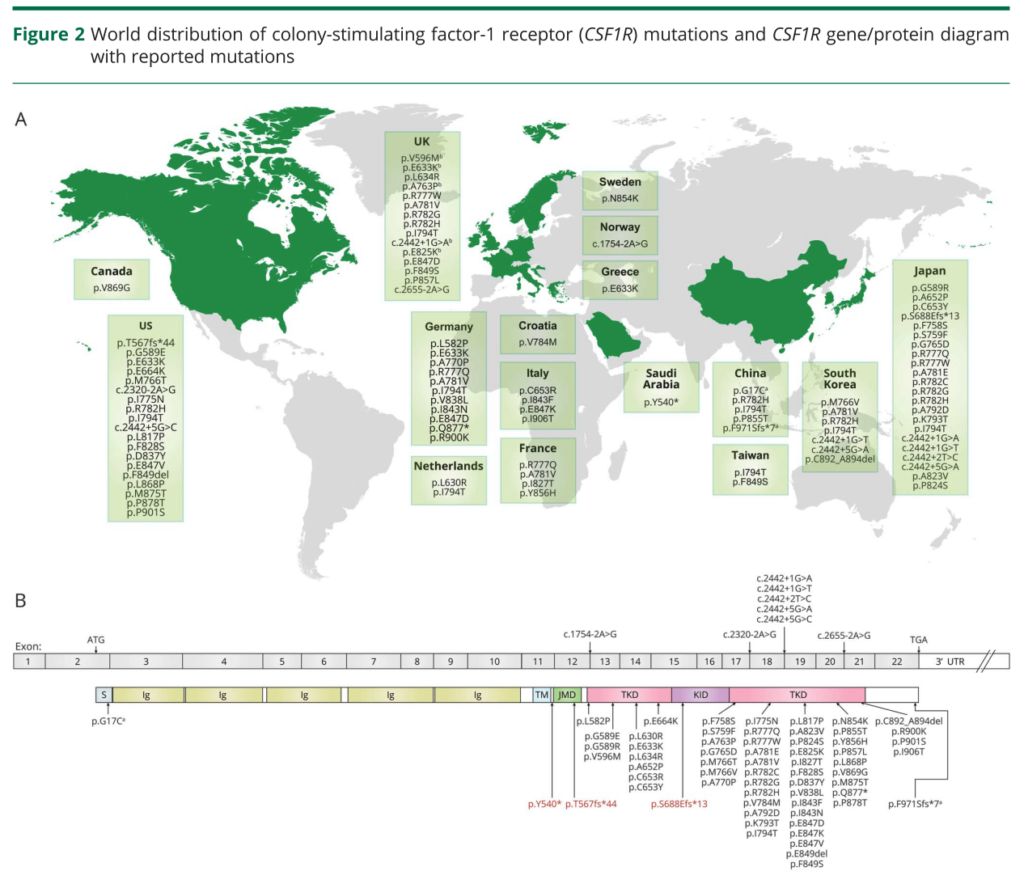
・神経軸索スフェロイド形成を伴う遺伝性びまん性白質脳症(hereditary diffuse leukoencephalopathy with spheroid:HDLS)は遺伝性(常染色体優性遺伝)の白質脳症を呈し、成人発症の若年性認知症の原因として重要です。ミクログリアの機能異常が病態で、ALSP(Adult onset leukoencephalopathy with neuroaxonal spheroids and pigmented glia)とも表現されます。1984年に初めて報告されてから、2012年に遺伝子診断(colony stimulating factor-1 receptor(CSF-1R))が可能となり(Nat Genet 2012;44:200-205.)、その名称も複雑になっています(下図参照)。家族歴がない症例の報告もあることから家族歴がないだけでは本疾患は否定できません。
臨床像
・30-40歳前後で発症し(一般的に女性の方が男性よりも若年で発症するとされています)、進行性の認知機能障害、人格変化、行動異常、抑うつ症状、パーキンソニズム、錐体路徴候などを呈し、数年以内に死亡してしまうことがあります。臨床像はかなりheterogeneousな様ですが、大きくまとめると前頭側頭葉変性症の病像に運動症状として錐体外路症状もしくは錐体路徴候が加わるようなイメージです。
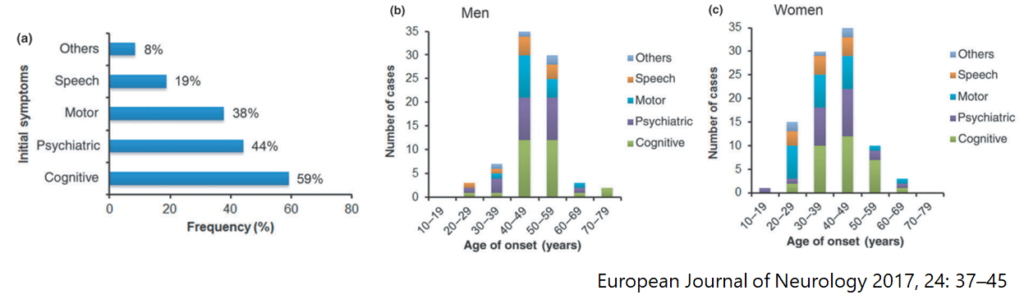
■122例ALSP(90家系)の臨床像まとめ European Journal of Neurology 2017, 24: 37–45
・122例(男性52例、女性66例、報告されていない4例)、90家系をまとめた包括的な報告です。
・発症年齢は43±11歳(18-78歳)、女性の方が有意に若年で発症しています(女性40歳 vs 男性47歳)。罹病期間は6.8年、死亡は53±12歳とされています。
・初発症状は認知機能障害59%、精神症状44%、運動症状38%、言語症状19%、その他8%に認めています(下図)。経過全体では認知機能障害96%、精神症状81%、錐体路徴候81%、前頭葉機能障害77%、パーキンソニズム65%、構音障害54%、嚥下障害50%を認めています。
・画像所見はこの後紹介しますが、側脳室拡大100%、両側性白質病変96%、皮質萎縮92%、脳梁菲薄化88%、脳梁異常信号88%、錐体路異常信号58%、DWI異常信号38%、Gd造影増強効果0%、CTでの石灰化54%とされています。
画像所見
特徴的な画像所見は以下の通りで、「脳萎縮」+「白質脳症」+「脳梁菲薄化」+「錐体路信号変化」+「微小石灰化病変」が鑑別に有用な所見です。
・脳室周囲の白質病変(前頭・頭頂葉優位)両側性だがかならずしも左右対称性ではない、U-fiberは通常spareされる
・内包・大脳脚などの異常信号 *小脳脚や小脳歯状核はspareされる
・側脳室の開大(年齢に比して)
・脳梁菲薄化・信号異常
・進行期の脳溝開大と皮質萎縮
・頭部CT検査での微小石灰化病変(1mm厚のthin sliceで撮影することが望ましい):側脳室前角周囲の白質や頭頂葉皮質下白質
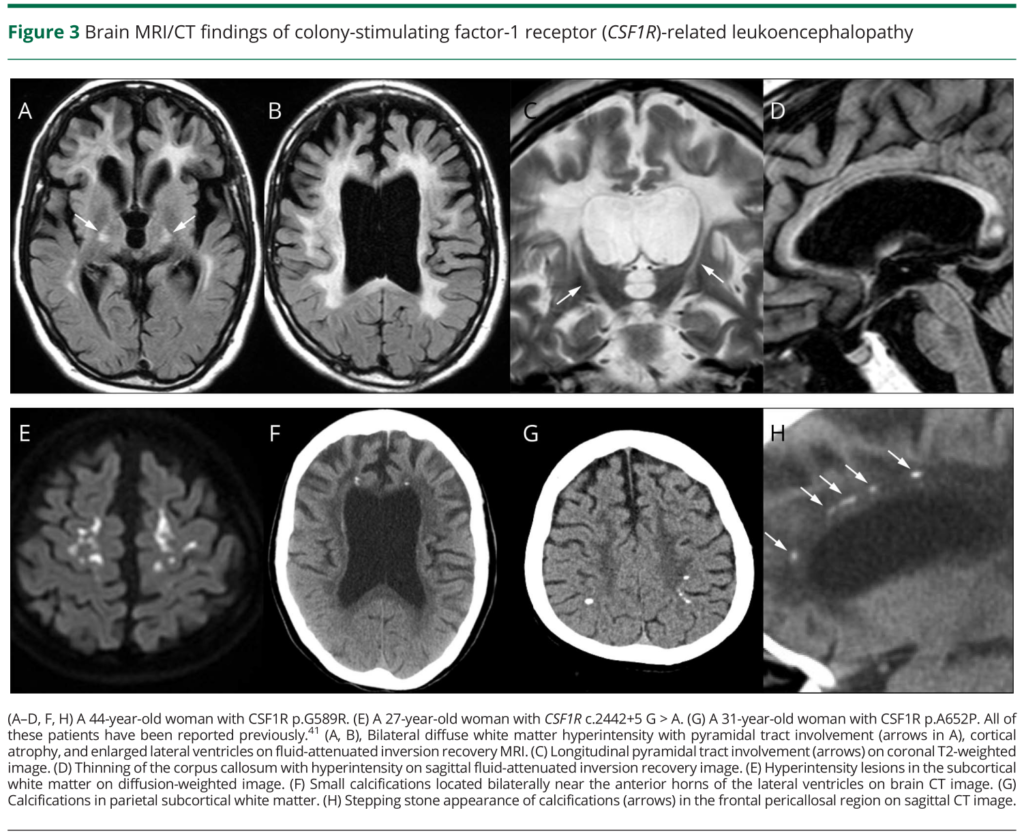
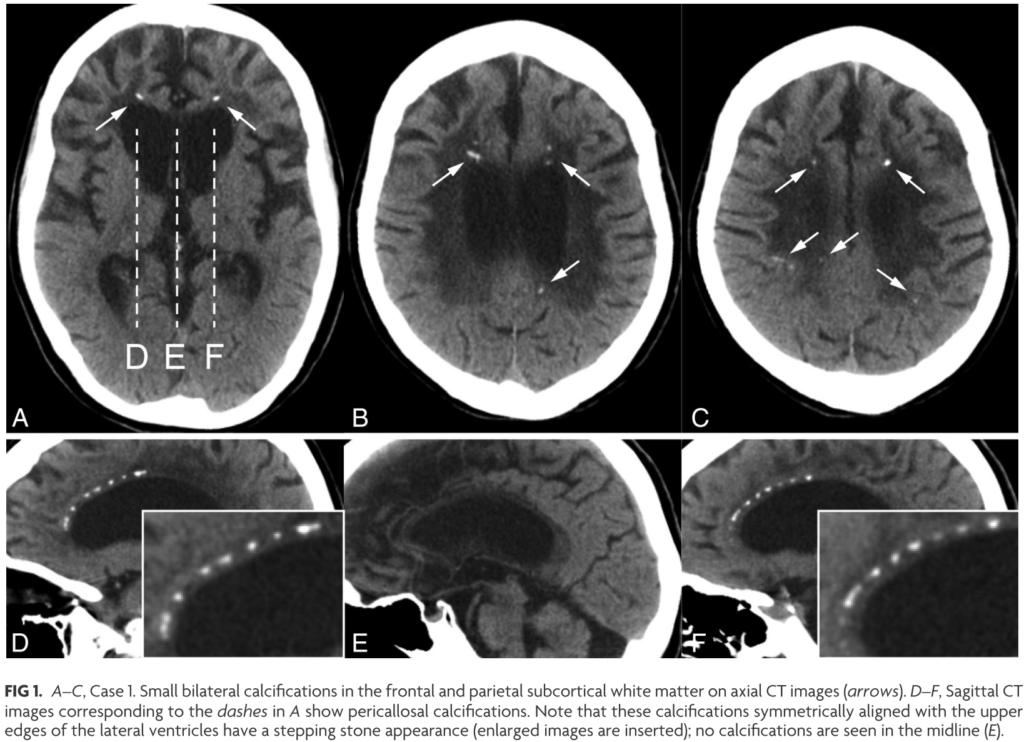
■石灰化病変
HDLSの診断に特異的な所見として重要なのが石灰化病変の指摘です。頭部単純CT検査をthin sliceで3方向で撮影することが重要です(通常のslice厚では石灰化を見逃してしまう可能性があるため)。石灰化は通常左右対称性で側脳室前角周囲に認める場合が多く、また下図矢状断の様に脳梁周囲前部に“stepping stone appearance”を認めることが特徴的とされています(American Journal of Neuroradiology January 2017, 38 (1) 77-83)。
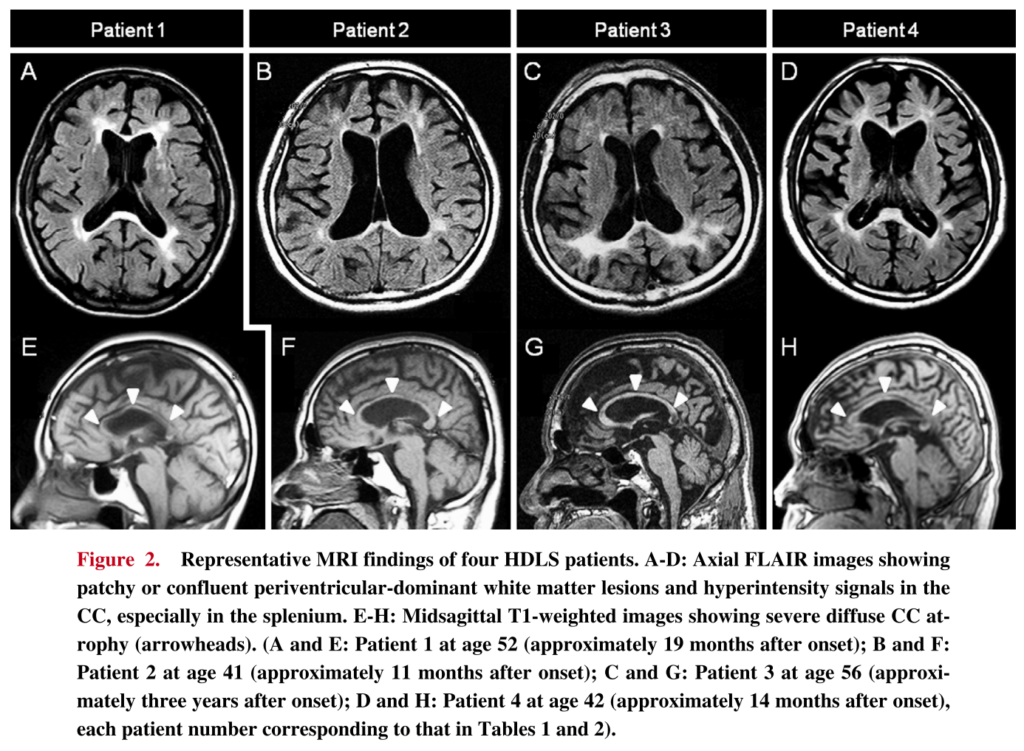
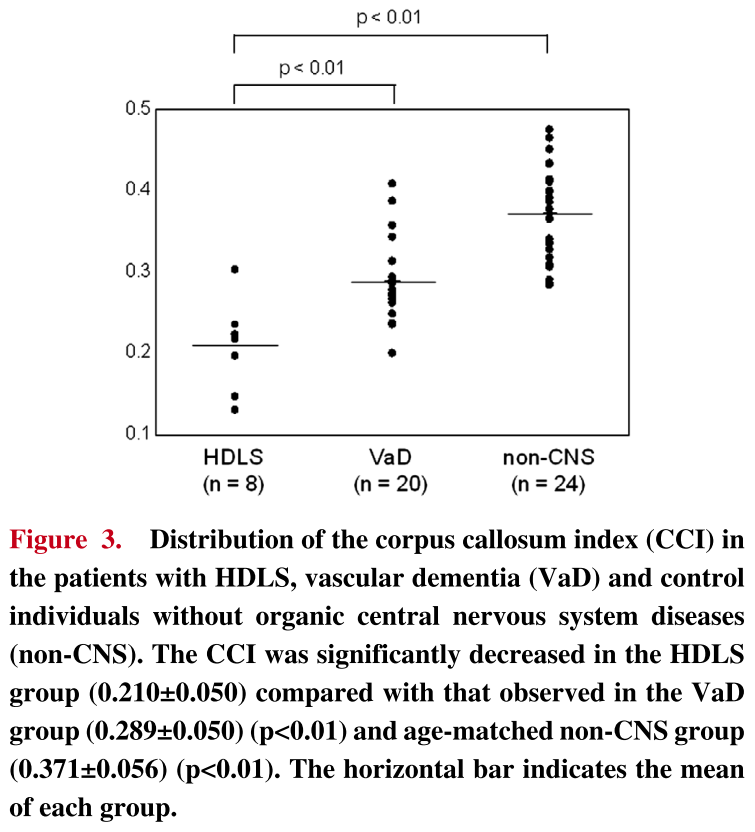
■HDLSの脳梁萎縮評価(HDLS6例) Intern Med 53: 21-27, 2014
この文献では脳梁萎縮を評価するためにCCI(corpus callosum index)という指標を導入しており、HDLSではVaD(20例)やコントロール(24例)と比較して有意に脳梁萎縮を認めたと報告しています(HDLS6例全例で脳梁萎縮と信号変化を認めている)。
■DWI高信号病変
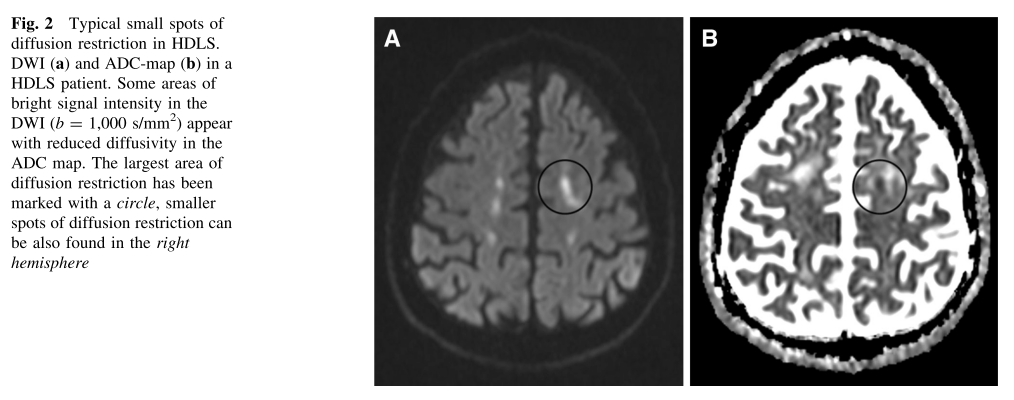
DWI:白質変化の内部に一部高信号(ADCmap低下を伴う)を認める場合があります(J Neurol (2014) 261:2351–2359)。これらは脳血管障害と異なり数ヶ月高信号が持続することがあり、髄鞘内の浮腫を反映しているとされています。(造影増強は通常認めません)
*錐体路の繊維に沿った線状高信号を呈することもあり特徴的です。
Verga腔や透明中隔腔をよく随伴するという報告もあります。
*参考:皮質脊髄路・中心前回にT2WI高信号を呈する成人疾患(「神経内科疾患の画像診断」より)
1:変性疾患 筋萎縮性側索硬化症、遺伝性痙性対麻痺
2:代謝性疾患 脳腱黄色腫症、低血糖、肝性脳症、成人型Krabbe病、Wilson病、副腎白質ジストロフィー、Kearns-Sayre症候群、神経核内封入体病、HDLS、LMNB1関連常染色体優性白質ジストロフィー
3:中毒性疾患 トルエン中毒、ヘロイン・コカイン中毒
4:感染・炎症・脱髄性 HAM、急性散在性脳脊髄炎、多発性硬化症、ベーチェット病、視神経脊髄炎
5:腫瘍 悪性リンパ腫、神経膠腫
診断
診断基準 「遺伝性脳小血管病およびその類縁疾患の診断基準の確立と治療法の研究班」より
主要項目
1.60 歳以下の発症
2.下記のうち二つ以上の臨床症状
a.認知機能障害,または性格変化・行動異常
b.錐体路徴候
c.パーキンソン症状
d.けいれん発作
3.常染色体優性遺伝形式もしくは孤発例
4.頭部 CT/MRI で下記の所見を認める
a.両側性の大脳白質病変
b.脳梁の菲薄化
5.血管性認知症,多発性硬化症,白質ジストロフィー(ALD,MLD 等)など他疾患を除外できる
除外項目
1.10 歳未満の発症
2.2 回以上の stroke-like episodes(脳血管障害様エピソード)。ただし,けいれん発作は除く
3.高度な末梢神経障害の合併
支持項目
1.臨床徴候や Frontal Assessment Battery(FAB)検査等で前頭葉障害を示唆する所見を認める
2.進行が速く,発症後 5 年以内に臥床状態となることが多い
3.頭部 CT で大脳白質に点状の石灰化病変を認める
判定
【definite】主要項目 2,3,4a を満たし,CSF-1R 変異または HDLS に特徴的な神経病理学的所見を認める
【probable】主要項目 5 項目全てを満たすが,CSF-1R 変異の検索および神経病理学的検索が行われていない
【possible】主要項目 2a,3,4a を満たすが,CSF-1R 変異の検索および神経病理学的検索が行われていない
*遺伝子検査は信州大学さん、新潟大学さんに依頼させていただいております。
治療
根本的な治療法は存在しない。
参考文献
・Neurology ® 2018;91:1092-1104. 新潟大学の今野卓哉先生が”CSF1R -related leukoencephalopathy”としてまとめられたreviewで大変分かりやすいです。
・Eur J Neurol. 2017 Jan;24(1):37-45.