私は今まで同脳炎の患者さんを2例主治医として診させていただいた経験がありますが、毎回非常に悩み、印象に深く刻まれる経験をさせていただきました。Dalmau先生によって2007年に同脳炎12例の報告されてから(Ann Neurol 2007;61:25)、その特徴的な臨床像もあいまって現在は認知度がかなり上がっている脳炎です。Dalmau先生が発表された当初は「卵巣奇形腫に合併する脳炎」という認識でしたが、腫瘍非合併例も多く報告されるようになり純粋な傍腫瘍症候群にとどまりません。自己免疫性脳炎の中で頻度は最も多く、ある程度閾値を低く考える脳炎なのかなと思います(自己免疫性脳炎総論に関してはこちらをご参照ください)。
病態
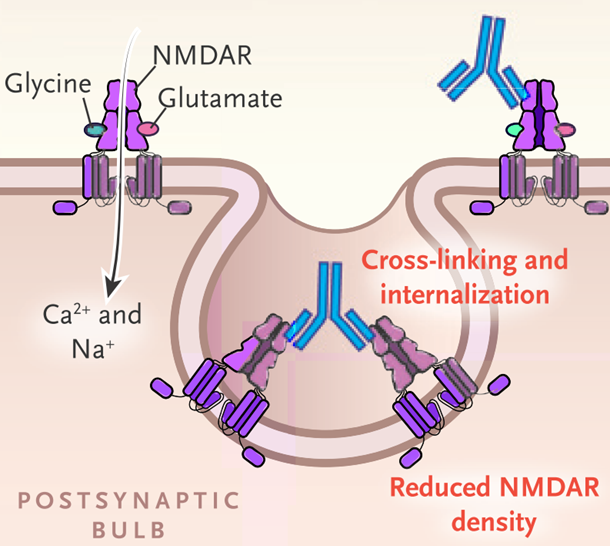
グルタミン酸受容体は大きく3種類あり、1:NMDA受容体、2:AMPA受容体、3:カイニン酸受容体の3つに分類され、そのうちのNMDA受容体が関係します。抗NMDA受容体脳炎では、抗NMDA受容体抗体により、受容体は細胞内に取り込まれ、細胞外に発現する受容体が減少する(internalizatoin and cross-linking)ことが関係しているとされています。
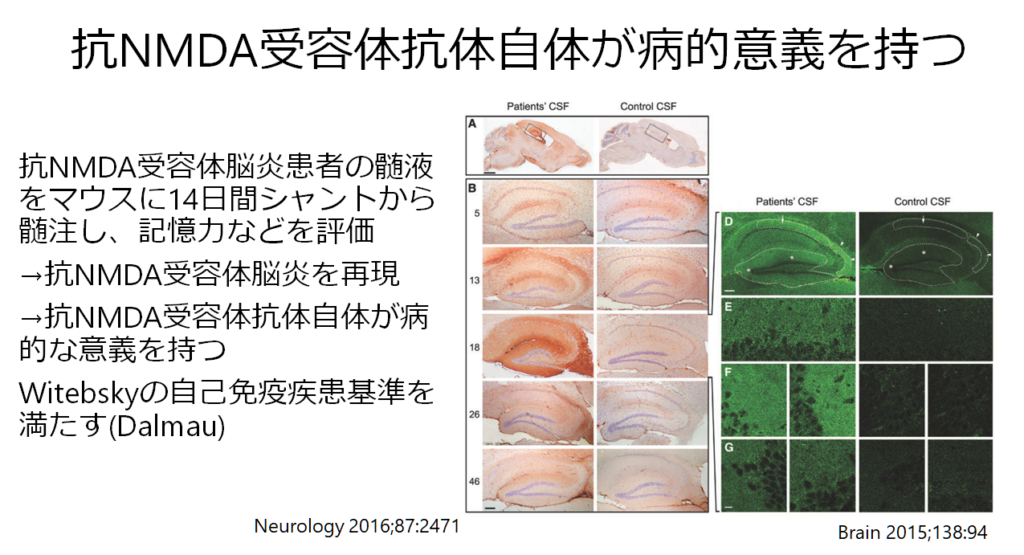
自己免疫疾患の抗体はそれが本当に主病態なのか(病的意義を持つのか)?もしくはたまたま同時に検出されているby-standerなのか?の判断が重要ですが、以下のマウスの実験で抗NMDA受容体抗体はpassive transferが証明されており主病態であることが知られています。
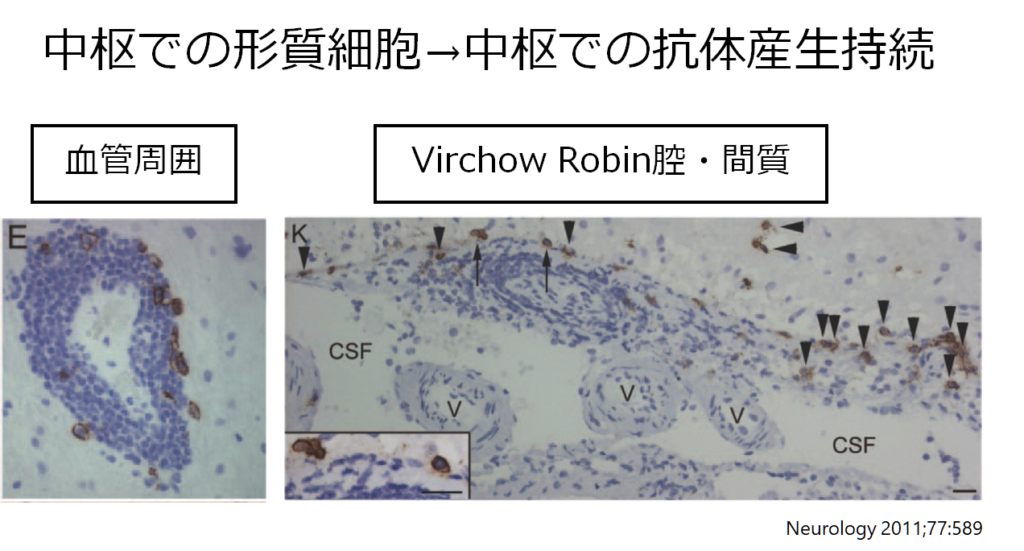
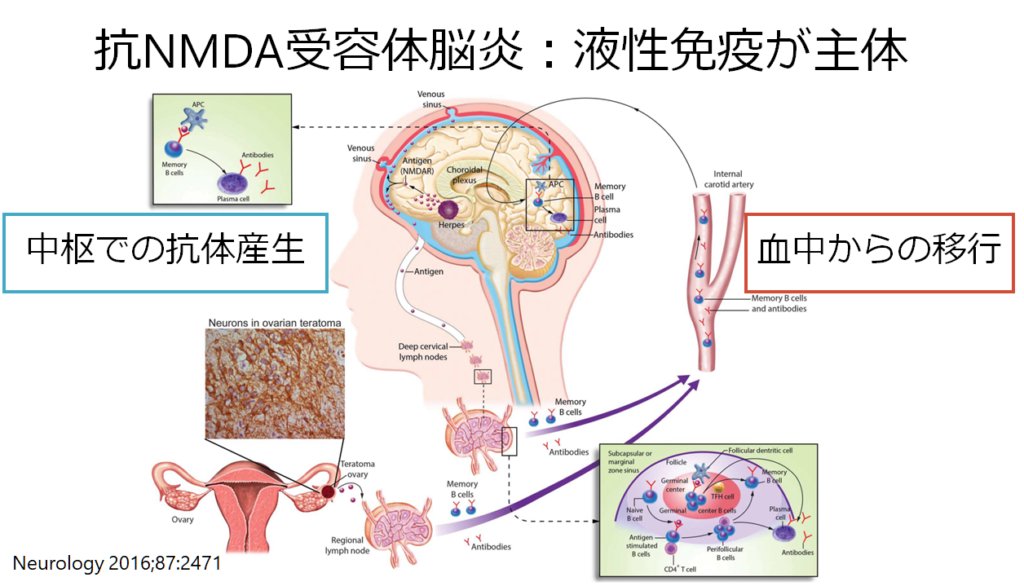
ではこの抗体はどこで産生されいるかどういうことですが、抗NMDA受容体脳炎では中枢神経で抗体産生が行われている点が病態の特徴です。中枢にてlong-lived B cellが持続的に抗体産生するため、免疫抑制治療薬の効果乏しいこととの関連が問題です。
抗NMDA受容体脳炎は初めは血液-リンパ系で抗原提示がされて抗体産生が行われますが、途中から中枢での抗体産生に移行します。以下のBrainの論文ではこれが臨床像と相関するのではないかとしています。つまり、はじめの発熱、頭痛といった前駆症状の期間は血中-リンパ系での抗体産生が起こり、中枢での抗体産生に移行すると痙攣、意識障害、不随意運動などを呈するのではないかという仮説です。
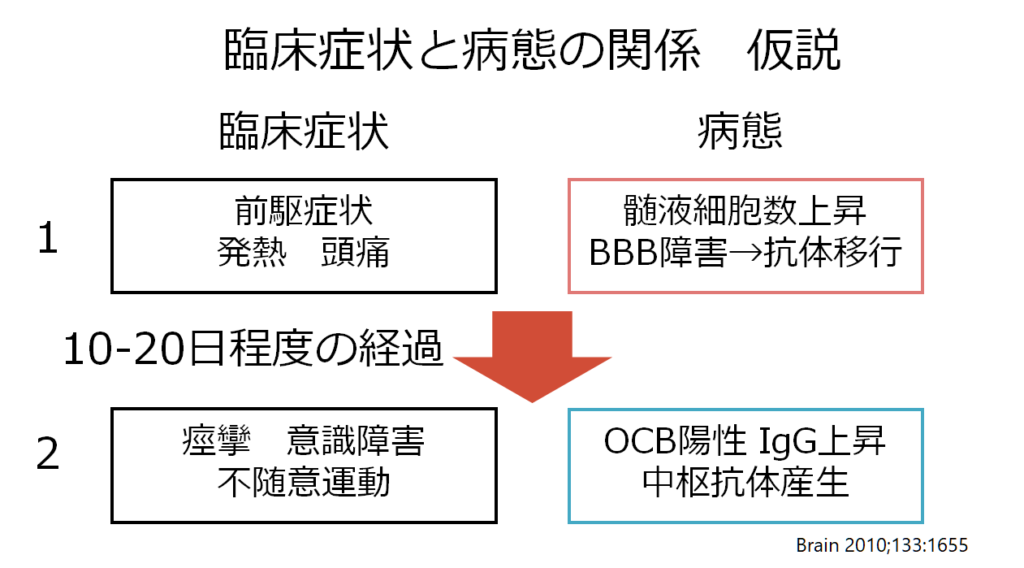
このことからわかる様に診断においては髄液中の抗NMDA受容体抗体の測定が重要で、CBA(cell-based assay)での測定が望まれます(ELISAではなく)。Dalmauの報告では全例髄液陽性(血清陽性、髄液陰性は基本的に偽陽性と判断する)です。また髄液中の抗体価と臨床経過は相関することが知られています(下図)。
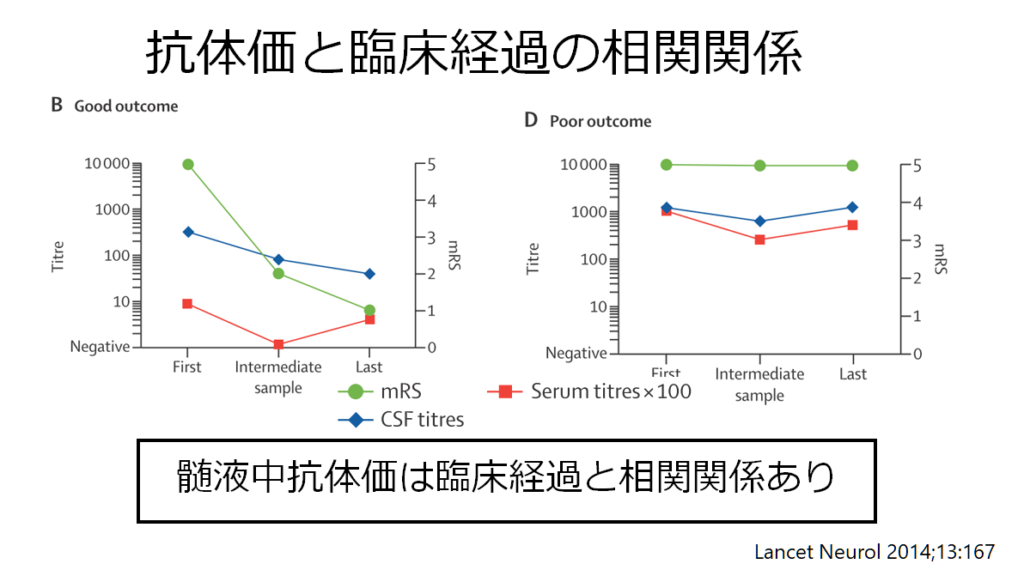
しかし、臨床的には改善しても抗体産生が15年も持続している症例報告もあり(JAMA Neurology 2013;70:117 下図は経過)、臨床的な文脈の中で抗体価を解釈する必要があります(抗体を治療しているのではなく、患者さんを治療している)。
臨床経過でどのように改善していくか?も抗NMDA受容体抗体の抗体価が関係しているとされ、症状が出現する順番と逆の経過をだどることがあるとされています。つまり、coma→自律神経障害安定→呼吸改善→不随意運動改善→M6入るように→言語機能改善→精神症状出現→落ち着いてくる→社会性や遂行機能の改善という順番になります。その後長期間のリハビリテーションが必要となる場合が多いです。
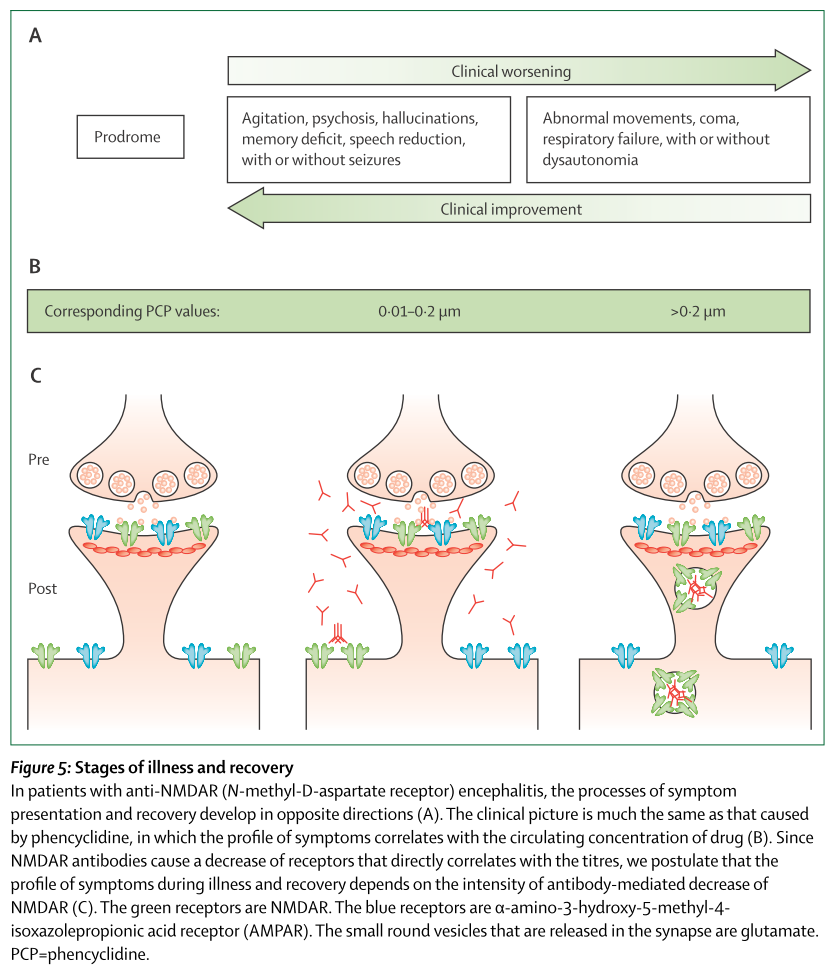
臨床症状
抗NMDA受容体脳炎は特徴的な臨床経過をとることが知られていいます。
1:前駆症状 発熱、倦怠感などの非特異的な症状
2:精神症状:統合失調症症状が進行性
3:痙攣→意識障害
4:中枢性低換気
5:不随意運動
6:回復期:数か月~数年かけて改善する
前駆症状は70%程度に認め頭痛、発熱、嘔気、嘔吐、下痢、上気道症状などを数日で認めます(通常は2週間以内)。精神症状は不安、不眠、恐怖、幻覚、mania paranoia、短期記憶障害、言語障害などがあり、統合失調症の急性期を思わせる場合もあります。不随意運動は“oro-lingual-facial dyskinesias”が最も特徴的です。一度診ると忘れませんが、Vincent先生は不随意運動の臨床像だけで抗NMDA受容体抗体関連脳炎の診断は困難であるとしています。自律神経障害:高体温、頻脈、涎、高血圧、徐脈など(タコつぼ型心筋症の報告もあり)。(下図は後輩N先生のスライドから引用)
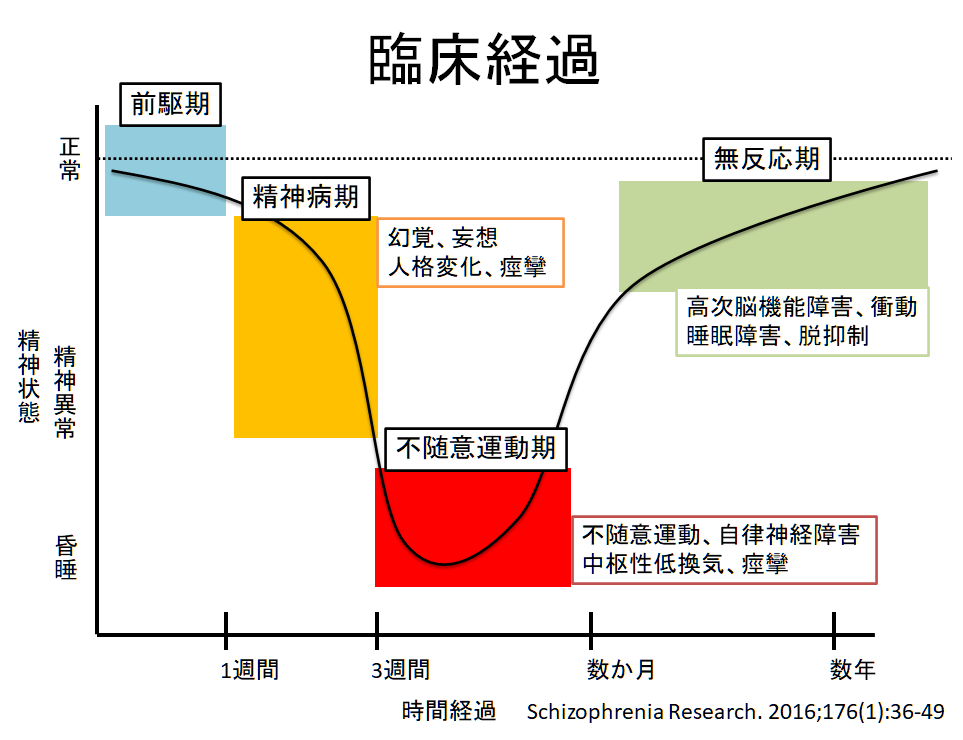
完全にこの経過通りにならないこともありますが、個人的な経験では非常に的を得ていると思います。以下にCEP(california encephalitis project)で集められたウイルス性脳炎と抗NMDA受容体脳炎の臨床像の比較を掲載します(Eur J Clin Microbiol Infect Dis 2009;28:1421)。臨床像としてはやはり精神症状が目立ち、髄液所見はウイルス性と比べると細胞数増多などが目立たない傾向があります。
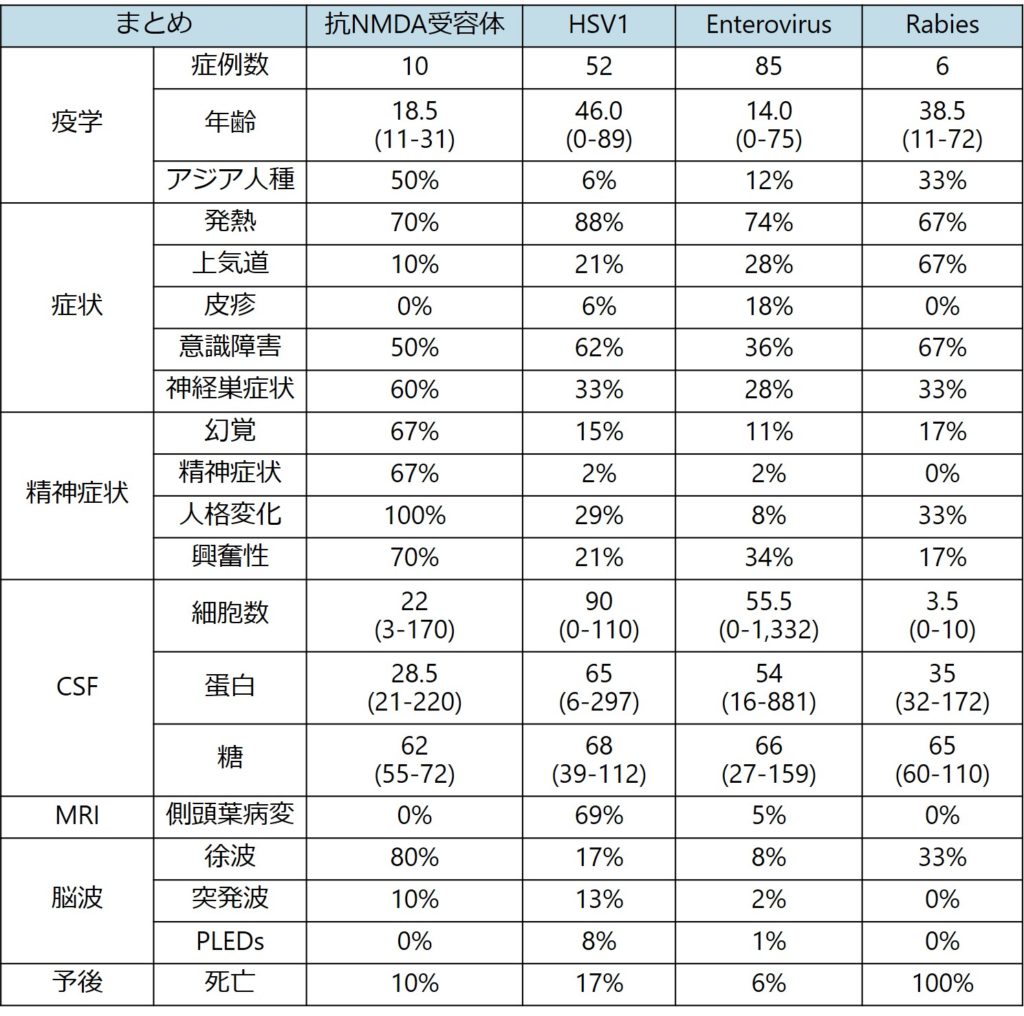
検査
■髄液検査
これは自己免疫性脳炎全ての特徴ですが、髄液検査正常だからといって同疾患を否定することはできません。以下に発症1週間以内の急性期の髄液所見をまとめたものを掲載します。IgG indexの自己免疫性脳炎での重要性は別記で述べたのでこちらをご参照ください。
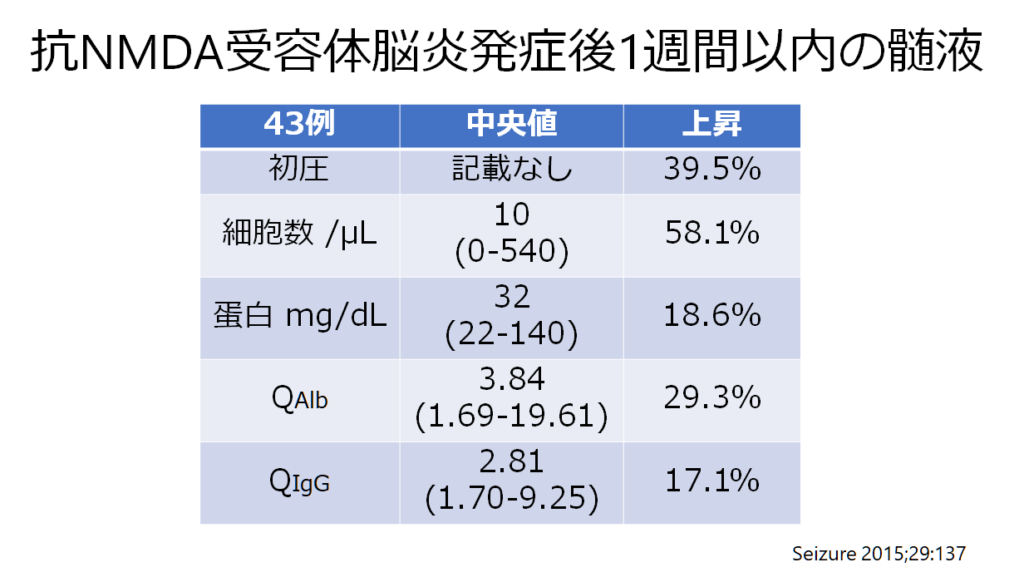
■脳波
抗NMDA受容体脳炎に特異的かもしれないといわれている脳波所見が”Extreme delta brush”という所見です。これはdelta activityの上に20-30Hzのβ波が合体している”riding on each wave”状態を表します。報告では抗NMDA受容体脳炎の30%に認めたとされ、特徴的な所見とされています(Neurology 2012;79:1094)。
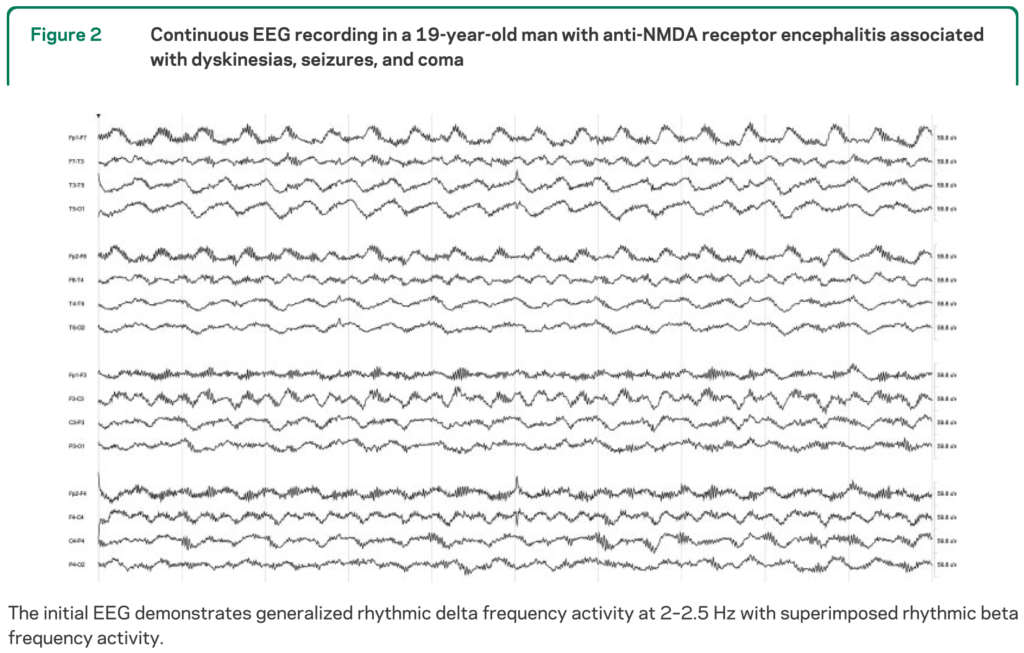
■画像検査
抗NMDA受容体脳炎53例のMRI所見をまとめた報告では、頭部MRI検査所見を下記の通り4つのtypeに分類しています。
・type 1:正常 53%
・type 2:海馬病変 13%
・type 3:海馬以外の病変 13%
・type 4:海馬+海馬以外の病変 21%
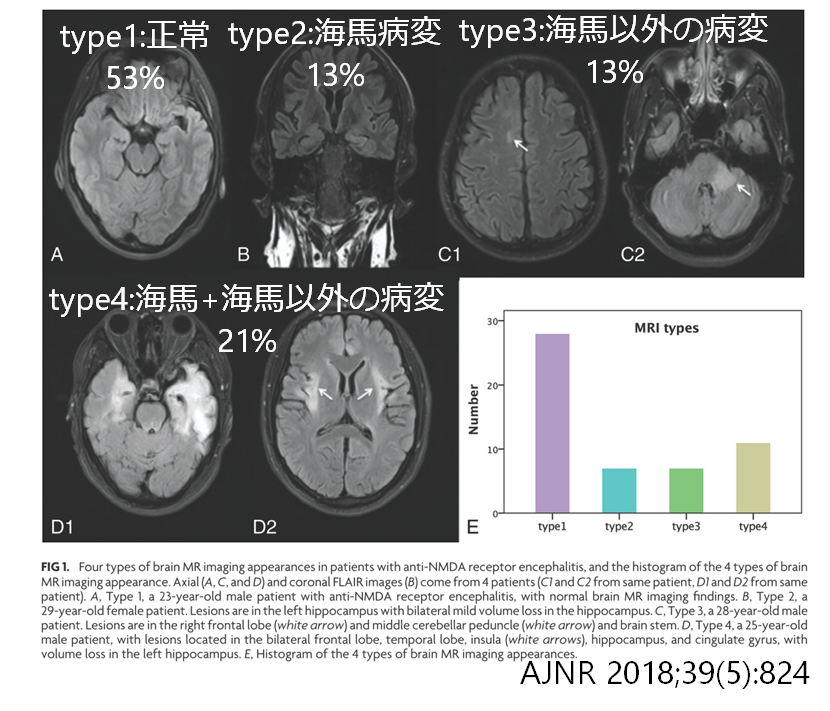
自己免疫性脳炎の中では頭部MRI検査が正常のものが多い印象です。また抗NMDA受容体脳炎に特異的な頭部MRI所見はないともいえます。
経過での頭部MRI所見に関しては、飯塚先生がご報告された治療により萎縮が可逆性であるというインパクトのある報告があります(JAMA Neurol 2016;73:706)。
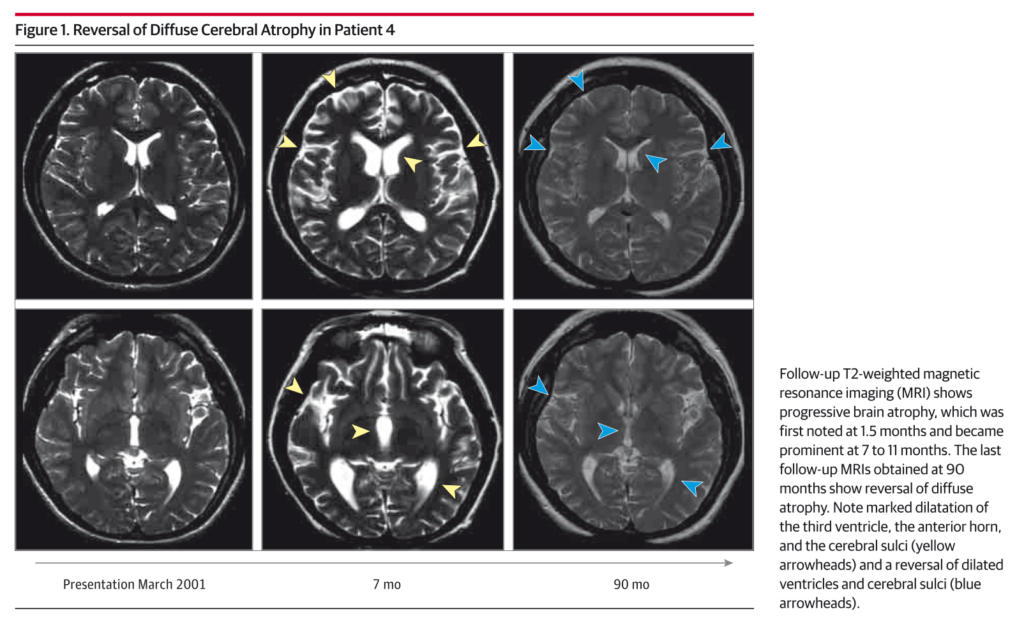
診断
以下を満たすことがdefiniteの診断基準とされています(Lancet neurol.2016;15(4):391-404)。
1.3ヶ月以内に出現する症状(下記のうち少なくとも1項目)
・異常行動(精神症状) / 認知機能障害
・言語障害
・痙攣
・運動障害、ジスキネジア、筋固縮、異常姿勢
・意識障害
・自律神経障害 / 中枢性低換気
2. IgG型 抗GluN1抗体 陽性
3.その他の疾患の除外
抗体を測定しないことには診断出来ないので、まずはある程度閾値を低く疑うことから始めるべきではないかと思います。
腫瘍合併
女性は卵巣腫瘍、男性は精巣胚細胞腫瘍に関して特に検索が必要です。卵巣腫瘍に関しては初期work upで検出されなくても2年間はフォローアップするべきとされています(実際に脳炎から遅れて腫瘍が見つかる報告があります Brain and development 2017;39:448)。このあたりはその他の傍腫瘍症候群と同様かと思います。以下にまとめを掲載します。
400例の腫瘍合併まとめ
女性(335例):49%(165人) 卵巣奇形腫以外:7例(2%)のみ 乳癌2例、NET2例、膵嚢腫1例
男性(65例):5%(3人) 精巣germinoma2例、SCLC1例
人種ごとの腫瘍合併頻度:Asian 43%, Caucasian 30%, African American 49%, Hispanic 32%, others 40%
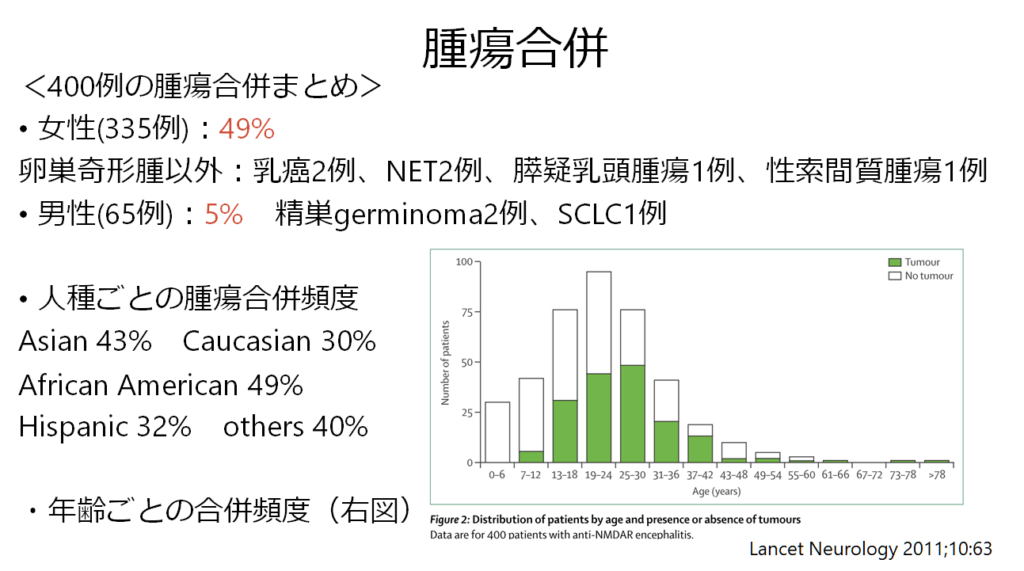
また腫瘍非合併例の方が腫瘍合併例と比べて予後不良で、再発率も高いとされています。
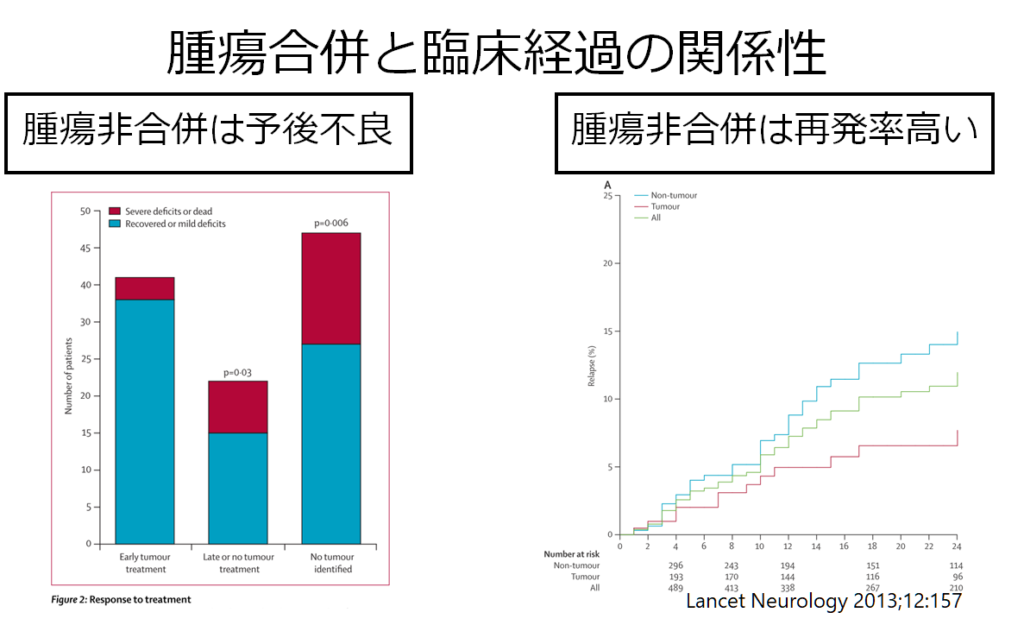
治療
自己免疫性脳炎のところでのまとめと同様ですが再掲させていただきます。
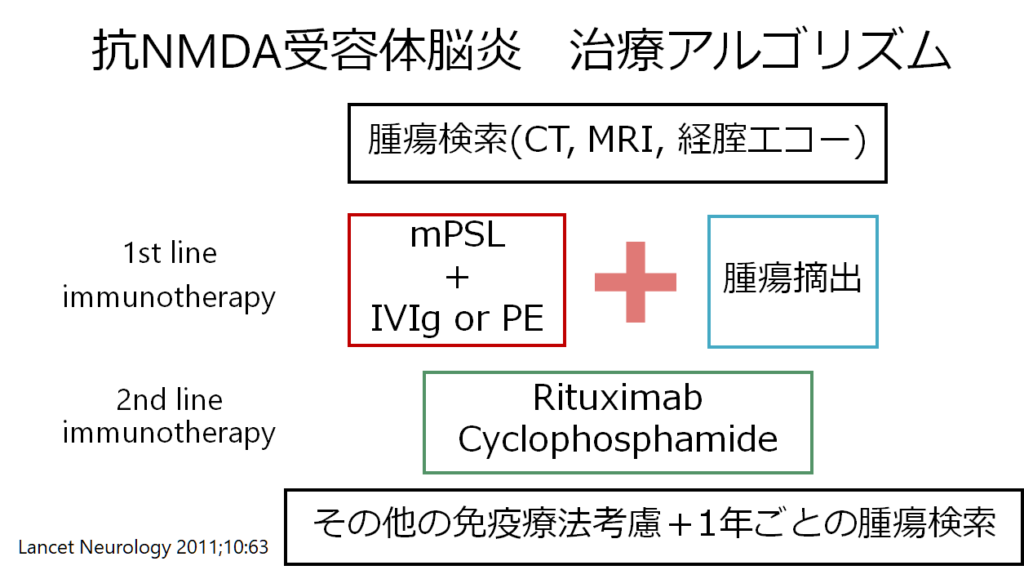
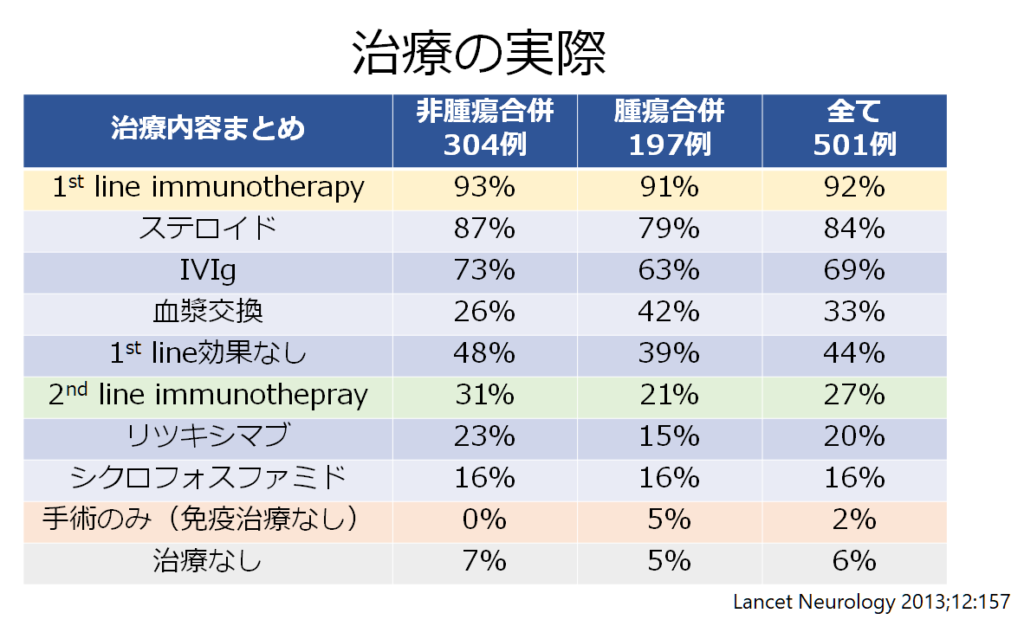
治療効果に関する報告のまとめは下記の通りです。
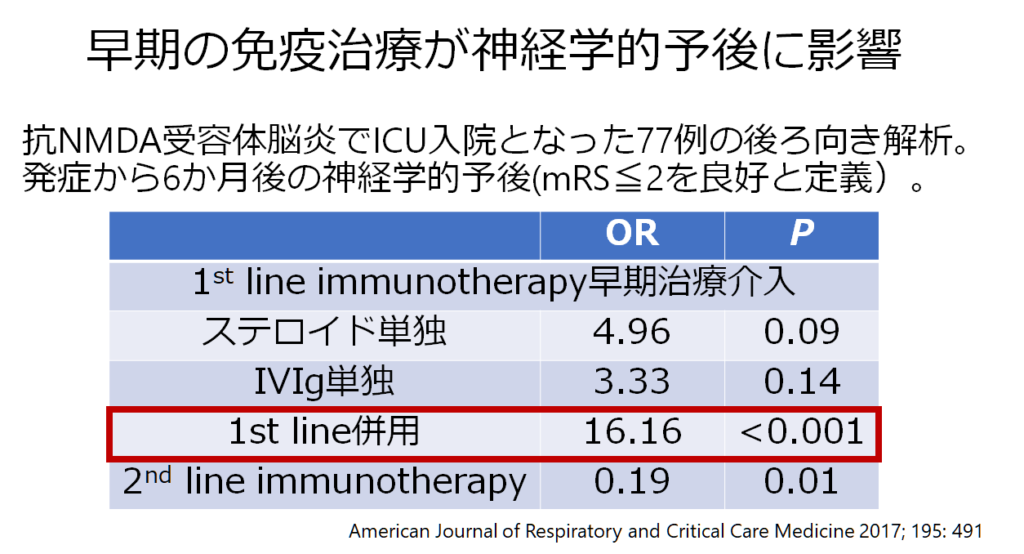
また後ろ向きの検討ですが、抗NMDA受容体脳炎でICU入室となった77例を解析した研究では早期の免疫治療の介入が神経学的予後と相関していた結果でした。抗体が出てから治療開始ではなく、抗体の結果が出るまで時間がかかるため各種検体(血清+髄液)を保存したら早期に免疫治療で介入することが重要と思います。
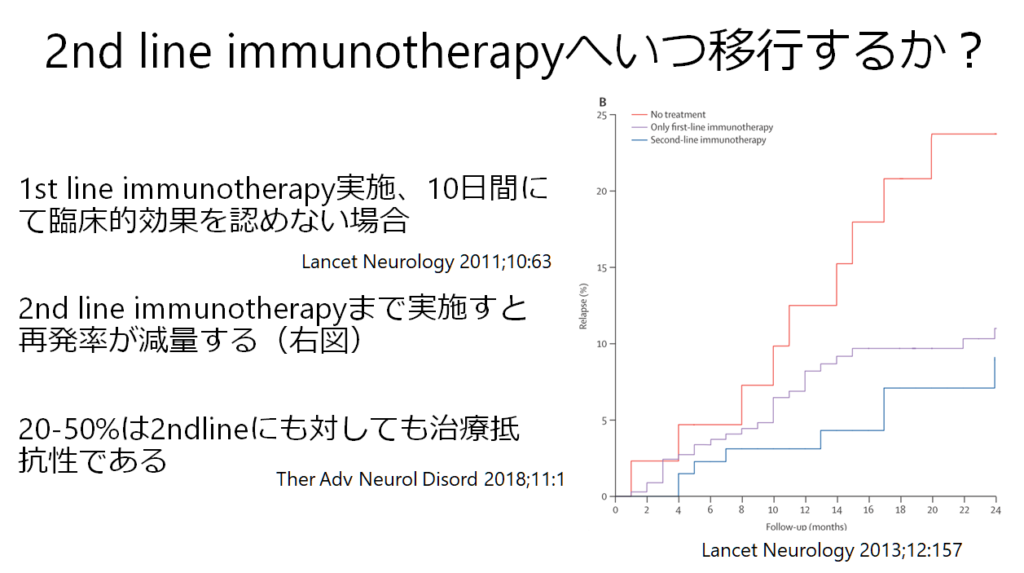
1st line therapyまではいいですが、問題は「いつ2nd line therapyに移行するか?」です。Dalmauの記載では10日間1st line therapy実施で臨床的効果を認めない場合とされていますが、実際にどの程度の改善を臨床的改善ととるか難しい場合もあります。以下の通り2nd line immunotherapyまで実施すると再発率が減少することも指摘されており、慣れた施設では早期からしっかり2nd line immunotherapyへ移行することと思います。しかし、これは実際にはなかなか勇気がいることなので経験も重要だと思います。
また併用薬で注意するべき薬剤はNMDA受容体と拮抗作用をもつ以下の薬剤が挙げられます。特に腫瘍合併例での手術ではこれらの薬剤に注意が必要です。麻酔関係の論文ではベンゾジアゼピン系薬剤+フェンタニルが最も安全に管理できるのではないか?と記載があります(BMC Anesthesiology 2014;14:5)。プロポフォールもin vitroではNMDA受容体を抑制する可能性を指摘されていますが、臨床的には問題なかったとする報告もあり使用は十分に可能と考えられます。
NO, Xenon, iso/sevo/desflurane(吸入麻酔薬),ketamine, tramadol, dextropropoxyphene, amantaidne
予後
75%:改善、25%:後遺症、死亡とされています。一般的に予後が良いイメージを持っている方も多いですが、決してそのようなことはありません。360例での6か月以上のフォローアップした研究では死亡率:4%(15例)、中央値:3.5か月(1-8か月)と報告されています。
内訳は感染症(3例)、心停止sudden cardiac arrest(2例)、呼吸障害(2例)、てんかんのコントロールつかない(2例)、腫瘍(2例)、撤退(1例)、不明(2例)となっています。長期管理になるため多くのケースで免疫抑制もあいまって感染との戦いになります。それ以外にもプロポフォール長期投与によるPRIS(ステロイド投与もPRISのリスクになりうる)、DVTなど一般的な内科・集中治療管理が重要です。
■高次脳機能の長期的な機能予後に関して Ann Neurol. 2021 Dec;90(6):949-961.
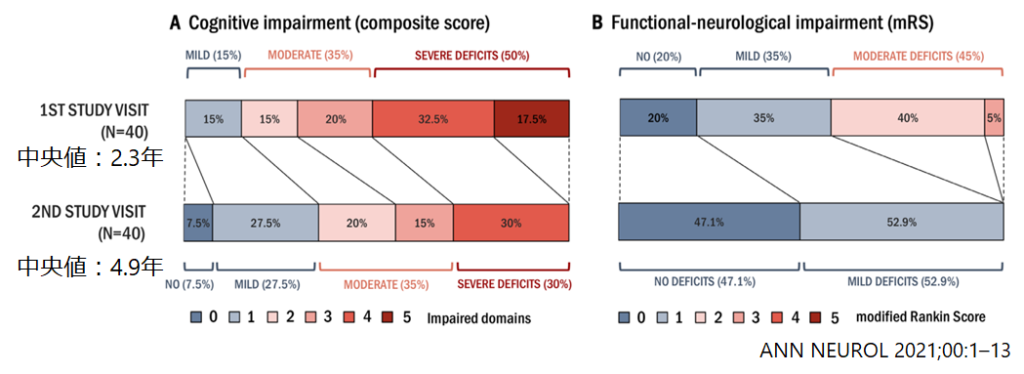
・43人の抗NMDA受容体抗体関連脳炎の患者さんの高次脳機能検査batteryを1回目(発症から中央値2.3年後)、2回目(発症から中央値4.9年後)とかなり長期にわたり高次脳機能をフォローした研究です。まだ疾患として確立したのが新しい分野ですが、約5年と非常に長期間フォローしている点がこの文献の強みと思います。
・約5年の経過でもmoderate-severeの高次脳機能障害を約2/3で認めた結果でした(下図左)。身体機能としてはno-deficitが約半数とかなり良い経過であるのに対して(下図右)、やはり高次脳機能障害の残存が目立つ印象があります。
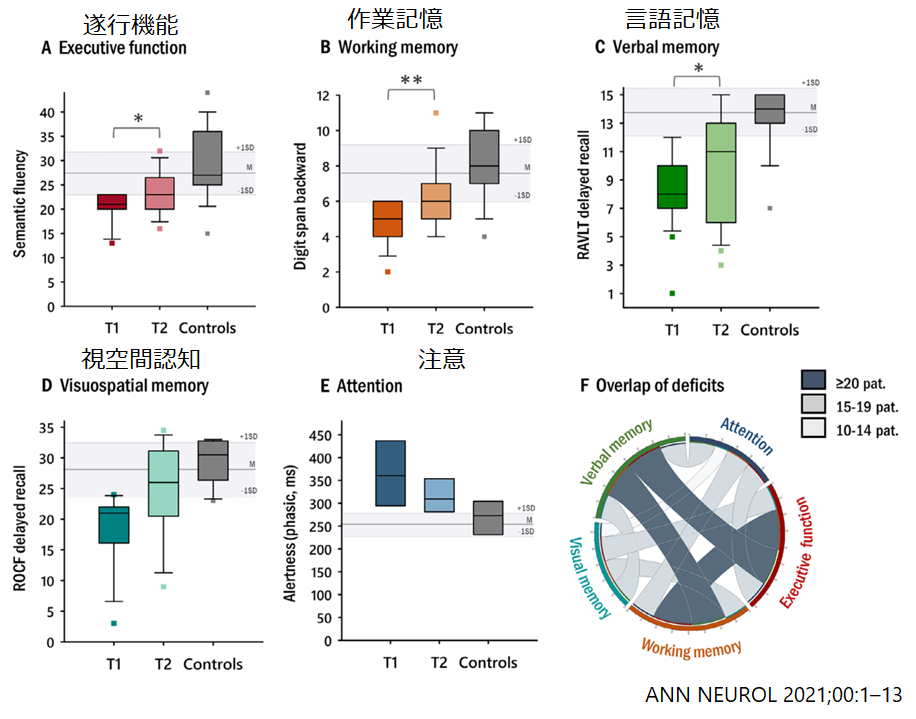
・高次脳機能障害残存のリスク因子としては治療の遅れ、当初の重症度、急性期治療期間の長さが挙げられています。
・この結果から実際の臨床で活かせることとしては「長期間的にゆっくりと高次脳機能が回復する可能性があるため、急性期治療後も年単位で長期に根気強く高次脳機能リハを継続することが重要である」ということになるかと思います。身体機能と比較して高次脳機能障害は一見気が付きにくい点なので(特に短い外来診療だけでは気が付きにくい)この点に注意しながら患者さんをフォローできればと思います。
参考文献
・Neurology 2016;87:2471:Dalmau先生によるlecture(必読)。
・Lancet Neurology 2011;10:63
管理人記録
・2021/10/28:高次脳機能の長期フォローに関する文献(ANN NEUROL 2021;00:1–13)追記