- 1 薬剤選択
- 2 2nd line therapy 薬剤比較検討の臨床試験
- 2.1 RCT
- 2.1.1 ESETT trial“Randomized Trial of Three Anticonvulsant Medications for Status Epilepticus” N Engl J Med 2019;381:2103-13.
- 2.1.2 IENE ECT with LIFE Trial “Levetiracetam versus fosphenytoin as a second- line treatment after diazepam for adult convulsive status epilepticus: a multicentre non- inferiority randomised control trial” J Neurol Neurosurg Psychiatry 2023;94:42–48.
- 2.2 コホート研究
- 2.1 RCT
- 3 初手から2nd line therapyの併用療法はありなのか?
薬剤選択
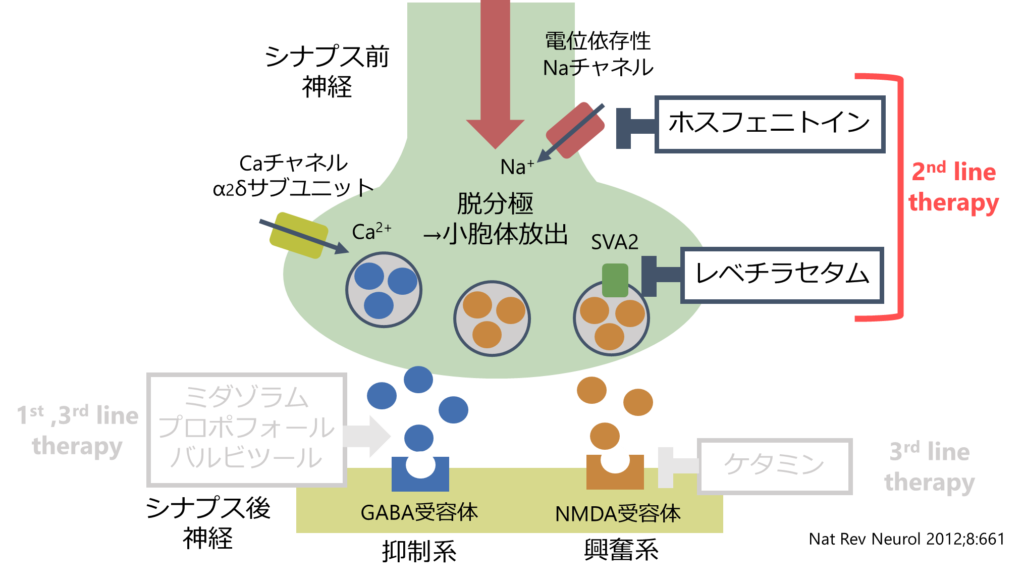
・どの薬剤がより優れているというデータはない。
・実臨床ではレベチラセタムまたはホスフェニトインを使用する。フェノバルビタールを使用することは管理人はない。
・レベチラセタムは重積量(3000mg)を投与することが重要(なんとなく1000mg投与とかにしない)。循環動態に影響を与えず、薬剤相互作用もないため投与しやすい。
・ホスフェニトインは血圧低下や房室ブロックになることが高齢者ではよくあるので、モニタリング新調に行う必要がある。また薬剤相互作用が多い点にも注意が必要。
・ラコサミドは今後てんかん重積における推奨度が上がる可能性がある。
| 項目 | レベチラセタム | ホスフェニトイン |
|---|---|---|
| 投与量 | 3000mg | Loading 22.5mg/kg |
| 副作用 | なし *長期は精神副作用 | 徐脈・血圧低下 |
| 相互作用 | なし | 多数あり |
| 注意点 | 中途半端な 投与量にしない | 高齢者では要注意 循環をモニターしながら投与 背景疾患や薬剤をよく確認 |
2nd line therapy 薬剤比較検討の臨床試験
RCT
ESETT trial“Randomized Trial of Three Anticonvulsant Medications for Status Epilepticus” N Engl J Med 2019;381:2103-13.
・目的とデザイン:てんかん重積での2nd line therapyのレベチラセタム、ホスフェニトイン、バルプロ酸(日本にはバルプロ酸静注薬はない)の治療成功における優越性 superiority または劣等性 inferiorityを検討するランダム化臨床試験
⇒中間解析の結果、試験を最大数まで継続したとしても、いずれかの薬剤が他よりも優れている、あるいは劣っていると特定できる確率は1%未満であると判断され早期終了
・ベンゾジアゼピン抵抗性の基準
①前提条件ベンゾジアゼピン累積投与量 ジアゼパム10mg, ロラゼパム4mg, ミダゾラム10mg
②ベンゾジアゼピン最終投与から5分以上経過しても、けいれんが持続または再発している(かつ最終投与から30分以内である)
・薬剤投与量(下表)
・プロトコルからの逸脱 27%:内訳①事前に投与されたベンゾジアゼピンの量が不十分だったケース(26名、②投与のタイミングが早すぎた、あるいは遅すぎたケース(50名)
・以下の薬剤をいずれも10分で投与
| 薬剤名 | 体重あたりの投与量 | 最大投与量 |
|---|---|---|
| レベチラセタム | 60 mg/kg | 4,500 mg |
| ホスフェニトイン | 20 mgPE/kg | 1,500 mgPE |
| バルプロ酸 | 40 mg/kg | 3,000 mg |
・主要評価項目:60分以内の発作消失かつ意識状態の改善
⇒失敗基準①臨床的にけいれんなどが消失していない、または②意識状態が改善していない(刺激に対する合目的な半報、指示理解、発語のいずれも認めない)
⇒これらの評価に脳波検査は含まれておらず医師による臨床観察で判断
・結論:3つの薬剤における有意差はなし
| 評価項目 | レベチラセタム | ホスフェニトイン | バルプロ酸 |
|---|---|---|---|
| 主要評価項目の達成率 (60分以内の発作消失と意識改善) | 47%(68/145人) | 45%(53/118人) | 46%(56/121人) |
| 最も効果的である事後確率 | 0.41 | 0.24 | 0.35 |
| 安全性:生命を脅かす低血圧 | 0.7% (1人) | 3.2% (4人) | 1.6% (2人) |
| 安全性:気管挿管 (60分以内) | 20.0% (30人) | 26.4% (33人) | 16.8% (21人) |
| 安全性:死亡 | 4.7% (7人) | 2.4% (3人) | 1.6% (2人) |
| 発作消失までの時間 (中央値) | 10.5分 | 11.7分 | 7.0分 |
| 急性発作再発 (60分〜12時間) | 10.7% | 11.2% | 11.2% |
| ICU(集中治療室)入院率 | 60.0% | 59.3% | 58.7% |
患者背景 384例
・平均32-33歳(1-94歳) 年齢内訳 -18歳 39%, 18-65歳 48%, 65歳- 13%
・てんかん既往 68%
・最終診断:てんかん重積状態 86%, PNES 10%
・発作持続時間(2nd line投与までの):約60分
・治療失敗の原因:発作頓挫せず 70%, 意識障害遷延 25%
limitation
1. 診断と評価に関する限界
• 心因性発作の混入: 登録された患者の10%が心因性非てんかん性発作(PNES)
• 脳波(EEG)による確認の欠如: 主要評価項目である発作消失の判定は、脳波ではなく**臨床的な観察(視覚的な判断)**に基づいて行われた。
• 意識障害の原因特定が困難: 臨床的なけいれんは止まったものの、60分時点で意識が改善しなかった患者が52名(治療全体の25%)いました。脳波がないためNCSEかどうか薬剤過鎮静か区別困難
2. 薬剤の投与量と盲検化に関する限界
• 用量設定: 薬剤の用量は公表されている知見に基づいて設定されたが、異なる用量であれば異なる有効性や安全性が示された可能性がある。
• ホスフェニトインの用量不足の可能性: ホスフェニトインは注入速度に制限があるため、最大用量が1500mgPEに抑えられました。これにより、体重75kg以上の患者にとっては投与量が不十分であった可能性。
• 盲検化の解除: 継続する発作に対して次の薬剤を選択する必要がある場合など、一部の症例で盲検化を解除(アンブライディング)する必要がありました。
3. データ収集とプロトコル遵守に関する限界
• 副作用データの不足: 登録から24時間以降の軽微な副作用(発疹や一過性の肝酵素上昇など)についてはデータが収集されていないため、遅発性の有害事象を見逃している可能性があります。
• プロトコルからの逸脱: 救急現場での緊急実施であったため、事前のベンゾジアゼピン投与量やタイミングが基準に合致しないなどの適格性の逸脱が比較的高い割合(27%)で発生しました。ただし、これを除外した解析でも主要解析と同様の結果が得られています。
IENE ECT with LIFE Trial “Levetiracetam versus fosphenytoin as a second- line treatment after diazepam for adult convulsive status epilepticus: a multicentre non- inferiority randomised control trial” J Neurol Neurosurg Psychiatry 2023;94:42–48.
| 項目 | 内容 |
|---|---|
| P (対象患者) | 救急搬送された成人の痙攣性てんかん重積状態(SE)患者。 ベンゾジアゼピン抵抗性かどうかは関係なし ・年齢:20歳以上。 ・SEの定義:5分以上続く発作、または意識障害が回復しないまま2回以上の発作が連続する場合。 ・除外基準:20歳未満、妊娠中、挿管済み、薬剤アレルギー、心因性発作疑いなど。 |
| I (介入) | レベチラセタム(LEV)の静脈内投与。 ・タイミング:第1選択薬であるジアゼパム(1~20mg)投与後。 ・投与量:1000~3000 mg(100mL生理食塩水に溶解)。 *実際投与の初回負荷中央値は2000mg ・投与速度:2~5 mg/kg/分。 |
| C (比較対照) | ホスフェニトイン(FPHT)の静脈内投与。 ・タイミング:第1選択薬であるジアゼパム(1~20mg)投与後。 ・投与量:22.5 mg/kg(フェニトイン換算で15 mg/kg)。 ・投与速度:3 mg/kg/分または150 mg/分を超えない速度。 |
| O (アウトカム) | 主要評価項目:薬剤投与開始から30分以内の発作停止率。 副次評価項目:24時間以内の発作再発率、24時間以内の気管挿管率、重篤な有害事象(心停止、不整脈、低血圧、呼吸停止など)の発生率。 |
| 研究デザイン | open-label RCT, non-inferiority |
結果:レベチラセタムのホスフェニトインに対する非劣性が確認
| 評価項目 | ホスフェニトイン | レベチラセタム | P値 |
|---|---|---|---|
| 主要評価項目 | |||
| 30分以内の発作停止, n (%) | 67 (83.8) | 83 (89.2) | 0.29 |
| 副次評価項目 | |||
| 24時間以内の発作再発率, n (%) | 12 (15.0) | 16 (17.2) | 0.70 |
| 24時間以内の気管挿管, (%) | 12 (15.0) | 15 (16.1) | 0.84 |
| その他の評価項目 | |||
| 入院7日後の修正Rankinスケール (mRS) | 0.74 | ||
| 0 (無症候) | 21 (26.3) | 26 (28.0) | |
| 1 (症候はあるが障害はない) | 16 (20.0) | 13 (14.0) | |
| 2 (軽度の障害) | 8 (10.0) | 6 (6.5) | |
| 3 (中等度の障害) | 7 (8.8) | 8 (8.6) | |
| 4 (中等度から重度の障害) | 14 (17.5) | 18 (19.4) | |
| 5 (重度の障害) | 11 (13.8) | 20 (21.5) | |
| 6 (死亡) | 3 (3.8) | 2 (2.2) |
治療内容まとめ
| 項目 | ホスフェニトイン | レベチラセタム | P値 |
|---|---|---|---|
| 試験薬の負荷投与量 (mg) | 1350 (1125, 1500) | 2000 (1000, 3000) | – |
| 試験薬投与前に投与されたジアゼパム投与量 (mg) | 10 (5, 10) | 10 (5, 10) | 0.35 |
| ジアゼパム静注から試験薬静注までの時間 (分) | 14 (7, 24) | 14 (9, 29) | 0.61 |
| 24時間以内の試験薬投与量 (mg) | 1350 (1125, 1500) | 3000 (1500, 3500) | – |
安全性:ホスフェニトイン群3例で重篤有害事象(レベチラセタム群では0例)
| 項目 | ホスフェニトイン | レベチラセタム | P値 |
|---|---|---|---|
| 1時間以内の重篤な有害事象, n (%) | 3 (3.7) | 0 (0) | 0.061 |
| 心停止 | 1 (1.2) | 0 (0) | |
| 呼吸停止 | 1 (1.2) | 0 (0) | |
| 低血圧 ※ | 1 (1.2) | 0 (0) | |
| 24時間以内の重篤な有害事象, n (%) | 0 (0) | 0 (0) | |
| 7日以内の重篤な有害事象, n (%) | 0 (0) | 0 (0) |
患者背景
| 項目 | ホスフェニトイン | レベチラセタム | P値 |
|---|---|---|---|
| 年齢 (歳) | 65 ± 19 | 67 ± 16 | 0.51 |
| 男性, n (%) | 57 (71.3) | 60 (64.5) | 0.32 |
| 肝疾患の既往, n (%) | 3 (3.7) | 3 (3.2) | 0.87 |
| 入院時cre(mg/dL) | 0.87 (0.7, 1.1) | 0.86 (0.6, 1.1) | 0.48 |
| てんかん重積状態の型, n (%) | 0.48 | ||
| 強直間代発作 (Tonic clonic seizure) | 57 (71.3) | 72 (77.4) | |
| 強直発作 (Tonic seizure) | 0 (0) | 1 (1.1) | |
| 反復性部分発作 (Repeated partial seizures) | 10 (12.5) | 10 (10.8) | |
| 欠神発作 (Absence of seizures) | 0 (0) | 1 (1.1) | |
| 複雑部分発作 (Complex partial seizure) | 13 (16.3) | 9 (9.7) | |
| てんかん重積状態の原因, n (%) | 0.37 | ||
| 特発性てんかん (Idiopathic seizure) | 19 (23.8) | 15 (16.1) | |
| 急性脳卒中 (Acute stroke) | 6 (7.5) | 12 (12.9) | |
| 陳旧性脳卒中 (Old stroke) | 22 (27.5) | 31 (33.3) | |
| 急性外傷 (Acute trauma) | 2 (2.5) | 2 (2.2) | |
| 陳旧性外傷 (Old trauma) | 5 (6.3) | 1 (1.1) | |
| 脳腫瘍 (Brain neoplasm) | 11 (13.8) | 12 (12.9) | |
| その他 (Others) | 15 (18.8) | 20 (21.5) | |
| 治療前の発作持続時間 (分) | 42.0 (21, 90) | 60 (30, 80) | 0.25 |
Limitation
1. 盲検化されていない(Open-label design) 治療を担当する医師やアウトカムを評価する医師が、どの薬剤を使用しているかを知っている「非盲検試験」でした。これにより、評価にバイアスがかかる可能性があります。
2. 投与量の設定基準の違い ホスフェニトイン(FPHT)の投与量は体重換算(22.5 mg/kg)で統一されていましたが、レベチラセタム(LEV)は日本のガイドラインに基づき1000 mgから3000 mgの範囲で医師の判断に委ねられました。
3. 対象患者の組み入れと薬剤投与のタイミング 本研究では、第1選択薬であるジアゼパムの効果判定(発作が止まったかどうか)を待たずに、ジアゼパム投与後に続けて第2選択薬(試験薬)を投与しました。これは日本のガイドラインや救急現場の実臨床に即したものですが、ベンゾジアゼピン単独で発作が止まっていた患者も含まれている可能性があり、その結果、両群ともに主要評価項目(発作停止率)が高い数値となった可能性があります。これは、ベンゾジアゼピン無効例のみを対象とした過去の先行研究とは異なる点です。
4. 実施施設と患者層の偏り 研究が行われたのは一般的な救命救急センターであり、てんかん専門センターではありませんでした,。そのため、難治性てんかん患者が集まる専門施設での研究とは異なり、脳卒中を原因とする高齢のてんかん患者が多く含まれており、これが有効性や安全性に影響を与えた可能性があります。
5. 診断精度の限界(脳波を用いていない) 過去の多くのランダム化比較試験と同様に、発作時の脳波(EEG)による診断を行っていません。そのため、心因性非てんかん発作などの「てんかん模倣疾患(Epilepsy-mimicking diseases)」が対象に含まれてしまった可能性があります(実際に除外された症例もありました),。また、痙攣のないてんかん重積状態(NCSE)の除外も課題として挙げられています。
6. その他の未調整因子 試験薬以外の治療介入がプロトコルで厳密に定義されておらず、医師の裁量でジアゼパムや試験薬の用量が選択されたため、未知の交絡因子(結果に影響を与える隠れた要因)が存在する可能性があります。
(管理人)本研究の特徴と注意点
・「ベンゾジアゼピンが効かなかった患者」を対象とした試験ではなく、「ジアゼパムを含む一連の初期治療フロー(ジアゼパム+第2選択薬)」を受けた患者を対象とした試験である点に注意(ESETT試験などはベンゾジアゼピンで頓挫しなかった例に限定して2nd lineを比較している点と異なる)
⇒この結果発作停止率が約80%強と非常に高い値である
・小児を含めず成人に限定している(ESETT試験は小児など全て含めている)
・レベチラセタムのホスフェニトインに対する非劣性を検討している
・レベチラセタムの初期投与量は2000mgとガイドライン推奨よりは少ない量(それでも非劣性を証明できている訳ではあるが)
コホート研究
“Comparison of lacosamide, levetiracetam, and valproate as second-line therapy in adult status epilepticus: Analysis of a large cohort” Epilepsia. 2025;66:e73–e77.
・方法:2013年1月から2022年12月までの10年間に、スイスの大学病院(CHUV)のレジストリに登録された成人SE症例961エピソードを分析
・比較対象:レベチラセタム(413件)、バルプロ酸(110件)、**ラコサミド(75件)の3剤
・評価項目:発作の終息率、人工呼吸器管理の必要性、退院時の臨床転帰(元の状態への回復、新たな障害、死亡)
⇒多変量解析の結果いずれも統計的に有意差は認めない結果
| 評価項目 | ラコサミド control | レベチラセタム OR(95%CI) | バルプロ酸 (95% CI) | モデル適合度 (p値) |
|---|---|---|---|---|
| 1st line, 2nd line therapyに抵抗性のSE | 1 | 1.22 (0.67–1.87) | 1.15 (0.63–2.08) | 0.294 |
| 人工呼吸器管理の必要性 | 1 | 0.85 (0.45–1.58) | 0.67 (0.31–1.41) | 0.208 |
| 機能状態のベースライン復帰 | 1 | 1.21 (0.71–2.10) | 1.07 (0.57–2.01) | 0.276 |
患者背景の比較
| 項目 | ラコサミド (n=75) | レベチラセタム (n=413) | バルプロ酸 (n=110) | p値 |
|---|---|---|---|---|
| 女性 (%) | 33 (44.0%) | 191 (46.2%) | 41 (37.2%) | .243 |
| 平均体重 (kg) | 73.3 | 70.9 | 70.4 | .088 |
| STESSスコア (中央値) | 2 | 3 | 2 | <.001 |
| 平均年齢 (歳) | 66.1 | 65.3 | 60.7 | .011 |
| 急性症候性発作 | 53.3% | 52.1% | 49.1% | |
| 初めてのてんかん発作 (%) | 42 (38.2%) | 169 (40.9%) | 67 (60.1%) | <.001 |
| 発作型:全般性強直間代発作 (GTC) (%) | 19 (25.3%) | 196 (47.5%) | 38 (34.5%) | <.001 |
| 治療前の昏迷・昏睡 (%) | 42 (56.0%) | 169 (40.9%) | 67 (60.9%) | <.001 |
| 致死的原因の可能性 (%) | 40 (53.3%) | 215 (52.1%) | 54 (49.1%) | .859 |
| 初期・第二選択治療の適切さ | 20 (26.7%) | 188 (45.5%) | 47 (42.7%) | .010 |
| 1時間以上の治療遅延 | 64 (85.3%) | 254 (61.5%) | 75 (68.1%) | <.001 |
| 平均負荷投与量 (mg) | 473 | 2186 | 1769 | – |
| 体重あたり平均投与量 (mg/kg) | 6.5 | 30.8 | 25.1 | – |
• 重症度の違い: てんかん重積状態の重症度スコアであるSTESSは、レベチラセタム群で有意に高く、より重症な症例に使用される傾向がありました。
• 治療の質とタイミング: ラコサミド群では、他の薬剤と比較して治療の遅れ(1時間以上)が多く(85.3%)、また初期治療および第二選択治療が「不適切」と判断される割合が高い(適切さが26.7%のみ)という特徴がありました。
• 発作の性質: バルプロ酸群では、今回が初めてのてんかん発作である割合が高く(60.1%)、一方でラコサミド群は治療前に昏迷や昏睡状態にある割合が高い(56.0%)傾向にありました。
• 投与設計: ラコサミドの平均投与量は6.5 mg/kgであり、治療の適切性の基準として設定された5 mg/kgを上回っていました。
⇒本研究ではラコサミドが2nd line therapyとして同等である可能性について提言
初手から2nd line therapyの併用療法はありなのか?
・早期にSEを頓挫させるためには、初手からベンゾジアゼピンに2nd line therapyを併用した方がよいのではないか?というストラテジーについてです。
・現時点では併用が単独より有益であるというデータはありません。
・このため現行もガイドライン上はStep-wise approachで初手からの併用療法に関して推奨はありませんが、今後変化していく可能性があります。
・現状あるRCTの2つ”VA Cooperative Study”と”SAMUKeppra Trial”を紹介します。
・”Monotherapy or Polytherapy for First-Line Treatment of SE?”Journal of Clinical Neurophysiology 33(1):p 14-17, February 2016.は併用療法についてのReview articleですが、少し古い内容でありレベチラセタム併用などの記載もないため紹介しません。
“VA Cooperative Study” N Engl J Med 1998;339:792-8.
Design:double-blinded RCT(ITT解析ではない*確定診断群による解析)
| 項目 | 内容 |
|---|---|
| P (Population) 対象患者 | CSE成人患者 518例(確定診断群) 1. Overt(明らかな発作) 384例:目視で確認できる全身けいれんが持続している状態。 2. Subtle(微細な発作)134例:昏睡状態で、脳波上の発作波(ictal discharges)が見られるもの(微細な筋収縮や眼球偏位を伴うこともある)。 |
| I (Intervention) & C (Comparison) 介入・比較 | 以下の4つの静脈内投与レジメンによるランダム化二重盲検比較試験。 1. ロラゼパム (0.1 mg/kg) 2. フェノバルビタール (15 mg/kg) 3. ジアゼパム (0.15 mg/kg) + フェニトイン (18 mg/kg) 4. フェニトイン単独 (18 mg/kg) |
| O (Outcome) アウトカム | 主要評価項目(治療成功の定義):薬剤注入開始から20分以内に臨床的および脳波上の発作活動がすべて消失し、その後40分間再発がないこと。 副次評価項目:12時間以内の発作再発率、副作用の発現率(低換気、低血圧、心拍リズム障害)、30日後の転帰(退院、入院継続、死亡), |
結果
・Overt群ではロラゼパム単独がフェニトイン単独よりも有意に治療成功率が高い
(フェノバルビタール単独やジアゼパム+フェニトイン併用とは有意差なし)
・2剤併用でも発作抑制効果は高くならない
・副作用も差はなし
| 項目 | ロラゼパム | フェノバルビタール | ジアゼパム + フェニトイン | フェニトイン |
|---|---|---|---|---|
| 投与量 | 0.1 mg/kg | 15 mg/kg | ジアゼパム: 0.15 mg/kg, フェニトイン: 18 mg/kg | 18 mg/kg |
| Overt群 治療成功率 | 64.9% (フェニトイン単独群に対し有意に優越 P=0.002) | 58.2% | 55.8% | 43.6% |
| Subtle群 治療成功率 | 17.9% | 24.2% | 8.3% | 7.7% (群間に有意差なし) |
| 副作用発現率 (Overt群) | 低換気: 10.3%, 低血圧: 25.8%, 不整脈: 7.2% | 低換気: 13.2%, 低血圧: 34.1%, 不整脈: 3.3% | 低換気: 16.8%, 低血圧: 31.6%, 不整脈: 2.1% | 低換気: 9.9%, 低血圧: 27.0%, 不整脈: 6.9% |
| 副作用発現率 (Subtle群) | 低換気: 12.8%, 低血圧: 59.0%, 不整脈: 7.7% | 低換気: 15.2%, 低血圧: 48.5%, 不整脈: 9.1% | 低換気: 2.9%, 低血圧: 58.3%, 不整脈: 5.6% | 低換気: 7.7%, 低血圧: 57.7%, 不整脈: 0.0% |
副作用:差なし
| GCSのタイプと副作用 | ロラゼパム | フェノバルビタール | ジアゼパム +フェニトイン | フェニトイン |
|---|---|---|---|---|
| Overt (明らかな発作) | ||||
| 低換気 (%) | 10.3 | 13.2 | 16.8 | 9.9 |
| 低血圧 (%) | 25.8 | 34.1 | 31.6 | 27.0 |
| 心拍リズム障害 (%) | 7.2 | 3.3 | 2.1 | 6.9 |
| Subtle (微細な発作) | ||||
| 低換気 (%) | 12.8 | 15.2 | 2.9 | 7.7 |
| 低血圧 (%) | 59.0 | 48.5 | 58.3 | 57.7 |
| 心拍リズム障害 (%) | 7.7 | 9.1 | 5.6 | 0.0 |
患者背景
| 項目 | Overt群 | Subtle群 |
|---|---|---|
| 平均年齢 | 58.6 ± 15.6 歳 | 62.0 ± 15.1 歳 |
| 性別(男性) | 82.3% | 85.1% |
| 退役軍人 (Veteran) | 70.1% | 80.6% |
| てんかんの既往 | 42.4% | 12.7% |
| てんかん重積の既往 | 12.8% | 4.5% |
| 発作重積の持続時間 (中央値) | 2.8 時間 | 5.8 時間 |
| 30日後の死亡率 | 27.0% | 64.7% |
薬剤投与の実際
| 薬剤 | 投与量 (mg/kg) | 血清中濃度 (µg/ml) | 注入時間(分) |
|---|---|---|---|
| ロラゼパム | 0.10 ± 0.01 | 0.231 ± 0.299 | 4.7 ± 7.2 |
| フェノバルビタール | 14.96 ± 2.53 | 31.2 ± 37.2 | 16.6 ± 11.5 |
| ジアゼパム +フェニトイン | 0.15 ± 0.02 15.08 ± 4.84 | 0.245 ± 0.307 31.8 ± 19.2 | 42.0 ± 38.1 |
| フェニトイン | 16.02 ± 3.21 | 30.0 ± 13.6 | 33.0 ± 20.1 |
Limitation
・治療成功の定義が「20分以内の発作消失+40分発作再燃なし」と厳格な定義であるため過去の研究よりも成功率が低い
・フェニトインは投与速度に制限があるため、不利に働いた可能性がある など
“SAMUKeppra Trial” Lancet Neurol 2016; 15: 47–55
“Prehospital treatment with levetiracetam plus clonazepam or placebo plus clonazepam in status epilepticus (SAMUKeppra): a randomised, double-blind, phase 3 trial”
背景・目的:てんかん重積は早期の頓挫が重要であるが、ベンゾジアゼピンでは30-40%でてんかん重積頓挫できない。
Design; double-blinded RCT, superiority フランスの13の救急医療センターと26の病院部門
| PICO | 内容 |
|---|---|
| P (Population) | 院外(病院到着前)18歳以上の成人患者。 5分以上持続するCSE、または意識回復のない反復性の全身けいれん患者。 妊娠中、即時手術が必要な外傷、心停止後、微細な発作(subtle status)などは除外。 |
| I (Intervention) | レベチラセタム(2500mg)5分間かけてIV + クロナゼパム(1mg)IV |
| C (Comparison) | プラセボIV + クロナゼパム(1mg)IV ※両群とも発作が5分以上持続した場合は、クロナゼパム(1mg)の追加投与 |
| O (Outcome) | 【主要評価項目】薬剤注入開始から15分以内のけいれん停止 ⇒結果はレベチラセタム群74%、プラセボ群84%であり、レベチラセタム追加による優越性は示されなかった,。 |
結果:レベチラセタム併用による発作頓挫の優越性は示せなかった
・post hoc analysisで15日後(または退院時)の神経学的後遺症がレベチラセタム併用が有意に少ない
| 評価項目 | クロナゼパム +レベチラセタム (n=68) | クロナゼパム +プラセボ (n=68) | RR(95% CI) | p値 |
|---|---|---|---|---|
| 主要評価項目 (Primary outcome) | ||||
| 治療開始から15分以内のけいれん停止 | ||||
| 修正ITT解析 | 50/68 (74%) | 57/68 (84%) | 0.88 (0.74–1.05) | 0.14 |
| Per-protocol解析 | 46/61 (75%) | 50/58 (86%) | 0.87 (0.73–1.04) | 0.14 |
| 副次評価項目 (Secondary outcomes) | ||||
| 初回注射からけいれん停止までの時間 (分) † | 3 (0–50) | 5 (0–41) | — | 0.97 |
| 5分後のクロナゼパム追加投与の必要性 | 28/67 (42%) | 28/65 (43%) | 0.97 (0.65–1.44) | 0.88 |
| 15分後の抗てんかん薬投与の必要性 | 19/67 (28%) | 15/65 (23%) | 1.23 (0.68–2.21) | 0.49 |
| 35分時点での覚醒徴候あり ‡ | 22/56 (39%) | 21/51 (41%) | 0.95 (0.60–1.51) | 0.84 |
| 35分時点での全身麻酔のための気管挿管 | 9/68 (14%) | 12/67 (18%) | 0.95 (0.82–1.09) | 0.45 |
| 病院到着時にけいれんあり | 1/68 (1%) | 2/66 (3%) | 0.49 (0.05–5.23) | 0.62 |
| 病院到着時に覚醒している | 29/39 (74%) | 31/44 (70%) | 0.87 (0.43–1.75) | 0.69 |
| 入院中のけいれん再発 | 7/67 (10%) | 13/68 (19%) | 0.55 (0.23–1.28) | 0.16 |
| 入院期間(全期間、日数) | 10 (1–15) | 10 (1–15) | — | 0.95 |
| 入院期間(ICU、日数) | 3 (0–15) | 3 (1–15) | — | 0.74 |
| 事後解析 (Post-hoc analyses), | ||||
| 1回目と2回目のクロナゼパム注射の間隔 (分) | 8 (5–25) | 10 (5–25) | — | 0.73 |
| 35分時点でのけいれん停止 | 55/68 (81%) | 55/68 (81%) | 1.00 (0.85–1.18) | 1 |
| 病院前けいれん再発 (35分以内に停止した患者において) | 9/42 (21%) | 11/49 (22%) | 0.95 (0.44–2.08) | 0.91 |
| 入院15日目(または退院時)の神経学的状態 | ||||
| 死亡 | 3/66 (5%) | 4/65 (6%) | 0.74 (0.17–3.17) | 0.72 |
| 新たな神経学的欠損 ¶ | 1/63 (2%) | 8/61 (13%) | 0.12 (0.02–0.94) | 0.016 |
患者背景
| 特性 | クロナゼパム+ レベチラセタム | クロナゼパム+ プラセボ |
|---|---|---|
| 年齢(歳) | 55 (18) | 53 (18) |
| 性別(男性) | 49 (72%) | 45 (66%) |
| 重積状態発症から薬剤注入までの時間(分) | 58 (15–135) | 60 (20–258) |
| 最終診断 | ||
| てんかん重積状態 | 66 (97%) | 64 (94%) |
| 非てんかん性心因性発作 | 2 (3%) | 4 (6%) |
| てんかんの既往歴あり | 46/66 (70%) | 38/64 (59%) |
| 抗てんかん薬の中断による重積状態 | 10/45 (22%) | 9/38 (24%) |
| てんかん症候群 | ||
| 特発性全般てんかん | 2/46 (4%) | 6/38 (16%) |
| 部分てんかん(焦点性てんかん) | 40/46 (87%) | 27/38 (71%) |
| その他 | 2/46 (4%) | 2/38 (5%) |
| 分類不能 | 2/46 (4%) | 3/38 (8%) |
| 原因 * | ||
| 器質的病変あり | 42/65 (65%) | 41/63 (65%) |
| 腫瘍 | 8/42 (19%) | 15/41 (37%) |
| 脳血管障害 | 16/42 (38%) | 13/41 (32%) |
| 外傷 | 13/42 (31%) | 11/41 (27%) |
| 炎症 | 0/42 (0%) | 1/41 (2%) |
| 変性疾患 | 3/42 (7%) | 1/41 (2%) |
| 代謝性 | 7/66 (11%) | 4/63 (6%) |
| 感染性 † | 3/66 (5%) | 6/63 (10%) |
| 中毒性(アルコール離脱含む) ‡ | 25/65 (38%) | 15/64 (23%) |
| その他 | 7/66 (11%) | 6/64 (9%) |
| 原因不明 | 3/65 (5%) | 6/64 (9%) |
Limitation
1. プラセボ群(対照群)の高い奏効率による「天井効果」
研究計画段階では、対照群(クロナゼパム+プラセボ)のけいれん停止率を50%と想定していましたが、実際の結果は**84%**と極めて高い成功率でした。対照群でこれほど高い効果が出てしまったため、レベチラセタムの上乗せによる追加効果(優越性)を統計的に検出することが困難になった可能性があります。
2. 評価タイミングと追加処置によるバイアス
主要評価項目である「15分後のけいれん停止」を判定する前に、現地のガイドラインに従って**5分後にクロナゼパムの追加投与(2回目)**が行われる場合がありました。
• もしレベチラセタムが有効であれば、実薬群では2回目のクロナゼパム投与の必要性は減るはずです。
• しかし、プラセボ群で発作が続いて2回目のクロナゼパムが投与され、それによって発作が止まった場合、15分時点での結果は「成功」と判定されます。
• これにより、実薬群とプラセボ群の差が縮まってしまい、レベチラセタム本来の効果がマスクされた(隠れてしまった)可能性があります。
3. 同意取得困難による除外(選択バイアス)
無作為に割り付けられた患者203名のリストのうち、法的に必要な同意が得られなかったため**47名(23%)**が解析から除外されました。治療の成功・失敗が患者の同意能力(事後承諾など)に影響を与えていた場合、解析結果にバイアスがかかっている可能性があります。ただし、除外された割合は両群で同程度でした。
4. 試験の早期中止とサンプルサイズ不足
中間解析の結果、両群に差がないことが明らかになったため、試験は予定よりも早期に中止されました,。その結果、全体のサンプルサイズが小さくなり、けいれんの原因別(腫瘍、脳卒中など)のサブグループ解析を行い、特定の原因に対する有効性を検証することが不可能となりました。
5. 患者背景の不均衡
無作為化を行ったにもかかわらず、腫瘍、代謝性、中毒性といったけいれんの原因の分布が、両群間で不均一でした,,。事後解析で神経学的予後に差が出たこと(レベチラセタム群で神経欠損が少ない)も、薬の効果ではなく、こうした併存疾患や原因の偏りに起因する可能性があります。
6. 治療開始までの遅延
けいれん重積状態の発症から最初の薬剤注入までの時間の中央値は約1時間(58〜60分)でした。より早期(1時間以内)にレベチラセタムを投与できていれば、より高い効果が得られた可能性は排除できませんが、救急搬送の現実としてこれ以上の短縮は困難であるとも述べられています。
7. 用量設定の可能性
本試験ではレベチラセタム2.5gを使用しましたが、これよりさらに高用量であれば効果があった可能性も完全には否定できないとされています


