病原体
・Cryptococcus neoformans(世界中どこでもあり基本)
・Cryptococcus gattii(亜熱帯、オーストラリア、パプアニューギニアなどで限定的)
感染経路:肺からの空気感染(airzole)
・肺からの血流感染を経由して中枢神経へ感染
・潜伏期間後の再活性化により発症する
・菌体は莢膜に包まれており、マクロファージに取り込まれて免疫細胞からの攻撃を免れる作戦をとる。具体的にはマクロファージに取り込まれたまま脳血管上皮細胞を通過し、血液脳関門を超える。髄液は発育しやすい環境である。
・ヒトからヒトへの感染例は報告なし
(動物からの直接感染を示唆するものも不十分であり人獣共通感染症とは言えない)
・感染の季節性を明確に指摘することはできない。
C.neoformans
・土壌に広く存在する(鳥、特に鳩の排泄物)、野菜、果物、ミルク、土中、世界中どこにも存在する
・木に存在する菌体を鳩がただvectorとして土壌へ運んでいるだけの可能性もある
・ヒトの常在菌ではない
*NewYorkでの10才以下ではほとんどがCryptococcusに対する抗体を保有しており、無症候性の感染を繰り返している可能性がある
・鳩が発症することは基本的になし(体温が高いため)
下図:N Engl J Med 2024;390:1597-610.より引用
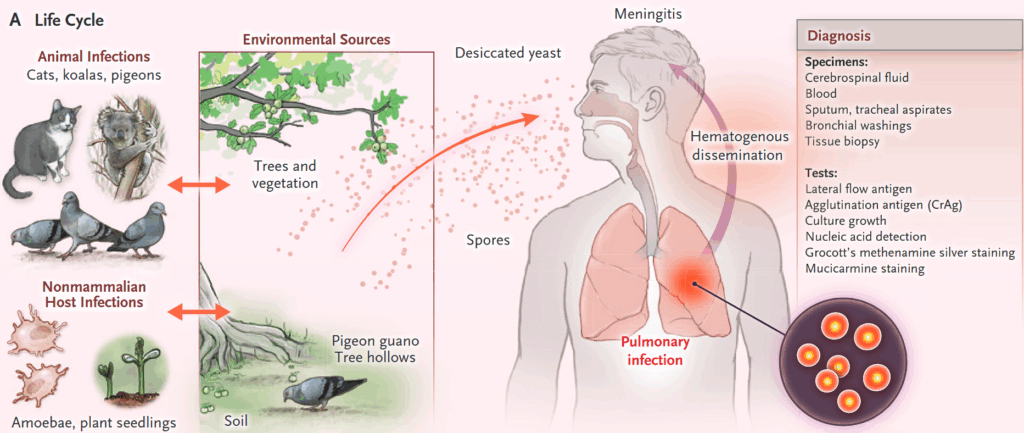
感染リスク因子
HIV感染を含む免疫抑制状態の有無は必ず検索する
・HIV(HIV患者の髄膜炎原因1位はクリプトコッカス髄膜炎)
・移植後免疫患者(アメリカでの非HIV関連クリプトコッカス症の約1/3を占める)
・免疫抑制状態
・HIV非感染者:ステロイド、サルコイドーシス、特発性CD4リンパ球減少症、特定の免疫抑制療法(インフリキシマブ、アレムツズマブ、イブルチニブ、フィンゴリモドなど)
臨床症候群の分類(抗真菌薬の選択・治療期間と関連する)
1. 中枢神経系疾患=クリプトコッカス髄膜炎
2. 播種性疾患 (Disseminated disease):肺以外の臓器への病変は播種性とする
3. 孤立性肺疾患 (Isolated pulmonary disease):subclinicalなこともある
・軽症:無症状または軽度な症状のみ、あるいは単発の小さな結節(2 cm未満)を持つ患者
・重症:多発性病変、大きな病変(2 cm以上)、大葉性肺炎像、空洞形成、多葉性病変、または低酸素血症を伴うもの
4. 直接皮膚接種 (Direct skin inoculation):通常は吸入感染から潜伏期間を経て再活性化するが、っ府へ直接接種する病態
検査
墨汁染色(india ink):感度:50-75%(HIV陽性:75%、HIV陰性:50%)
髄液クリプトコッカス抗原(latex):感度、特異度ともに90%以上→非常に有用
*Latex凝集法とEIA法があるが日本国内で採用されているのはlatex法のみ
*治療効果判定に使用することは出来ない
血清クリプトコッカス抗原:感度low/特異度high
真菌培養検査:診断のGold standard(3-5ml以上を提出することが望ましい)
下表:N Engl J Med 2024;390:1597-610.より
| 検査(髄液) | 感度 | 特異度 | PPV | NPV |
|---|---|---|---|---|
| クリプトコッカス抗原 | 99.3% | 99.1% | 99.5% | 98.7% |
| CSF培養 (CSF culture) | ||||
| 100 mm³ の場合 | 94.2% | 100% | 100% | 91.2% |
| 10 mm³ の場合 | 82.4% | 100% | 100% | 75.8% |
| 墨汁染色 | 86.1% | 97.3% | 98.2% | 80.2% |
| クリプトコッカス抗原ラテックス凝集アッセイ (Cryptococcal antigen latex agglutination assay) | ||||
| Meridian | 97.8% | 85.9% | 92.6% | 95.5% |
| IMMY | 97.0% | 100% | 100% | 95.3% |
| メタゲノム次世代シーケンシング | 93.5% | 96.0% | 87.8% | 98.0% |
| PCRアッセイ‡ | 82.0% | 98.0% | 98.0% | 79.0% |
画像所見
1:血管周囲腔、脳脊髄液にてcolony形成
・血管周囲腔の拡大:T2WI高信号、FLAIR高信号(血管周囲腔との違い)
・好発部位:基底核、視床、小脳、脳室周囲皮質下白質
・ゼラチン様偽嚢胞(gelatinuous pseudocysts):菌体が粘液物質を産生(血管周囲腔からの伸展)
2:肉芽腫性(Cryptococcoma):ring状、結節状の造影効果(さらに脳実質への伸展)
造影効果は細胞性免疫の状態と対応がある(免疫抑制状態では造影効果が少ない場合が多い)
治療
抗真菌薬(①導入:アムホテリシンB+フルシトシン⇒②地固め:フルコナゾール⇒③維持:フルコナゾール)
基本のレジメン
①導入療法:リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回
・導入療法の1週目または2週目の終わりに腰椎穿刺を行い、CSF培養の無菌性を確認することを検討すべきです。CSF培養が2週間で陽性のままである場合、導入療法を延長することを検討
②地固め療法:フルコナゾール400-800mg/日
③維持療法:フルコナゾール200mg/日
以下はGlobal guideline for the diagnosis and management of cryptococcosis: an initiative of the ECMM and ISHAM in cooperation with the ASMlobal guideline for the diagnosis and management of cryptococcosis: an initiative of the ECMM and ISHAM in cooperation with the ASM” Lancet Infect Dis 2024; 24: e495–512より
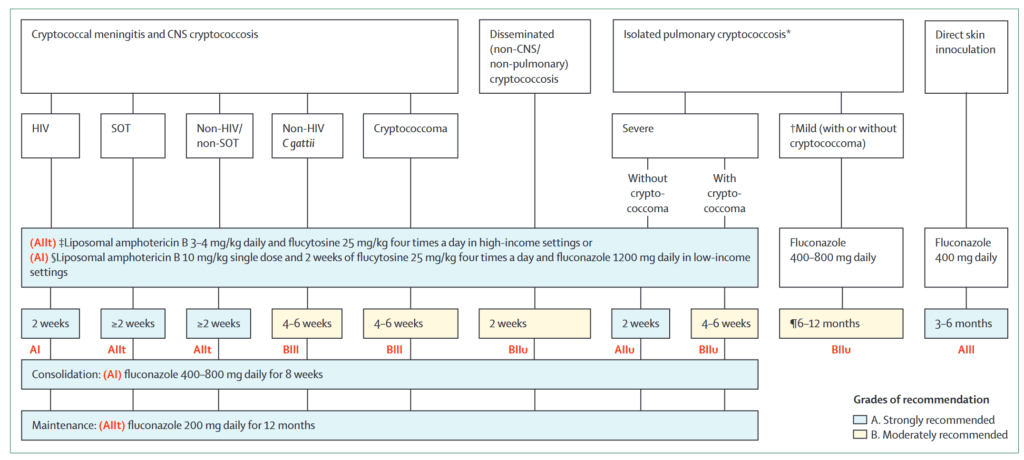
| 症候群 | 患者背景 | 導入療法 | 期間 | 地固め療法 | 期間 | 維持療法 | 期間 |
|---|---|---|---|---|---|---|---|
| クリプトコッカス髄膜炎およびCNSクリプトコッカス症 | HIV陽性者 | リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回 | 2週間 | フルコナゾール 400–800 mg/日 | 8週間 | フルコナゾール 200 mg/日 | 12ヶ月 |
| 固形臓器移植 | リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回 | 2週間 | フルコナゾール 400–800 mg/日 | 8週間 | フルコナゾール 200 mg/日 | 12ヶ月 | |
| 非HIV/非固形臓器移植 | リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回 | 2週間 | フルコナゾール 400–800 mg/日 | 8週間 | フルコナゾール 200 mg/日 | 12ヶ月 | |
| 非HIV C. gattii感染者(クリプトコッコーマなし) | リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回 | 2週間 | フルコナゾール 400–800 mg/日 | 8週間 | フルコナゾール 200 mg/日 | 12ヶ月 | |
| 非HIV C. gattii感染者 (クリプトコッコーマあり) | リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回 | 4–6週間 | フルコナゾール 400–800 mg/日 | 8週間 | フルコナゾール 200 mg/日 | 12ヶ月 | |
| 播種性(非CNS/非肺)クリプトコッカス症 | 全て | CNS疾患と同様に治療することが推奨されます。無菌部位からの分離株(CNS症状がない場合でも)やクリプトコッカス血症の場合、侵襲的な導入療法が考慮されるべきです。 | ≥2週間 | 4–6週間 | 6–12ヶ月 | AIIu | |
| 孤立性肺クリプトコッカス症 | 重症 | リポソームアムホテリシンB 3–4 mg/kg/日 + フルシトシン 25 mg/kg 1日4回 | 2週間 | 4–6週間 | 6–12ヶ月 | AIIu | |
| 軽度 | フルコナゾール 400 mg/日 | 6–12ヶ月 | なし | なし | BIIu¶ | ||
| 軽度 (クリプトコッコーマの有無にかかわらず) | フルコナゾール 400 mg/日 | 6–12ヶ月 | なし | なし | BIIu¶ | ||
| 直接皮膚接種 | 全て | フルコナゾール 400 mg/日 | 3–6ヶ月 | なし | なし | AIII |
髄液培養検査が2週間陽性の場合は導入療法を延長することを検討する
頭蓋内圧コントロール
・病態:酵母が直接くも膜顆粒を閉塞することで、髄液排泄を障害する
・急性症候性の頭蓋内圧亢進(CSF ≥20 cm)連日の治療的腰椎穿刺(通常20〜30 mLのCSF除去)によって管理し、圧力を開始圧の50%または20 cmH2O以下に低下させるべき(またはドレナージ、シャントといった外科的減圧を考慮すべき)
各薬剤に関して
アムホテリシン
分類:ポリエン polyene
作用:真菌細胞膜を構成するエルゴステロールに結合→細胞膜透過性亢進、不安定化(最初の抗真菌薬)、auto-oxidation→free radical細胞障害
代謝:腎(腎機能、肝機能による用量調節必要なし *透析で除去されないため透析患者でも同様)
特徴:重症真菌感染症第一選択(ほとんどすべての真菌に効果がある)
liposomal amphotericin B 商品名:アムビゾーム®
製剤:50mg/1V (1Vあたり注射用水12mlにて溶解する) + 5%ブドウ糖液250mlに溶解
*5%ブドウ糖液以外には混注不可
投与時間:1-2時間かけて投与(3時間かけてもよい)*deoxycholateよりは速く投与してよいとされている
投与量:Cryptococcus meningitisの場合 3-4mg/kg q24hr
副作用:とても多い
・腎機能障害(必発):pre-renal、輸入細動脈攣縮 80%程度に認める
*腎機能障害はAmpBの投与量と相関している
*基本的に腎障害なしに治療を終えることは難しいと考える(Cre-1.0mg/dl以下の患者が1.5-2.0mg/dl程度になって治療を終えることが多い)→腎機能は数か月経過して正常化することが多い
・頻回な腎機能、電解質のフォローは週2,3回はするべき
・尿細管障害による低K血症、低Mg血症→積極的補正が必要
・投与時反応(fever, chill, nausea)*高齢者、急速投与によりrisk上昇する *最初の1週間以内に多く、4-5日でtachyphylaxisが生じることで副作用は減弱することが多い
5-FC(flucytosine)
分類:フルオロピリジン系抗真菌薬
作用機序:真菌細胞内にて5-FUに変化し核酸合成阻害
一般名:フルシトシン 商品名:アンコチル®
製剤:500mg/錠
使用量:25mg/kg q6hr (=100mg/kg/day)
投与量の腎機能による調節
CCr>40ml/hr:25-50mg/kg q6hr
CCr=20-40ml/hr:25-50mg/kg q12hr
CCr=10-20ml/hr:25-50mg/kg q24hr
CCr<10ml/hr:50mg/kg q24hr以上
併用禁忌:TS-1
血中濃度測定:30-80μg/mlが目標治療域(100μg/ml以上では骨髄抑制のリスクが上昇する)
参考文献
以下はGlobal guideline for the diagnosis and management of cryptococcosis: an initiative of the ECMM and ISHAM in cooperation with the ASMlobal guideline for the diagnosis and management of cryptococcosis: an initiative of the ECMM and ISHAM in cooperation with the ASM” Lancet Infect Dis 2024; 24: e495–512より


